Термин «клеточный иммунитет» - это функция Т-кл (т-эффекторы = т-к и т-регуляторы=т-х)
- Т-киллеры – аналоги АТ в гуморальном ИО (завешают исполнительную работу клеточного ИО)
- Т-хелперы – участвуют в регуляции направления ИО
Клетки врожденного иммунитета (МФ, Дк, NK и др.) играют важную, но вспомогательную роль. Они не обеспечивают главное – специфичность адаптивного иммунитета.
От эффективности АГспецифичных Т-кл во многом зависит также функция гуморального иммунитета (Ig-АТ).
Происхождение Т-кл:
есть определенные закономерности в их развитии. На этот процесс оказывают влияние клетки врожденного иммунитета (МФ, NK, тучные клетки и др.) – определяют направление дифференцировки т-лф

Активация Т-клеточного ИО:

- В процессе лимфопоэза т-клетки получают АГраспознающие рецепторы (TCR), CD белки (корецепторы различной направленности, играющие роль рецепторов/лиганд; распознают белки гистосовместимости)
- После АГ стимула от АПК начинается иммунопоэз: превращение т-кл под действием цитокинов и других внешних воздействий в т-к/т-х 1 или 2 типа
NB!!! Т-киллеры не работают против клеток/частиц, не относящихся к собственным клеткам организма (т.е против бактерий, вирусов и т.д).
АГ-распознающие рецепторы (TCR)
у 90% Т-лф этот рецептор имеет альфа и бета цепи. На мембране ассоциированы с CD 3, образуя единый комплекс через CD 3 происходит передача сигнала с Т-кл рецептора внутрь клетки.
Когда происходит взаимодействие с АГ, случается «короткое замыкние» - передача сигнала в клетку
По сути это аналог Ig-рецепторов В-лф для распознавания АГ и МНС
у 5-10% Т-лф (Тх3) состав рецептора иной: гамма и дельта цепи, но общее строение сходное. Важный признак субпопуляций гамма и дельта: другое химическое строение полипептидных цепей
Существенное отличие TCR от ВСR:
у В-лф это фрагменты мономеров IgM и IgD, а у Т-лф – это тоже полипептидные цепочки, которые представляют собой димеры альфа и бета (их называют гетеродимеры), нет симметрии, как у рецепторов В-лф

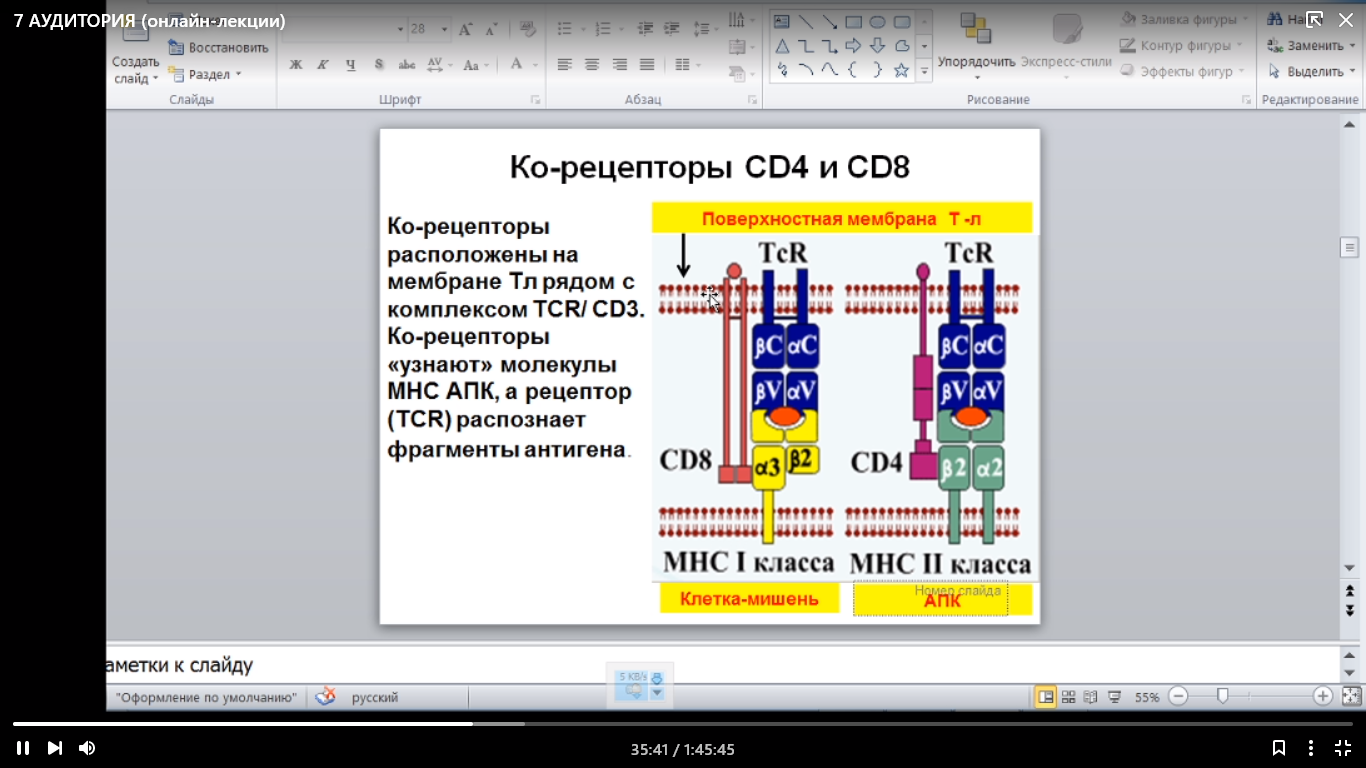
клетка-мишень – это клетка организма, которая имеет признаки чужеродности
оранжевый кружок – это детерминанта чужеродного
для TCR рецептора «своё» - это АГ
для CD белка «своё» - это белок гистосовместимости
но для организма АГ – это чужое
Функции отдельных субпопуляций Т-клеток
Подтипы зрелых Т-хелперов:
1 тип – включают клеточный ИО, продуцируют IL-12,2 IFN гамма и др. => активируют Т-киллеры
Так они обеспечивают и защиту организма от внутриклеточных паразитов, и от опухолевых клеток (они же работают против пересаженных клеток/органов).
Их избыток может провоцировать аутоиммунитет
2 тип -включают гуморальный ИО, синтезируют IL-4,5,10,6 и др. => активируют В-лф (то есть участвуют в образовании АТ)
Так они обеспечивают защиту от инфекций, внеклеточных патогенов, глистных инвазий, экзо и эндотоксинов (то есть всего, что еще не попало в клетку организма).
Участвуют в гиперчувствительности немедленного типа (ГЧНТ)
Основная локализация – под эпителием слизистых оболочек (дополняют гуморальный местный иммунитет sIgA).
3 тип (= Т-reg/T-supressor), имеют дополнительный CD25 – регулируют- гармонизируют активность 1 и 2 типов Т-хелперов (например, излишнее смещение ИО в сторону Т-х 2 типа – усиливается синтез IgE и развивается аллергическая реакция)
поддерживают толерантность к аутоАТ, подавляя аутоиммунные реакции
особенность: на стимуляцию АГ не отвечают пролиферацией
Но!! их избыток приводит к росту опухолей, персистирующим инфекциям, т.к они начинают подавлять ИО против опухолевых клеток, инфекционных патогенов
недостаток: срыв иммунологической толерантности, что проявляется в аутоиммунных и аллергических заболеваниям, патологии беременности
Открыты и другие субпопуляции Т-х (17, 22) – играют роль в провоспалительных и воспалительных процессах
CD белки Т-x: CD 45, CD 3 (обязательны для всех лимфоцитов) и CD 4
Т-киллеры
=эффекторы клеточного иммунитета
=цитотоксические Т-лф
- трансформируются из пре-CTL под влиянием Т-х1
- цитотоксическая активность проявляется в виде:
- разрушение перфоринами и гранзимами эукариотической клетки (!своей!) с признаками чужеродности (на поверхности т-к есть специальные адгезины, обеспечивающие прочное связывание с клеткой-мишенью)
перфорины – в некоем роде аналог МАК комплемента; они пробивают дырки, вставляют трубки, через которые проникают гранзимы, фрагментины и др.вещества, которые разрушают клетку; в клетку резко проникает вода и клетка разрывается
- гранзимы включают гены апоптоза клеток-мишеней
- активируют цитотоксическую функцию МФ и NK-кл

Ведущая роль Т-клеток в иммунитете:
- противовирусный иммунитет (т.к АТ не проникают внутрь клетки)
- реакции отторжения трансплантата
- онкоиммунитет
патологическое действие (побочная функция Т-клеток):
- аутоиммунные заболевания
- ГЗТ (гиперчувствительность замедленного типа)
Именно у Т-клеточного иммунитета ведущая роль в ИС
Иммунодефицит Т-типа (клеточный) более тяжелый, часто такие дети погибают или становятся тяжелыми инвалидами
Т-к постоянно патрулируют организм в поиске клеток с «иностранными» пептидами на поверхности, так как их наличие указывает на поражение клеток.
Так у больных ВИЧ нарушается соотношение между Т-х и Т-к: количество Т-х убывает (т.к ВИЧ чувствителен к CD4 – проникает в клетки, а Т-к уничтожают Т-х, МФ

У некоторых опухолевых или зараженных клеток имеются белки-рецепторы (PD-L1, CD112, CD155), которые при взаимодействии с Т-клетками вызывают блокировку ИО
Такие же ингибиторные действия могут быть на МФ и NK-кл
Это объясняет, почему ИС не распознает опухолевые процессы


Революционный прорыв в иммунотерапии опухолей
(Нобелевская премия 2018 года)
Получили Джеймс Эллисон и Таску Хондзё
Режим киллера Т-к против опухолевой клетки запускается только после того, как его поверхностный белок CD 28 свяжется с определенной молекулой-лигандом (В7 или 80,86) на опухолевой клетке
Но! Раньше это обычно успевает сделать другой белок на Т-к – CTLA-4, который блокирует цитотоксическую атаку против опухолевой клетки, то есть, конкурируя с CD28 за молекулы В7 на АПК, не дает Т-к активирующий сигнал
Эллисон открыл: CTLA-4 появляется на активированных Т-клетках специально для деактивации (этот белок схож по структуре с CD28 и тоже может связываться с В7 на поверхности Дк, даже сильнее, чем CD28
Тасуку Хондзё открыл: на поверхности Т-лф рецептор PD-1, связь которого с молекулами раковых клеток также подавляет антионкогенную активность Т-к
Таким образом, на каждой активированной Т-к есть ингибирующая молекула, которая конкурирует с активирующей молекулой за прием сигнала.
Сигнальные пути CTLA4 + B7 и PD1 + PD-L2 назвали чекпоинтами
Как «должно быть»: В7+CD28 стимулирует антионкогенную активность Т-лф

Как происходит на самом деле:

Полагают, что это нужно для блокировки избыточной аутоиммунной активности
Так опухоли одурачивали АПК. Что с этим делать? Как разозлить Т-к против опухолевых клеток?
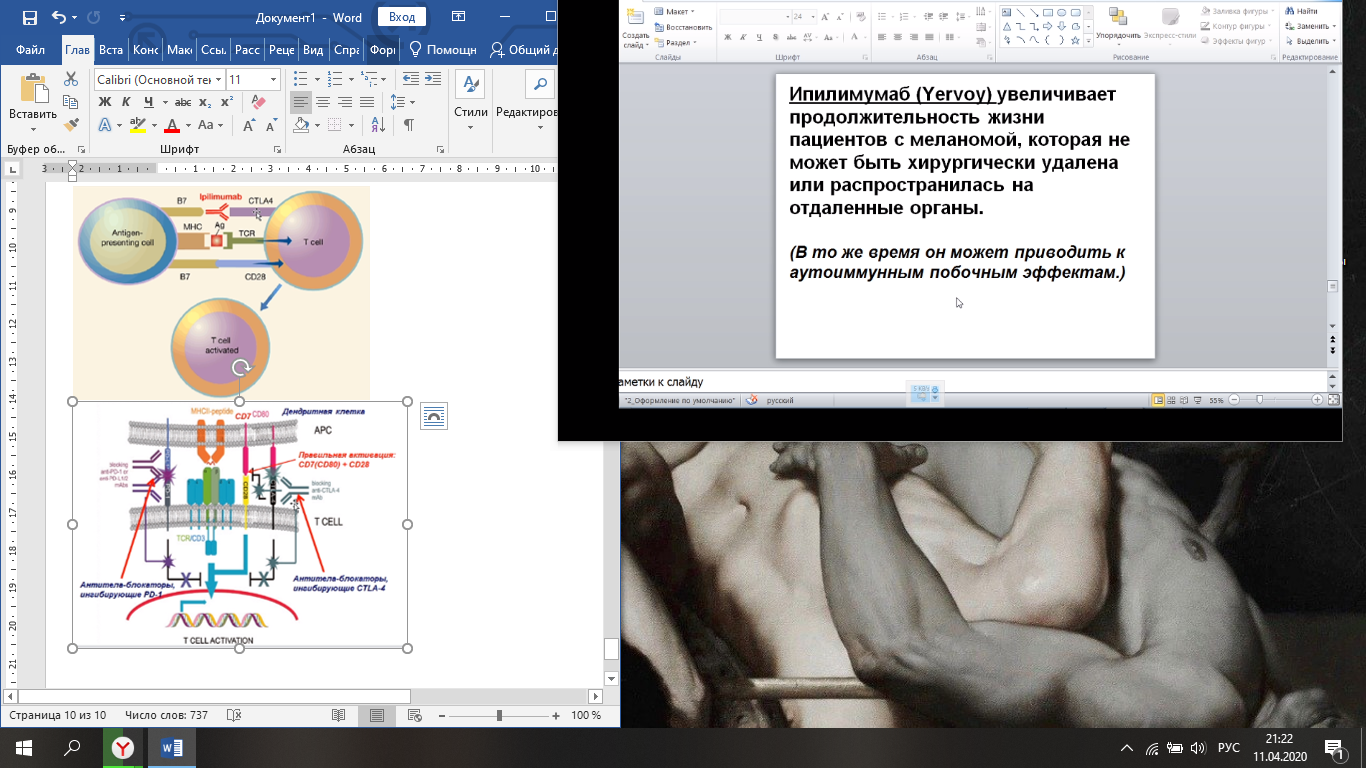
Ученые предложили связывать инактивирующие молекулы на Т-к, чтобы включить противоопухолевую активность Т-к. Для этой цели были разработаны и применены моноклональные АТ (Ipilimumab). Тогда активирующие молекулы Т-к беспрепятственно связываются с раковыми клетками и лимфоциты начинают убивать соответствующие клетки



 2020-05-25
2020-05-25 186
186






