Задание
1. Составить уравнение реакции горения смеси исходного газа (или паров жидкости) с воздухом.
2. Рассчитать температуру и давление при взрыве паров горючего с воздухом, если концентрация паров горючего нестехиометрическая, начальная температура смеси t0 ,оС, начальное давление р0, МПа.
3. Изучите методику расчета температуры и давления взрыва.
4. Недостающие для расчетов данные примите по таблице 26 – 27, приложения 3 [3].
Пример 2.
Рассчитать температуру и давление при взрыве паров ацетона в смеси с воздухом, если концентрация паров ацетона составляет 4%, начальная температура смеси 27оС и начальное давление 0,1 МПа.
Решение.
1.По табл. 26, прил. 3 [3] определяем теплоту горения ацетона Qг.в. (ΔНг):
Qг.в. (ΔНг) = 1789, 77 кДж/моль.
2.Составляем термохимическое уравнение реакции горения ацетона в воздухе.
СН3СОСН3 + 4(О2 + 3,76N2) → 3СО2 + 3Н2О + 15,04 N2 + 1789770Дж/моль
3.Концентрация ацетона исходной смеси составляет 4%. Поэтому произведем пересчет состава смеси, состоящей из трех компонентов – ацетона, кислорода, азота. Теоретический состав воздуха: 21% кислорода, 79% азота.
Итак,
концентрация кислорода
21(100 – 4)/100 = 20,16 %,
концентрация азота
79(100 – 4)/100 = 75,84 %.
4.Предположим, что сгорел 1 моль горючей смеси, тогда смесь будет иметь следующий состав:
ацетона – 0,04 моля = nг.в.
кислорода – 0,2016 моль = nО2
азота - 0,7584 = nN2
______________________________________________
всего – 1 моль = nг.с. (сумма молей исходной смеси).
5.Определяем внутреннюю энергию исходной смеси при температуре 27оС
(Т0 = 300К), по формуле (1): 
Qвн.эн.см.= 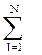 nг.с.СViТ0, Дж/моль.
nг.с.СViТ0, Дж/моль.
Величину СVi (мольную теплоемкость при постоянном объеме) определим из выражения (2). Принимаем по табл.26, прил. 3, [3] мольную теплоемкость при постоянном давлении, она равна
СР(ацетона) = 75,3Дж/(моль*К), СР(кислорода) = 29,37Дж/(моль*К),
СР(азота) = 29,1Дж/(моль*К).
Определяем мольную теплоемкость при постоянном объеме6
СV(ацетона) = 75,3 – 8,31 = 67 Дж/(моль*К),
СV(кислорода) = 29,37 – 8,31 = 21,06 Дж/(моль*К),
СV(азота) = 29,1 – 8,31 = 20,89 Дж/(моль*К).
6.Рассчитываем внутреннюю энергию исходной смеси по формуле (1):
Qвн.эн.см. = 0,04*300*67 + 0,2016*300*21,06 + 0,7584*300*20,89 = 6812,4Дж.
7.Определяем теплоту взрыва исходной смеси из расчета, что в горючей смеси содержится 0,04 моля ацетона, формула (3):
Qвзр = 0,04*1789770 + 6812,4 = 78403 Дж.
8.Определяем состав продуктов горения. Стехиометрические коэффициенты принимаем по термохимическому уравнению горения. При сгорании 0,04 моля ацетона выделится:
углекислого газа 0,04*3 = 0,12 моля = n(СО2);
паров воды 0,04*3 = 0,12 моля = n(Н2О).
При этом расходуется кислорода 0,04*4 = 0,16 моля, следовательно, избыток кислорода составит
n О2 = 0,2016 – 0,16 = 0,0416 моля.
Весь азот перейдет в продукты горения. Итак, состав продуктов горения следующий:
n(СО2) = 0,12 моля;
n(Н2О) = 0,12 моля;
n О2 = 0,0416 моля;
n N2 = 0,7584 моля.
Σ ni = 1,04 моля.
9.Определяем среднее значение внутренней энергии продуктов взрыва по формуле (4)
СV Твзр = Qвзр / Σni.
Отсюда СV Твзр = 78403,2 / 1,04 = 75387,7 Дж.
10. По табл. 27, прил. 3 [3] находим Твзр. Для этого сравниваем среднее значеие внутренней энергии СV Твзр = 75387,7 Дж со значениями внутренних энергий СО2, Н2О, О2, N2. Принимаем Твзр.= 2800К.
11. Определяем внутреннюю энергию продуктов взрыва по формуле (1):
Qп.г. = 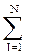 nп.г.СVп.г.Твзр, Дж/моль.
nп.г.СVп.г.Твзр, Дж/моль.
Внутреннюю энергию каждого компонента продуктов взрыва находим по табл. 27, прил. 3 [3].
Q2800 = 0,12*127300,5 + 0,12*100967,3 + 0,0416*74553,1 + 0,7584*70865,5 = 84237,56 Дж.
Сравниваем теплоту взрыва исходной смеси Qвзр = 78403,2 Дж с рассчитанной внутренней энергией продуктов взрыва.
Qвзр < Q2800,
следовательно, температура взрыва меньше 2800К.
Принимаем температуру Твзр = 2000К и определяем внутреннюю энергию продуктов взрыва:
Q2000 = 0,12*84502,8 + 0,12*65510,9 + 0,0416*51270,1 + 0,7584*48256,2 = 56731,98 Дж.
Сравниваем теплоту взрыва исходной смеси с внутренней энергией продуктов взрыва при 2000К:
Qвзр > Q2000.
Принимаем температуру взрыва 2200К и определяем внутреннюю энергию продуктов взрыва:
Q2200 = 0,12*95035,8 + 0,12*74092,2 + 0,0416*57210,8 + 0,7584*52819,4 = 62733,6 Дж.
Сравниваем теплоту взрыва исходной смеси с внутренней энергией продуктов взрыва при 2200К:
Qвзр > Q2200.
Следовательно, Твзр находится в интервале температур между 2200 и 2800К.
11.Методом линейной интерполяции определяем температуру взрыва паров ацетона с воздухом.
Твзр. = 2200 + (78403,32 – 62733)(2800 – 2200) / (84152,99 – 62733) = 2637,2К.
12.Рассчитываем давление при взрыве паров ацетона с воздухом по формуле(5):
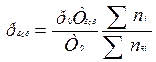 ,
,
где р0 = 0,1 МПа, Твзр = 2637,2 К, Т0 = 300 К, Σ ni = 1,04 моля, Σ nг.с. =1 моль.
Рвзр = 0,1* 2637,2 * 1,04 / (300* 1) = 0,91 МПа.
Ответ. Давление при взрыве паров ацетона составляет 0,91 МПа.
Содержание отчета
Отчет должен отвечать требованиям общих методических указаний по выполнению работ, содержать обоснованные выводы по результатам расчетов.
В отчете приведите результаты расчетов и ответы на контрольные вопросы.
Контрольные вопросы
1. Как рассчитать внутреннюю энергию газо- и паровоздушной смеси?
2. Какая смесь называется стехиометрической, а какая – нестехиометрической?
3. Как определить число молей каждого компонента горючей смеси?
4. Назовите пределы взрываемости паровоздушной смеси. От чего они зависят?
5. Какие факторы влияют на давление взрыва?
 2020-06-12
2020-06-12 1082
1082








