Щетинина Анастасия 10 «Б»
ЛАБОРАТОРНАЯ РАБОТА «ОПРЕДЕЛЕНИЕ ЗАРЯДА ЭЛЕКТРОНА»
Цель работы: определить заряд электрона.
ПРИБОРЫ И ПРИНАДЛЕЖНОСТИ: электролитическая ванна с раствором электролита, источник тока, амперметр, ключ, весы, секундомер, соединительные провода.
Ход работы:
Исследование №1
Определение заряда электрона.
Оборудование: Источник питания, амперметр лабораторный с пределом измерения 2 А., ключ, реостат, электролитическая ванна, электроды, раствор сульфата меди (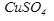 ), весы, разновесы.
), весы, разновесы.
Цель: Определить заряд электрона, используя законы электролиза.
Гипотеза: Заряд электрона должен получиться  .
.
Ход работы:
m 1 = 0, 11195 кг
m 2 = 0,11208 кг
M = 0,0635 кг/моль
n = 2
I = 0,5 А
t = 800 с.





Вывод: гипотеза доказана полностью e = 
Исследование №2
Определение заряда электрона при электролизе других солей.
Оборудование: Источник питания, амперметр лабораторный с пределом измерения 2 А., ключ, реостат, электролитическая ванна, электроды, раствор сульфата никеля, весы, разновесы.
Цель: Определить заряд электрона, используя законы электролиза.
Гипотеза: Заряд электрона должен получиться  , при использовании других солей.
, при использовании других солей.
Ход работы:
m 1 = 0,16247 кг
m 2 = 0.16259 кг
M = 0,059 кг/моль
n = 2
I = 0,5 А
t = 800 с.





Вывод: гипотеза доказана полностью e = 
Исследование №3
Определение заряда электрона при изменении силы тока
Оборудование: два источника питания, соединенных последовательно, амперметр лабораторный с пределом измерения 2 А., ключ, реостат, электролитическая ванна, электроды, раствор сульфата меди (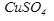 ), весы, разновесы.
), весы, разновесы.
Цель: Определить заряд электрона, используя законы электролиза.
Гипотеза: Заряд электрона должен получиться  .
.
Ход работы:
m 1 = 0,10856 кг
m 2 = 0.10884 кг
M = 0,0635 кг/моль
n = 2
I = 1 А
t = 852 с.





Вывод: гипотеза доказана полностью e = 
Исследование №4
Определение заряда электрона при изменении концентрации
раствора медного купороса.
Оборудование: Источник питания, амперметр лабораторный с пределом измерения 2 А., ключ, электролитическая ванна, электроды, раствор сульфата меди (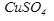 ), весы, разновесы.
), весы, разновесы.
Цель: Определить заряд электрона, используя законы электролиза.
Гипотеза: Заряд электрона должен получиться  .
.
Ход работы:
m 1 = 0,32797 кг
m 2 = 0, 32824 кг
M = 0,0635 кг/моль
n = 2
I = 1 А
t = 804 с.





Вывод: гипотеза доказана полностью e = 
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. В чем заключается процесс электролитической диссоциации?
Основная идея данной теории заключается в том, что электролиты под действием растворителя самопроизвольно распадаются на ионы. И именно эти ионы являются носителями заряда и отвечают за электропроводность раствора.
2. Что такое катод, анод, катион, анион? Что будет происходить в растворе электролита, если в него опустить два электрода? Что такое электролиз?
Катод - отрицательный электрод, анод — положительный. Положительные ионы — катионы, отрицательные ионы — анионы.
Если в р-р электролита опустить два электрода, по раствору пройдёт ток.
Электролиз - процесс выделения на электроде вещества, связанный с окислительно-восстановительными реакциями
3. Как влияет химический состав вещества, концентрация раствора и сила тока на результат опыта? На величину заряда электрона?
Чем выше концентрация р-ра, тем меньше заряд электрона.
Чем больше сила тока, тем больше заряд электрона.
4. Какая формула выражает зависимость между зарядом электрона и величинами, измеренными в ходе проведения опыта по электролизу? Какое числовое значение получено для заряда электрона?
 (Кл)
(Кл)
е = 1,6 *10-19 Кл
 2020-06-08
2020-06-08 857
857






