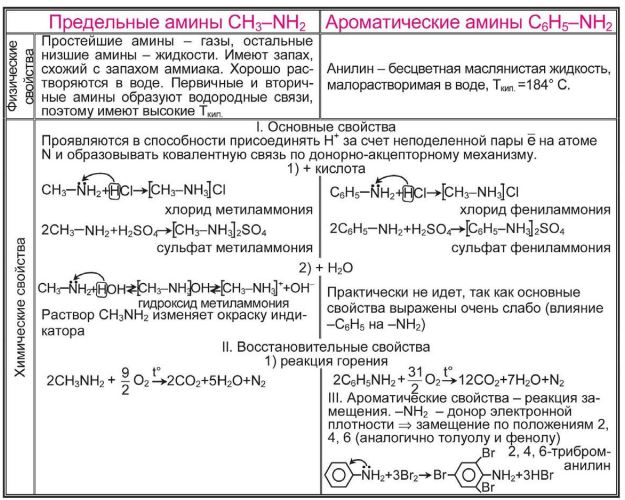
Химические свойства аминов определяются в основном наличием у атома азота неподеленной электронной пары.
Амины как основания. Атом азота аминогруппы, подобно атому азота в молекуле аммиака, за счет неподеленной пары электронов может образовывать ковалентную связь по донорно-акцепторному механизму, выступая в роли донора. В связи с этим амины, как и аммиак, способны присоединять катион водорода, т. е. выступать в роли основания:
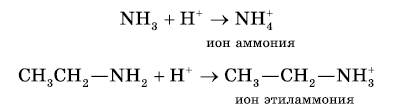
https://youtu.be/pI-wcKf4v50
https://youtu.be/3nenZjkvboI
1. Реакция амионов с водой приводит к образованию гидроксид-ионов:

https://youtu.be/BdP9Xgbe0xg
2. Реакция с кислотами. Аммиак, реагируя с кислотами, образует соли аммония. Амины также способны вступать в реакцию с кислотами:


С Н3─ СН2 ─ NH2 + Н2 SO4 →[ С Н3─ СН2 ─ NH 3 ] Н SO4 ↓
Основные свойства алифатических аминов выражены сильнее, чем у аммиака. Это связано с наличием одного и более донорных алкильных заместителей, положительный индуктивный эффект которых повышает электронную плотность на атоме азота. Повышение электронной плотности превращает азот в более сильного донора пары электронов, что повышает его основные свойства:

3. Горение аминов. Амины горят на воздухе с образованием углекислого газа, воды и азота:

4. Взаимодействие ароматического амина (анилина) с бромной водой
https://youtu.be/d_pxNj5sd8g
С6 Н5 NH2 + 3Br2 (вода) → С6 Н 2 Br 3 NH2 ↓ +3Н Br
ПОЛУЧЕНИЕ АМИНОВ
1. [С Н3─ СН2 ─ NH3 ] Сl + NаОH→ С Н3─ СН2 ─ NH2 + Nа Сl + Н2 О
2. С Н3─ СН2 Сl + 2 NH3 → С Н3─ СН2 ─ NH2 + NH 4 Сl
Кат.
3. С Н3─ СН2 ОН + NH3 → С Н3─ СН2 ─ NH2 + Н2 О
Кат.
4. С6 Н5 NО 2 + 6Н → С6 Н5 NH2 +2 Н2 О РЕАКЦИЯ ЗИНИНА
https://youtu.be/VILzXkBnXho
Применение аминов
Амины широко применяются для получения лекарств, полимерных материалов. Анилин — важнейшее соединение данного класса, которое используют для производства анилиновых красителей, лекарств (сульфаниламидных препаратов), полимерных материалов (анилинформальдегидных смол).

 2020-06-10
2020-06-10 726
726







