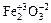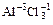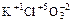Степень окисления – это условный заряд, возникающий на атоме, в результате полной или частичной отдачи или приема электронов. Обозначается СО.
Атомы, от которых полностью или частично смещены электроны, имеют положительную степень окисления.
Атомы, к которым присоединились или приблизились электроны, имеют отрицательную степень окисления.
Если атом принимает электроны, то степень окисления уменьшается, а если отдает, то увеличивается.
При написании химических формул на первое место, как правило, ставиться элемент с положительной степенью окисления (металл, водород или неактивный неметалл).
ПРАВИЛА ОПРЕДЕЛЕНИЯ СТЕПЕНЕЙ ОКИСЛЕНИЯ:
1. Степень окисления простых веществ равна нулю.
2. Степень окисления металлов всегда положительна и равна его валентности (исключение – соединения металлов друг с другом).
3. Степень окисления кислорода в большинстве случаев равна –2, в пероксидах –1, а в соединениях со фтором +1 или +2.
4. Степень окисления водорода в большинстве случаев равна +1, а в соединениях с металлами, кремнием и бором –1.
5. Суммарная степень окисления в любом сложном веществе равна нулю, т.е. общее число положительных зарядов (плюсов) должно всегда равняться общему числу отрицательных зарядов (минусов).
НАПРИМЕР: определить степени окисления в веществах:
| Fe2O3 По правилу 3 степень окисления О–2. По правилу 5 общее число минусов: –2*3= –6
Определяем СО железа: +6:2=+3. Ответ: | Na2S По правилу 2 степень окисления Na+1. По правилу 5 общее число плюсов: +1*2= +2
Определяем СО серы: –2:1=–2. Ответ: | AlCl3 По правилу 2 степень окисления Al+3. По правилу 5 общее число плюсов: +3*1= +3
Определяем СО хлора: –3:3=–1. Ответ: | H2
По правилу 1 СО простого вещества равна нулю.
Ответ: 
| NH3 По правилу 4 степень окисления Н+1. По правилу 5 общее число плюсов: +1*3= +3
Определяем СО азота: –3:1=–3. Ответ: | ZnI2 По правилу 2 степень окисления Zn+2. По правилу 5 общее число плюсов: +2*1= +2
Определяем СО йода: –2:2=–1. Ответ: | Mn2O7 По правилу 3 степень окисления О–2. По правилу 5 общее число минусов: –2*7= –14
Определяем СО марганца: +14:2=+7. Ответ: | KClO3 По правилу 2 степень окисления K+1. По правилу 3 степень окисления О–2. По правилу 5 общее число минусов: –2*3= –6
Определяем СО хлора: +1 + х = +6 х = +5
Ответ: | Al2(SO4)3 По правилу 2 степень окисления Al+3. По правилу 3 степень окисления О–2. По правилу 5 общее число минусов: –2*4*3= –24
Определяем СО серы: +3*2 + х*3 = +24 3х = +24–6 3х = +18 х = +6
Ответ: |
S8
По правилу 1 СО простого вещества равна нулю.
Ответ: 
|
 2020-06-08
2020-06-08 583
583 число плюсов тоже равно +6.
число плюсов тоже равно +6.