Лекция 9
Работа и энергия. Закон сохранения энергии









Задание 1. Составить конспект по схеме
I. Механическая работа
§ Понятие работы А и расчетная формула с пояснением каждой величины
§ рисунок 3.3., пояснить что такое 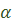
§ Записать формулу (3.4)
§ Единицы измерения работы в СИ
II. Мощность
§ Выписать что характеризует мощность
§ Понятие мощности и расчетная формула с пояснением каждой величины
§ Единицы измерения работы в СИ
III. Механическая энергия
§ Понятие «энергия»
§ Обозначение энергии, единицы измерения работы в СИ
Виды энергии
 | |||
 | |||
кинетическая энергия потенциальная энергия
 |  | ||||||
 | |||||||
 | |||||||
Выписать в каком случае тело обладает каждым видом энергии
Выписать формулы с пояснением каждой величины для каждого вида
§ Определение «консервативные силы»
§ Формула связи консервативных сил и потенциальной энергии
IV. Полная механическая энергия
§ Формулировка полной механической энергии и формула
V. Закон сохранения полной механической энергии
§ Формулировка закона
Практическая работа № 15 «Механическая работа. Мощность»
Задание: четные фамилии в списке -1 Вариант, НЕ четные-2 вариант


Контрольная работа № 3
«Законы сохранения в механике»

Лекция 10
Основные положения молекулярно-кинетической теории (МКТ). Размеры и масса молекул. Броуновское движение.
Существенный вклад в развитие молекулярно-кинетической теории сделал в середине 18в великий русский ученый М. В. Ломоносов.
Молекулярно-кинетической теорией называется учение о строении и свойствах вещества, использующее представления о существовании атомов и молекул как наименьших частицах химического вещества.
3 основных положения МКТ:
Любое вещество состоит из мельчайших частиц-молекул
Молекулы находятся в непрерывном движении
Молекулы способны взаимодействовать между собой - притягиваться и отталкиваться.
Молекула-это мельчайшая частица данного вещества, сохраняющая все его химические свойства и способная к самостоятельному существованию.
Так как известно, что молекулы состоят из атомов, то массу молекул удобно выражать в относительных атомных единицах массы (а. е. м.). Масса атома углерода равна 12 а.е.м. Атомные массы других атомов указаны в таблице Менделеева (см. после лекции 10 - приложение 1)
Например, масса атома водорода 1 а.е.м., атома азота-14 а.е.м., атома кислорода-16 а.е.м.

Относительную молекулярную массу вещества принято обозначать Mr. Например, относительная молекулярная масса воды Mr(H2O)= 1 а.е.м.·2 +16 а.е.м.=18 а.е.м.
Относительная молекулярная масса серной кислоты

Любое вещество состоит из частиц, поэтому количество вещества принято считать пропорциональным числу частиц. Обозначается 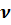 («нью»), единица измерения моль. Количество вещества можно найти с помощью формул:
(«нью»), единица измерения моль. Количество вещества можно найти с помощью формул:

Число молекул, содержащихся в одном моле любого вещества, есть величина постоянная и составляет 6·1023 моль-1. Это значение было найдено в 1811г итальянским физиком А. Авагадро и названа ПОСТОЯННАЯ АВАГАДРО.
Под молярной массой понимают массу вещества, взятого в количестве 1 моль. Молярная масса обозначается М, единицы измерения кг/моль.
Молярной массой М называется величина, равная отношению массы вещества m к количеству вещества 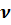 : М =
: М = 
Молярную массу М можно вычислить, пользуясь таблицей Менделеева
М= Mr ·10-3 кг/моль.
Например, молярная масса SO4 
М(SO4)= 32+16·2 =64 г /моль=64 · 10-3 кг /моль=0,064 кг/моль
Задание 1. Ответить на вопросы
1. Написать определение понятия «броуновское движение» и не менее трех примеров.
2. Написать определение понятия «диффузия» и не менее трех примеров.
 2020-06-29
2020-06-29 134
134






