Способы получения ацетилена
1. Ацетилен был открыт Г.Дэви в 1836 году в продуктах разложения метана, под действием искровых электрических разрядов.
2. В 1860 г. М. Бертло синтезировал ацетилен из простых веществ, пропуская водород через электрическую дугу между угольными электродами.
3. В 1862 г. Ф.Велер получил ацетилен из карбида кальция, действуя на него водой.
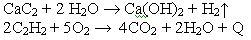
Химические свойства
Алкины во многих реакциях обладают большей реакционной способностью, чем алкены. Для алкинов, как и для алкенов, характерны реакции присоединения. Так как тройная связь содержит две π-связи, реакции присоединения к алкинам могут происходить в две стадии.
Вначале идет присоединение по месту двойной π-связи с образование производных олефинов, а затем по месту второй π-связи с образованием производных алканов.
Реакции присоединения для алкинов протекают медленнее, чем для алкенов. Это объясняется тем, что π-электронная плотность тройной связи расположена более компактно, чем в алкенах, и поэтому менее доступна для взаимодействия с различными реагентами.
Реакции присоединения
Гидрирование
Присоединение водорода происходит при нагревании в присутствии металлических катализаторов. Реакция протекает в две стадии: алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем образованием алканов (разрывается вторая π-связь):
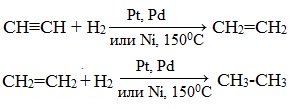
Галогенирование
Присоединение галогенов протекает также в две стадии. На первой стадии образуются дигалогеналкены, на второй – тетрагалогеналканы:
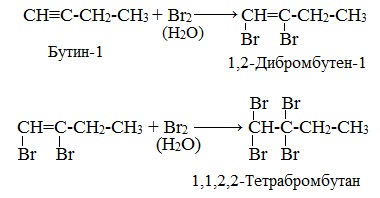
Реакция алкинов с бромной водой является качественной реакцией на алкины. Бромная вода обесцвечивается.
Гидрогалогенирование
Галогеноводороды присоединяются к алкинам в две стадии. Вторая стадия идет по правилу Марковникова. Присоединение НCl в отсутствии катализатора идет очень медленно. Катализатором этой реакции служат кислоты Льюиса – соли меди (I) и ртути (II):
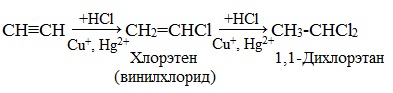
Получаемый продукт – хлористый винил (винилхлорид) – подобно этилену легко полимеризуется, образуя полимер – поливинилхлорид, который широко применяется в производстве поливинилхлоридных смол:
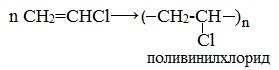
4. Гидратация (реакция Кучерова)
Присоединение воды протекает в присутствии солей ртути (II) при нагревании – HgSO4, Hg (NO3)2 – с образованием уксусного альдегида (при обычных условиях ацетилен с водой не взаимодействует):
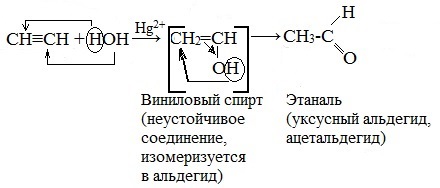
На первой стадии реакции образуется непредельный спирт, в котором гидроксильная группа находится непосредственно у атома углерода при двойной связи. Такие спирты принято назвать виниловыми или енолами. Отличительной чертой енолов является их неустойчивость. В момент образования они изомеризуются в более стабильные карбонильные соединения (альдегиды или кетоны) - водород гидроксильной группы переходит к соседнему атому углероду. При этом π-связь между атомами углерода разрывается и образуется π-связь между атомом углерода и атомом кислорода. Причиной изомеризации является большая прочность двойной связи С=О по сравнению с двойной связью С=С.
Реакции полимеризации
В присутствии катализаторов алкины могут реагировать друг с другом, причем в зависимости от условий образуются различные продукты.
1. Димеризация под действием водно-аммиачного раствора CuCl:
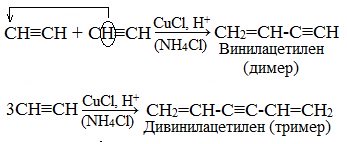
2. Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского):
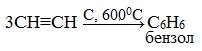
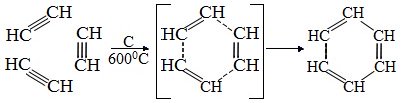
Реакции окисления
Горение
При сгорании алкинов происходит их полное окисление до СО2 и Н2О. Горение ацетилена сопровождается выделением большого количества тепла:
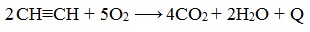
Неполное окисление
Ацетилен и его гомологи легко окисляются окислителями — КMnO4, K2Cr2O7. Алкины окисляются с разрывом молекулы по тройной связи. Строение продуктов окисления зависит от природы окислителя и условий проведения реакций.
Алкины обесцвечивают разбавленный раствор перманганата калия, что доказывает их ненасыщенность.
О кисление алкинов происходит без разрыва σ-связи С─С (разрушаются только π-связи).
Например, при взаимодействии ацетилена с разбавленным раствором КMnO4 при комнатной температуре образуется двухосновная щавелевая кислота:
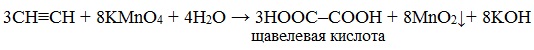
Применение алкинов
Наибольшее практическое значение имеют ацетилен и винилацетилен. Ацетилен используется для получения самых разнообразных веществ: уксусной кислоты, поливинилхлорида, синтетического каучука. Винилацетилен является важным промежуточным продуктом в производстве масло- и бензостойкого синтетического хлоропренового каучука.
ДОМАШНЕЕ ЗАДАНИЕ
1. Выполните тест:
2. Молекула ацетилена
1) линейная; 2) плоская; 3) тетраэдрическая; 4) зигзагообразная
3. Тип гибридизации атомов углерода в молекуле ацетилена
1) sp; 2) sp2; 3) sp3 4) spd
3. Число ϭ связей в молекуле бутин-1: 1) 4; 2) 3; 3) 9; 4) 1
4. Число π связей в молекуле пентин-2: 1) 1; 2) 2; 3) 3; 4) 4
5. Выберите соответствие:
| 1.Ацетилен | А) Форма молекулы тетраэдрическая |
| 2.Метан | Б) sp гибридизация атомов углерода |
| 3.Этилен | В) Число ϭ-связей равно 6 |
| 4.Пропин | Г) второе валентное состояние атомов углерода |
2. З адание:
1. Из приведенного перечня веществ выпишите вещество, которое называется пентин-1 и подберите ему изомер отсюда же.

2. Зная, что у ацетилена на два атома водорода меньше, чем у этилена, предложите способ его получения. Напишите соответствующее уравнение реакции получения ацетилена из алкенов в тетрадь.
3. Осуществите цепочку превращений: СаСО3 → СаО → СаС2 → С2Н2 → СНзСНО
4. Из каких мономеров можно получить полимеры?
УРОК № 58
Тема: Арены. Бензол
Базовые понятия и термины: арены, π -электронное облако, ароматическая связь, бензольное кольцо, формула Кекуле, реакции окисления, замещения и присоединения
Смотреть по ссылке: https://www.youtube.com/watch?v=8jkl7KCAAG8
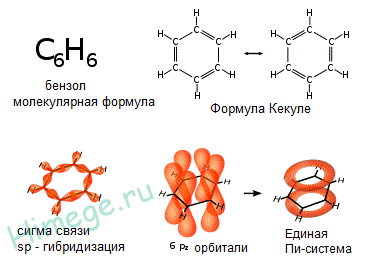
Ароматические углеводороды – соединения углерода и водорода, в молекуле которых имеется бензольное кольцо. Важнейшими представителями ароматических углеводородов являются бензол и его гомологи – продукты замещения одного или более атомов водорода в молекуле бензола на углеводородные остатки.
 2020-06-29
2020-06-29 405
405







