ФАРМАЦЕВТИЧЕСКИЙ ФИЛИАЛ
ГБОУ СПО «СВЕРДЛОВСКИЙ ОБЛАСТНОЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ»
Кафедра химии и фармацевтической технологии
АМИНОКИСЛОТЫ
Учебное пособие для самостоятельной работы студентов по учебной дисциплине «Органическая химия»
Екатеринбург
2013
Пособие для самостоятельной работы студентов по общей и неорганической химии / сост. преподаватель химии Т.В. Главатских – Екатеринбург; Фармацевтический филиал ГБОУ СПО «СОМК», 2012. – 15 с.
Рецензент: Лужкова И.В., научный сотрудник ФГУБН Института химии твердого тела УрО РАН.
Учебное пособие для самостоятельной работы по теме: «Аминокислоты» в виде обучающего текста, содержит несколько разделов. В нем отражены вопросы, связанные с определением, классификацией, изомерией, свойствами аминокислот. Пособие знакомит студентов с физическими и химическими свойствами аминокислот. Пособие содержит задания по номенклатуре, изомерии, химическим свойствам аминокислот. Материал тесно взаимосвязан с профессиональной направленностью: некоторые аминокислоты являются лекарственными препаратами, a - аминокислоты играют важную роль в жизнедеятельности организма.
Данное пособие позволяет подготовиться изучению ПМ 02 МДК 02.02. «Контроль качества лекарственных средств».
Учебное пособие рассмотрено на заседании кафедры химии и фармацевтической технологии (протокол № 2 от 06 сентября 2013 года)
СОДЕРЖАНИЕ:
|
1. ОПРЕДЕЛЕНИЕ.
2. КЛАССИФИКАЦИЯ.
3. НОМЕНКЛАТУРА.
4. ФИЗИЧЕСКИЕ СВОЙСТВА.
5. ХИМИЧЕСКИЕ СВОЙСТВА.
6. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ АМИНОКИСЛОТ,
ПРИМЕНЕНЯЕМЫЕ В МЕДИЦИНЕ.
7. ЛИТЕРАТУРА
8. ПРИЛОЖЕНИЕ
1. ОПРЕДЕЛЕНИЕ.
АМИНОКИСЛОТЫ – гетерофункциональные органические соединения, производные карбоновых кислот, в радикале которых один или более атомов водорода замещены на аминогруппу.
Общая формула аминокислот:
H
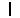
R  C
C  COOH
COOH
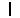
NH2
2. КЛАССИФИКАЦИЯ АМИНОКИСЛОТ.
I. По характеру углеводородного радикала
- Предельные СН3 – СН – СООН
|
NH2 аланин
- 
 Ароматические
Ароматические
– СН2 – СН – СООН
 |
|
NH2 фенилаланин
-
|


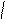
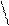 Гетероциклические – СН2 – СН – СООН
Гетероциклические – СН2 – СН – СООН
|
|
|
|
II. По количеству – СООН групп
- Одноосновные NH2 – CH2 – COOH глицин
- Двухосновные HOOC – CH2 – CH – COOH
|
NH2 аспарагиновая
кислота
III. По количеству – NH2 групп
- Одна -NH2 группа СH3 – CH – СН – COOH
| |
CH3 NH2 валин
- Две -NH2 группы СH2 – CH2 – СН2 – СН2 – СН – COOH
| |
NH2 лизин NH2
3. НОМЕНКЛАТУРА.
1. Для аминокислот, участвующих в построении белков, применяются в основном тривиальные названия.
2. Заместительная номенклатура (вариант систематической номенклатуры ИЮПК).
Задание:
Заполните таблицу. Дайте название аминокислотам по заместительной номенклатуре.
| ФОРМУЛА АМИНОКИСЛОТЫ | ТРИВИАЛЬНОЕ НАЗВАНИЕ | ПО ЗАМЕСТИТЕЛЬНОЙ НОМЕНКЛАТУРЕ |
1. H2N  CH2 CH2  COOH
2. H3C COOH
2. H3C  СН СН  COOH COOH
 NH2
3. NH2 –CH2–CH2–COOH
4.H3C
NH2
3. NH2 –CH2–CH2–COOH
4.H3C  CH CH  CH CH  COOH
| |
CH3 NH2 COOH
| |
CH3 NH2
| Глицин, гликокол α - аланин β - аланин валин | ? ? ? ? |
ИЗОМЕРИЯ.
Для аминокислот характерны два вида изомерии:
1. Структурная или изомерия строения
2. Стереоизомерия или пространственная изомерия
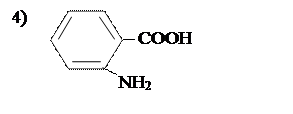
Задание: выбрать изомеры и дать им название:
| |||||||
 | |||||||
| |||||||
 | |||||||
| |||||||
Задание: Из предложенных аминокислот выберите те, которые способны существовать в виде энантиомеров
1) 2-аминопропановая кислота
2) 2-амино-2-метилпропановая кислота
3) 4-аминобутановая кислота
Определить асимметричный атом углерода; составить формулы Фишера для энантиомеров.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ: все аминокислоты, входящие в состав белков, относятся к L-ряду.
4. ФИЗИЧЕСКИЕ СВОЙСТВА. Алифатические аминокислоты являются
белыми кристаллическими порошками, мало растворимые в холодной воде, лучше в горячей, нерастворимые в органических растворителях.
Если аминокислота имеет 1 карбоксильную и 1 аминогруппу в α-положении, то реакция водных растворов на лакмус нейтральная. Это объясняется тем, что карбоксильная и аминогруппа взаимодействуют с образованием так называемых внутренних солей.
Внутренние соли - это соли, образующиеся в результате взаимодействия кислотных и основных групп, находящихся в пределах одной и той же молекулы



 O O
O O

 R – CH – C → R – CH – C
R – CH – C → R – CH – C
| OH | O-
H2N NH3+
Об образовании внутренних солей свидетельствует и малая растворимость их в органических растворителях.
Двухосновные кислоты, содержащие две карбоксильных группы и одну аминогруппу в α-положении, имеют кислую реакцию, а диаминокислоты, имеющие две аминогруппы и одну карбоксильную группу обладают щелочной реакцией.
5. ХИМИЧЕСКИЕ СВОЙСТВА алифатических аминокислот
ЗАДАНИЕ:
Запишите общую формулу алифатических аминокислот и найдите:
1. Кислотный и основный центр.
2. Электрофильный и нуклеофильный центр.
Исходя из химического строения, предположите в какие реакции
будут вступать аминокислоты. Используйте свои знания из темы “Карбоновые кислоты”, “Амины”.
Аминокислоты будут проявлять:
1. Кислотно-основные свойства, т.е. они являются амфотерными соединениями.
В щелочной среде аминокислоты существуют в виде анионов, в кислой – в виде катионов.

2. Так как аминокислоты – это гетерофункциональные соединения, то им присущи реакции карбоновых кислот и аминов.
(Ряд этих реакций имеет свои особенности, вызванные одновременным присутствием двух функциональных групп)
3. Специфические реакции (подобно гидроксикислотам).
(Их появление обусловлено наличием в молекуле аминокислот двух различных функциональных групп.)
Задание: составить схему реакций:
Реакции по карбоксильной группе
 2020-09-24
2020-09-24 207
207







