При прохождениии тока по проводнику проводник нагревается, и происходит теплообмен с окружающей средой, т.е. проводник отдает теплоту окружающим его телам.
Количество теплоты, выделяемое проводником с током в окружающую среду, равно произведению квадрата силы тока, сопротивления проводника и времени прохождения тока по проводнику.
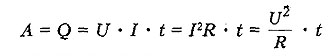
По закону сохранения энергии количество теплоты, выделяемое проводником численно равно работе, которую совершает протекающий по проводнику ток за это же время.
Мощность тока.
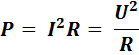 По закону Ома для полной цепи U = Ir – ε. Тогда, учитывая, что знак ЭДС противоположен знаку силы тока, получим
По закону Ома для полной цепи U = Ir – ε. Тогда, учитывая, что знак ЭДС противоположен знаку силы тока, получим 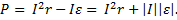 Когда аккумулятор разряжается
Когда аккумулятор разряжается 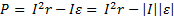 .
.
Мощность на участке цепи, содержащем ЭДС, может как потребляться этим участком цепи, так и передаваться в цепь.
_____________________________________________________________________________________________
Билет №8.
1. Свойства поверхности жидкости. Поверхностная энергия. Сила поверхностного натяжения. Влияние примесей на поверхностное натяжение.
2. Электрический ток в электролитах. Законы электролиза. Применение электролиза.
3. Задача на основное уравнение молекулярно-кинетической теории.
4. Задача на определение параметров электрической цепи.
_____________________________________________________________________________________________
1. Свойства поверхности жидкости. Поверхностная энергия. Сила поверхностного натяжения. Влияние примесей на поверхностное натяжение.
Поверхность жидкости стремится к сокращению. Многочисленные опыты и наблюдения показывают, что жидкость принимает такую форму, при которой ее свободная поверхность имеет наименьшую площадь. В своем стремлении сократиться поверхностная пленка придавала бы жидкости сферическую форму, если бы не притяжение к Земле. Чем меньше капелька, тем большую роль играют поверхностные силы по сравнению с объемными (силами тяготения). Молекулы поверхностного слоя находятся в среднем на больших расстояниях друг от друга, чем молекулы внутри жидкости.
Молекулы поверхностного слоя жидкости обладают избытком потенциальной энергии по сравнению с энергией, которой эти молекулы обладали бы, находясь внутри жидкости. Избыточную потенциальную энергию, которой обладают молекулы на поверхности жидкости, называют поверхностной энергией. С макроскопической (термодинамической) точки зрения поверхностная энергия – это один из видов внутренней энергии, отсутствующих у газов, но имеющаяся у жидкостей. Отношение поверхностной энергии Uп участка поверхности жидкости к площади S этого участка есть величина постоянная, не зависящая от площади S. Эту величину называют коэффициентом поверхностного натяжения или просто поверхностным натяжением: σ = Uп/S. Поверхностное натяжение представляет собой удельную поверхностную энергию, приходящуюся на единицу площади. В СИ поверхностная энергия выражается в 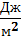 . Так как 1 Дж = 1 Н*м, то поверхностное натяжение можно выражать в
. Так как 1 Дж = 1 Н*м, то поверхностное натяжение можно выражать в  .
.
Силу, которая действует вдоль поверхности жидкости перпендикулярно линии, ограничивающей эту поверхность, и стремится сократить ее до минимума, называют силой поверхностного натяжения. Чтобы измерить силу поверхностного натяжения, проделаем следующий опыт. Возьмем прямоугольную проволочную рамку, одна сторона которой AB длиной Ɩ может перемещаться с малым трением в вертикальной плоскости. Погрузив рамку в сосуд с жидким раствором, получим на ней жидкую пленку. Как только мы вытащим рамку из мыльного раствора, проволочка AB сразу же придет в движение. Мыльная пленка будет сокращать свою поверхность. Следовательно, на проволочку AB действует сила, направленная перпендикулярно проволочку в сторону пленки. Это и есть сила поверхностного натяжения.
От чего зависит сила поверхностного натяжения. Если проволочку переместить вниз на расстояние h, то внешняя сила F1 = 2F совершит работу: A = F1h = 2Fh. Согласно закону сохранения энергии эта работа равна изменению энергии (в данном случае поверхностной) пленки. Начальная поверхностная энергия мыльной пленки площадью S1 равна Uп1 = 2σS1, так как пленка имеет 2 поверхности одинаковой площади. Конечная поверхностная энергия Uп2 = 2σS2, где S2 – площадь пленки после перемещения проволочки на расстояние h. Следовательно,A = Uп2 – Uп1 = 2σS2 - 2σS1 = 2σ(S2 – S1).
Так как S2 – S1 = Ɩh, то A = 2σƖh. Приравнивая правые и левые части, получим: 2Fh = 2σƖh. Отсюда сила поверхностного натяжения, действующая на границу поверхностного слоя длинойƖ, равна: F = σl. Направлена сила поверхностного натяжения по касательной к поверхности перпендикулярно границе поверхностного слоя (перпендикулярно проволочке AB в данном случаи).
Зависимость поверхностного натяжения от примесей. Значительное влияние на поверхностное натяжение жидкости оказывают примеси растворенных в ней веществ. Наличие примесей в жидкости приводит, как правило, к уменьшению поверхностного натяжения.
2. Электрический ток в электролитах. Законы электролиза. Применение электролиза.
Заряженные частицы, обеспечивающие электрический ток в растворах, образуются в результате электролитической диссоциации. Из-за взаимодействия с полярными молекулами воды молекулы растворяемых веществ распадаются на разноименно заряженные “осколки” – ионы. Положительно заряженными оказываются ионы металлов и водорода, а отрицательно заряженными – кислотные остатки и гидроксильная группа (OH). Степень диссоциации, т.е доля молекул растворенного вещества, которые распадаются на ионы, зависит от температуры, концентрации раствора и диэлектрической проницаемостью растворителя. С увеличением температуры степень диссоциации возрастает и, следовательно, увеличивается концентрация положительно и отрицательно заряженных ионов. Наряду с процессом диссоциации в растворах электролитов происходит и обратный процесс. Ионы различных знаков при встрече могут снова объединиться в нейтральные молекулы – рекомбинировать (воссоединяться). При отсутствии внешнего электрического поля ионы вместе с нераспавшимися молекулами находятся в хаотическом тепловом движении. Если сосуд с раствором электролита включить в электрическую цепь, то между электродами образуется электрическое поле и ионы в растворе придут в упорядоченной движение. Положительно заряженные ионы станут двигаться по направлению напряженности поля, т.е к катоду (электроду, соединенному с отрицательным полюсом источника тока), а отрицательно заряженные ионы – в противоположном направлении, т.е к аноду (электроду, соединенному с положительным полюсом источника тока). Отрицательные ионы, пришедшие к аноду и называемые поэтому анионами, отдают свои лишние электроны аноду. Положительные ионы, пришедшие к катоду и потому называемые катионами, получают недостающие им электроны из избытка их на катоде. При этом через раствор электролита заряд переносится вместе с частицами вещества ионами. Такую проводимость называют ионной.
Электролиз. Процесс выделения на электродах вещества, связанных с окислительно-восстановительными реакциями, называется электролизом. Масса m выделившегося вещества равна произведению массы одного иона mi, на число ионов N, осевших на электроде. Масса иона равна:
mi = 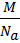 , где M – молярная масса, Na – число Авогадро. Число ионов осевших на электроде, Ni =
, где M – молярная масса, Na – число Авогадро. Число ионов осевших на электроде, Ni = 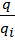 , где
, где
q = It заряд протекший через раствор электролита за время t, qi – заряд иона, который равен произведению заряда электрона на валентность атома: qi = e*n. m = 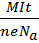
Закон Фарадея. Обозначим через k коэффициент пропорциональности между массой вещества m и зарядом q= It: k = 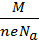 . Тогда m = kIt. Следовательно, масса вещества, выделившегося на каждом из электродов, прямо пропорциональна силе тока и времени прохождения тока через раствор электролита. Коэффициент k называют электрохимическим эквивалентом вещества и выражают в
. Тогда m = kIt. Следовательно, масса вещества, выделившегося на каждом из электродов, прямо пропорциональна силе тока и времени прохождения тока через раствор электролита. Коэффициент k называют электрохимическим эквивалентом вещества и выражают в 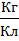 .
.
Постоянная Фарадея. Произведение элементарного заряда e на число Авогадро Na, носит название постоянной Фарадея: F = eNa. Тогда: m = 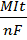 . Постоянная Фарадея численно равна заряду, который надо пропустить через раствор электролита, чтобы выделить на электроде один моль одновалентного вещества. Постоянная Фарадея равна F = 9.65*10000 Кд/моль.
. Постоянная Фарадея численно равна заряду, который надо пропустить через раствор электролита, чтобы выделить на электроде один моль одновалентного вещества. Постоянная Фарадея равна F = 9.65*10000 Кд/моль.
Применение электролиза. Гальваностегия – покрытие металлических изделий тонким слоем другого металла с целью предохранения от окисления и придания изделию привлекательного внешнего вида (оцинковка или хромирование). Гальванопластика – электролитическое изготовление копий с рельефных предметов. Рафинирование меди – очищение меди от примесей.
Получение алюминия. Для этого подвергают электролизу не растворы солей этого металла, ап его расплавленные оксиды.
_____________________________________________________________________________________________
Билет №9.
1. Кристаллические и Аморфные тела, их свойства. Виды кристаллов. Их свойства. Анизотропия.
2. Электрический ток в газах. Самостоятельный и несамостоятельный разряд. Типы самостоятельных разрядов. Понятие о плазме.
3. Задача на абсолютную и относительную влажность.
4. Задача на определение ЭДС и внутреннего сопротивления источника тока.
_____________________________________________________________________________________________
1. Кристаллические и Аморфные тела, их свойства. Виды кристаллов. Их свойства. Анизотропия.
Кристаллы. Кристаллом называют тело определенной геометрической формы, ограниченное естественными плоскими гранями. Тело представляющее собой один кристалл, называется монокристаллом. Но большинство кристаллических тел состоит из множества беспорядочно расположенных и сросшихся между собой мелких кристалликов. Такие тела называют поликристаллическими. Кристаллы различных веществ имеют разнообразную форму и размеры. Размеры кристаллов поликристаллического типа могут с течением времени изменяться. Так например мелкие кристаллы стали и железа переходят в крупные. Этот переход ускоряется при ударах и сотрясениях. Очень многие тела одинакового химического состава в кристаллическом состоянии в зависимости от условий могут существовать в двух и более разновидностях(модификациях). Это свойство называют полиморфизмом. Существенным свойством монокристалла является анизотропия – неодинаковость его свойств (механических, электрических, тепловых) по разным направлениям. О неодинаковости теплового расширения кристалла по разным направлениям можно заключить из следующего опыта. Если из монокристалла, например кварца, изготовить тело шарообразной формы и нагреть его, то после нагревания оно уже не будет шарообразным. Вдоль трех взаимно перпендикулярных диаметров тело расшириться неодинаково и, вместо шара получаем так называемый эллипсоид. Поликристаллические тела изотропны, т.е обнаруживают одинаковые свойства по разным направлениям. Это объясняется тем, что кристаллики, из которых состоит поликристаллическое тело, ориентированы друг по отношению к другу хаотически. В результате нм одно из направлений не отличается от других.
существует 4 типа кристаллов: молекулярные, ковалентные (или атомные), ионные и металлические. Во всех видах кристаллов образующие их частицы (молекулы, атомы, ионы) располагаются таким образом, что их энергия оказывается минимальной. К молекулярным кристаллам относятся кристаллы водорода, азота, брома, нафталина и др. Прочность всех этих кристаллов невелика. Ковалентные кристаллы. К ковалентным кристаллам относится алмаз, полупроводники кремний и германий, а также многие соединения. Ионные кристаллы. Коллективизация валентных электронов связывает также атомы ионных кристаллов. К их числу относятся неорганические соединения. Но в ионных кристаллах, например в кристалле поваренной соли, коллективизация электронов в сущности сводится к экспроприации хлором одного электрона у натрия. Все ковалентные электроны движутся по узлам решетки, занятых хлором, и кристалл фактически состоит из ионов противоположных знаков. Связь в этом случаи обеспечивается электростатическими силами притяжения. Металлические кристаллы. При образовании куска металла из отдельных атомов валентные электроны полностью утрачивают связь со своими атомами и «собственностью» всего куска в целом. Положительные ионы окружены «электронным газом», образованным коллективизированными электронами.
2. Электрический ток в газах. Самостоятельный и несамостоятельный разряд. Типы самостоятельных разрядов. Понятие о плазме.
Изолирующие свойства газов (воздуха) объясняются отсутствием в них свободных электрических зарядов: атомы и молекулы газов в естественном состоянии являются нейтральными. Процесс протекания тока через газы называют электрическим разрядом в газах. Распад молекулы на электроны и положительные ионы называют ионизацией газа. Нагревание газа до высокой температуры не является единственным способом ионизации молекул или атомов газа. Нейтральные атомы или молекулы могут ионизироваться под воздействием других факторов, важнейшими из которых являются рентгеновские лучи и излучения радиоактивных веществ, ультрафиолетовые лучи и т.д. Факторы, вызывающие ионизацию газа называют ионизаторами. В ионизированном газе имеются носители зарядов трех сортов: электроны, положительные ионы, отрицательные ионы. Процесс ионизации газа сопровождается противоположным ему процессом восстановления нейтральных молекул из разноименно заряженных ионов вследствие их электрического (кулоновского) притяжения. Такой процесс называют рекомбинацией заряженных частиц. Если действие ионизатора неизменно, то в ионизированном газе устанавливается динамическое равновесие, при котором в единицу времени восстанавливается столько же молекул, сколько их распадается на ионы. Наличие заряженных частиц в газе – явление временное (пока действует ионизатор). Электрический ток в газе представляет собой направленное движение положительных ионов к катоду, а отрицательных ионов и электронов – к аноду. В газах сочетается электронная проводимость, подобная проводимости металлов, с ионной проводимостью, подобной проводимости водных растворов или расплавов электролитов.
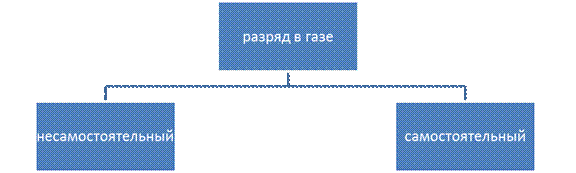
Рассмотренный выше механизм прохождения электрического тока через газы при постоянном воздействии на газ внешнего ионизатора представляет собой несамостоятельный заряд, так как при прекращении действия ионизатора прекращается и ток в газе.
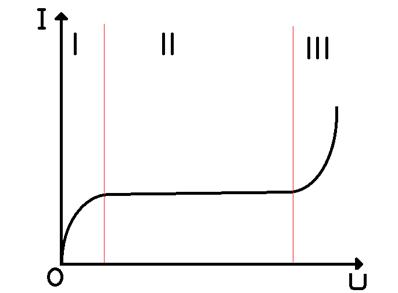
| - несамостоятельный заряд
|| - насыщение газа
- самостоятельный заряд
При некотором определенном напряжении наступает такой момент, при котором все заряженные частицы, образующиеся в газе ионизатором за секунду, достигают за это же время электродов. Дальнейшее увеличение напряжения уже не может привести к увеличению числа переносимых ионов. Ток, как говорят, достигает насыщения (горизонтальный участок графика).
Самостоятельный заряд.
Если после достижения продолжать увеличивать разность потенциалов между электродами, то сила тока при достаточно большом напряжении станет резко возрастать. Число заряженных частиц может стать таким большим, что внешний ионизатор уже не нужен для поддержания заряда. Поскольку разряд не нуждается для своего поддержания во внешнем ионизаторе, его называют самостоятельным разрядом.
Типы самостоятельного разряда.
Тлеющий разряд.
При давлении 1 – 2мм. Рт. Ст и ниже возникает тлеющий разряд. Вблизи катода происходит катодное падение потенциала. Это обусловливает эмиссию электронов из металла катода. Основными процессами, поддерживающими заряд, являются ионизация электронными ударами в объеме и вторичная электронная эмиссия на катоде. Все это происходит благодаря существованию катодного падения потенциала. Следовательно, катодное падение потенциала есть наиболее характерный признак тлеющего разряда.
Тлеющий разряд используют в трубках для рекламы. Важнейшее применение тлеющий разряд получил в газовых лазерах.
Коронный разряд.
При атмосферном давлении в газе, находящимся в сильно неоднородном электрическом поле (около остриев, проводов линий высокого напряжения), наблюдается разряд, светящаяся область которого часто напоминает корону. Разряд наступает, когда напряженность поля превышает 3 * 10 ** 6 в/м. С давних времен это свечение называют огнями святого Эльма. Коронный разряд приводит в утечке электроэнергии, поэтому высоковольтные провода должны быть толстыми.
Искровой разряд.
При большой напряженности электрического поля (около 3 * 10 ** 6 в/м) между электродами при атмосферном давлении возникает искровой разряд. Искровой разряд в отличие от коронного приводит к пробою воздушного промежутка. При искровом разряде возникаю каналы ионизированного газа – стриммеры, имеющие вид прерывистых ярких зигзагообразных нитей. Этот разряд нашел применение в двигателях внутреннего сгорания в автомобильных свечах.
Молния.
Пример гигантского искрового разряда – молния. Сила тока в молнии достигает 500 000 А, а разность потенциала между облаком и землей – миллиарда вольт.
Дуговой разряд.
Если в качестве электродов взять два угольных стержня, и привести их в соприкосновение и приложить напряжение 30 – 50 вольт, то по получившейся замкнутой цепи пойдет сильный ток. Сила тока в небольшой дуге достигает нескольких ампер, а в больших дугах – нескольких сотен ампер. На положительном электроде дуги образуется углубление – кратер. Температура в кратере при атмосферном давлении достигает 4000 градусов Цельсия. Температура катода достигает 3000 градусов. Дуговой разряд возникает и между металлическими электродами. При увеличении мощности источника искровой разряд может превратиться в электрическую дугу. Таким образом для возникновения дугового разряда не обязательно сближение электродов.. электрическую дугу применяют для сварки металлических деталей (дуговая электросварка)
Плазма.
 2014-02-04
2014-02-04 1387
1387
