МеС, Ме2С, Ме 7С3, Ме23С6, Ме6С.
Добавленные в сталь легирующие элементы могут образовывать твердые растворы или химические соединения с железом и между собой. В большинстве случаев для сталей важную роль имеет взаимодействие ЛЭ с углеродом и азотом. Способность ЛЭ к образованию карбидов или нитридов в стали, где основу составляет железо, определяется их сродством к С и N. Если сродство ЛЭ к С и N больше, чем у железа, то будет образовываться карбид на основе ЛЭ, а не цементит.
Так как закономерности образования карбидов и нитридов в стали имеют одинаковый характер и углерод чаще применяется при легировании, чем азот, обычно рассматривают закономерности карбидообразования.
Все легирующие элементы можно разделить на две группы: карбидообразующие и не образующие карбидов в стали.
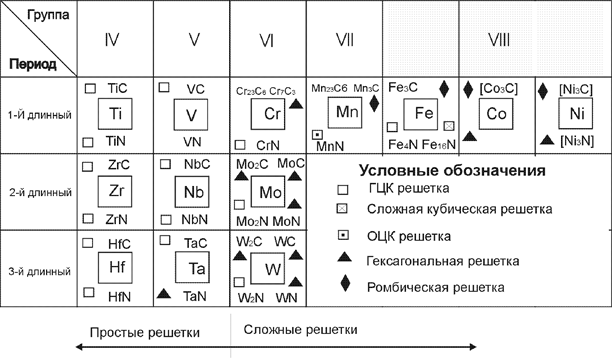
Карбиды и нитриды относятся к фазам внедрения, которые и образуются между d -переходными металлами и соответственно углеродом и азотом. Активность карбидообразующих элементов тем больше и устойчивость карбидных фаз тем выше, чем менее достроена d -электронная оболочка у данного металла. На рис. 77 приведен фрагмент таблицы Д. И. Менделеева, где расположены карбидо- и нитридообразующие элементы.
Co и Ni, представленные на рис. 77, не образуют карбиды и нитриды в стали, так как они имеют более совершенное электронное строение, чем железо.
В периодах сродство к углероду возрастает справа налево (Fe 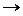 Ti), а в группах – сверху вниз (Cr
Ti), а в группах – сверху вниз (Cr 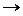 W). Таким образом, самым активным из представленных в таблице элементов будет Hf. С увеличением содержания легирующего элемента в стали образуется карбид более высокого класса (с бóльшим содержанием ЛЭ). Например, для хрома: (Cr,Fe)3C
W). Таким образом, самым активным из представленных в таблице элементов будет Hf. С увеличением содержания легирующего элемента в стали образуется карбид более высокого класса (с бóльшим содержанием ЛЭ). Например, для хрома: (Cr,Fe)3C 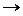 Cr7C 3
Cr7C 3 Cr23C6.
Cr23C6.
Рис. 77. Структуры d–переходных металлов, карбидов и нитридов, образуемых в стали |
В некоторых карбидах легирующих элементов может растворяться железо. Так, например, в карбидах Cr3c и Мn3С железо растворяется неограниченно. Карбиды Cr7C3 и Mn23C6 образуют ограниченные твердые растворы с железом.
Прочность связи между атомами металла и неметалла в карбидах и нитридах характеризуются теплотой образования 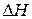 298К, кДж/(г-атом) и свободной энергией образования фаз (
298К, кДж/(г-атом) и свободной энергией образования фаз (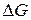 298к, кДж/(г-атом), температурой их плавления и структурно-нечувствительными упругими свойствами. Наиболее высокие значения из указанных свойств имеют карбиды и нитриды элементов IV и V групп. По мере увеличения номера группы свойства изменяются в сторону уменьшения прочности связи атомов в карбиде и нитриде или, как говорят, прочности или стойкости карбидов и нитридов.
298к, кДж/(г-атом), температурой их плавления и структурно-нечувствительными упругими свойствами. Наиболее высокие значения из указанных свойств имеют карбиды и нитриды элементов IV и V групп. По мере увеличения номера группы свойства изменяются в сторону уменьшения прочности связи атомов в карбиде и нитриде или, как говорят, прочности или стойкости карбидов и нитридов.
Следовательно, переходные металлы по их сродству к углероду и азоту, прочности и стойкости карбидов и нитридов, их устойчивости к распаду можно расположить в следующий убывающий ряд: Hf, Zr, Тi, Та, Nb, V, Мо, Сr, Мn, Fе.
Карбид Сr7С3 образуется чаще всего в конструкционных сталях с относительно невысоким содержанием хрома (до 3 – 4%). Этот карбид имеет сложную гексагональную решетку с 80 атомами на одну элементарную ячейку (56 атомов металла и 24 атома углерода).
В сталях этот карбид может содержать от 30 до 50 % Сr, т. е. его формула должна быть в пределах Fе4Сr3С3 и Fе2Сr5С3. Обычно такой карбид обозначают (Сr, Fе) 7С3 или Me7C3.
Карбид Сr23С6 образуется в высоколегированных хромистых сталях при большом содержании хрома (выше 5 – 8 %). Он имеет сложную г. ц. к. решетку, элементарная ячейка которой содержит 116 атомов, в том числе металла 92 атома и углерода – 24. В сталях карбид Сr23С6 в чистом виде не встречается, часть атомов хрома в нем замещается карбидообразующими элементами, входящими в состав стали (Fе, Мо, W).
В зависимости от характера легирования атомы металла могут содержать два или несколько элементов. Так, в высокохромистых сталях содержание железа в карбиде может повышаться до 35 %, т. е. часть атомов хрома замещается железом, при этом формула карбида имеет, например, вид Fе8Сr15С6. При меньшем содержании хрома возможно образование карбида Fе12Сr11С6. В общем виде такой карбид в сталях принято обозначать формулой (Сr, Fе) 23С6 или Me23C6. В сталях с молибденом формула карбида будет Fе20Мо2С6, а в сталях с несколькими легирующими элементами (Сr, Мо, W и др.) все они могут входить в состав карбида.
Железо широко замещает в этом карбиде хром, но так как размер атомов железа несколько меньше размера атомов хрома, то начиная с определенного момента (после замещения ~30% Сr) эти узлы становятся слишком “просторными”, и для устойчивости решетки необходимо присутствие крупных атомов W (или Мо). Атомы W (Мо) занимают также определенные позиции в решетке карбида Ме23С6, поэтому их максимальное число в элементарной ячейке составляет 8 из 92 атомов металла. Дальнейшее увеличение в стали концентрации вольфрама и молибдена в выделяющейся фазе сверх этого предела приводит к переходу Ме23С6 Þ Ме6С, как к следующему карбиду, который может вместить большее количество W и Mo.
Этот карбид образуется только при сложном легировании, поэтому он является комплексным карбидом. Его преимущество перед другими карбидами на основе Mo, W и других тугоплавких элементов заключается в том, что он имеет более низкую температуру диссоциации, что позволяет переводить Мо и W при нагреве при закалке в твердый раствор (аустенит).
Однако этот карбид метастабильный и при высокой температуре и длительных выдержках он превращается в стабильные карбиды типа МеС или Ме2С. По этой причине высоколегированные стали, содержащие в больших количествах Cr, W, Mo и V не подвергают смягчающему отжигу с нагревом и длительной выдержкой при температурах 1100...1200 о С. При закалке из этой области температур длительность выдержки строго регламентирована.
Л 5.2. Влияние легирующих элементов на С–образные кривые.
Влияние легирующих элементов на критические точки и свойства стали
Легирующие элементы значительно влияют на температурное положение критических точек в сталях. В частности, они могут интенсивно смещать точку Ас1. Подобное влияние легирующих элементов связано с двумя факторами.
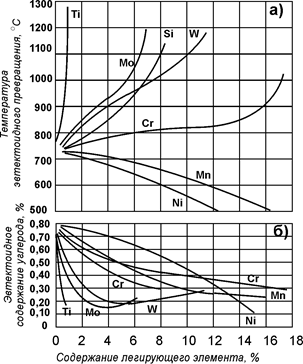 |
| Рис. 78. Влияние легирующих элементов на положение критической точки Ас1 (а) и содержание углерода в эвтектоиде (б) |
Как известно, критическая температура Ас1 в углеродистой стали отвечает превращению эвтектоидной смеси перлита 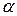 + Fе3С в аустенит путем фазового перехода a®g, диссоциации карбида и растворению углерода в g -железе. С одной стороны, легирующие элементы изменяют температуру
+ Fе3С в аустенит путем фазового перехода a®g, диссоциации карбида и растворению углерода в g -железе. С одной стороны, легирующие элементы изменяют температуру 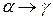 – прeвращения для феррита, входящего в состав эвтектоида (перлита), и, с другой стороны, влияют на температуру диссоциации эвтектоидных карбидов и последующее растворение углерода и легирующих элементов в g -железе. Как правило, карбидообразующие элементы повышают температуру диссоциации карбидов, и, если при этом они также повышают температуру
– прeвращения для феррита, входящего в состав эвтектоида (перлита), и, с другой стороны, влияют на температуру диссоциации эвтектоидных карбидов и последующее растворение углерода и легирующих элементов в g -железе. Как правило, карбидообразующие элементы повышают температуру диссоциации карбидов, и, если при этом они также повышают температуру 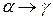 -превращения, то влияние их на точку Ас1 сказывается особенно сильно (рис. 78).
-превращения, то влияние их на точку Ас1 сказывается особенно сильно (рис. 78).
Некарбидообразующие элементы, растворяясь в цементите, несколько понижают температуру диссоциации карбида. При этом никель и марганец понижают температуру 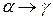 -перехода и, следовательно, снижают точку Ас1. Своеобразно влияние хрома на точку Ас1. Он до 12–13 % сравнительно слабо повышает точку Ас1, а при содержании его более 14 % наблюдается резкое повышение температуры Ас1. Подобное влияние объясняется тем, что при содержании хрома до 12 – 13 % он понижает температуру
-перехода и, следовательно, снижают точку Ас1. Своеобразно влияние хрома на точку Ас1. Он до 12–13 % сравнительно слабо повышает точку Ас1, а при содержании его более 14 % наблюдается резкое повышение температуры Ас1. Подобное влияние объясняется тем, что при содержании хрома до 12 – 13 % он понижает температуру 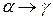 - перехода, а наблюдаемое при этих содержаниях хрома повышение точки Ас1 обусловлено более сильным влиянием диссоциации эвтектоидных карбидов при этих температурах. Закономерности влияния элементов на критические точки в основном сохраняются и в сталях, содержащих одновременно несколько легирующих элементов.
- перехода, а наблюдаемое при этих содержаниях хрома повышение точки Ас1 обусловлено более сильным влиянием диссоциации эвтектоидных карбидов при этих температурах. Закономерности влияния элементов на критические точки в основном сохраняются и в сталях, содержащих одновременно несколько легирующих элементов.
Легирующие элементы значительно влияют и на положение эвтектоидной точки S (рис. 79), и на предельную концентрацию углерода в аустените (точку Е). Некарбидообразующие элементы (никель, кобальт, кремний), растворяясь в феррите и замещая часть атомов железа в его решетке, тем самым уменьшают содержание железа в эвтектоиде и смещают точку S в сторону меньших концентраций углерода. Аналогично влияют и карбидообразующие элементы, которые в большом количестве растворяются в феррите. Их карбиды участвуют в образовании эвтектоида (например, Мп и Сr). Такие элементы, как Мо и W, сначала уменьшают, а затем увеличивают содержание углерода в эвтектоиде.
Имеются сведения, что сильные карбидообразующие элементы Тi, Nb и V, незначительно растворяющиеся в феррите и образующие стойкие карбиды, которые не участвуют в образовании эвтектоида, уменьшают количество эвтектоида в стали и увеличивают содержание углерода в эвтектоиде, т. е. смещают точку S в сторону больших концентраций углерода. В то же время, если Тi, Nb и V растворены в аустените, то они снижают содержание углерода в эвтектоиде.
Большинство легирующих элементов понижает предел растворимости углерода в  - железе и, следовательно, смещает точку Е на диаграмме Fе – Fе3С в сторону меньших концентраций углерода.
- железе и, следовательно, смещает точку Е на диаграмме Fе – Fе3С в сторону меньших концентраций углерода.
 |
| Рис. 79. Изменение содержания углерода в эвтектоиде и эвтектике при легировании |
Легирующие элементы смещают не только критические точки равновесных систем, но и изменяют кинетику распада аустенита. Кинетика распада аустенита определяет поведение стали при термической обработке. Влияние же легирующих элементов на кинетику превращения аустенита очень велико.
Элементы, которые только растворяются в феррите или цементите, не образуя специальных карбидов, оказывают лишь количественное влияние на процессы превращения (изменяют длительность инкубационного периода). Они или ускоряют превращение (к таким элементам относится только кобальт), или замедляют его (большинство элементов, в том числе марганец, никель, медь и др.).
 |
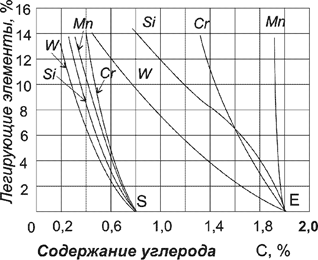
| Рис. 80. Диаграммы изотермического превращения аустенита: доэвтектоидной (а), эвтектоидной (б) и заэвтектоидной (с) углеродистой стали |
Карбидообразующие элементы вносят не только количественные, но и качественные изменения в кинетику изотермического превращения. Так, легирующие элементы, образующие растворимые в аустените карбиды, при разных температурах по-разному влияют на скорость распада аустенита: при 700 – 500 о С (образование перлита) – замедляют превращение, а при 500 – 400 о С – весьма значительно замедляют превращение; при 400 – 300 оС (образование бейнита) – ускоряет превращение при малых концентрациях и замедляют при больших.
Таким образом, в сталях, легированных карбидообразующими элементами (хром, молибден, вольфрам), наблюдаются два максимума скорости изотермического распада аустенита, разделенных областью высокой устойчивости переохлажденного аустенита. Изотермический распад аустенита имеет два явно выраженных интервала превращений – превращение в пластинчатые кристаллиты (перлитное превращение) и превращение в игольчатые кристаллиты (бейнитные превращения).
Диаграммы изотермического распада представлены на рис. 80 и 81. Видно, что увеличение содержания углерода понижает температуры начала и конца мартенситного превращения; форма кривых начала и конца перлитного превращения принципиально не изменяется.
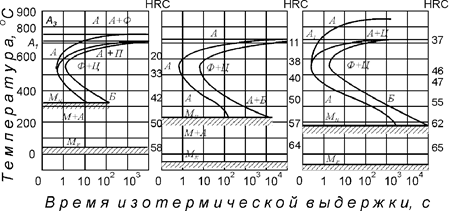
При легировании карбидообразующими элементами диаграмма приобретает другой вид (рис. 81). Причины изменения формы диаграммы подробно изучаются в дисциплине “Теория термической обработки”. Следует обратить внимание на тот факт, что положение бейнитной области зависит от содержания углерода и ЛЭ-карбидообразователя.
В легированных сталях в зависимости от положения линий начала перлитного превращения и точки Мн можно получить стали перлитного, мартенситного, бейнитного или аустенитного классов. Увеличение инкубационного периода при легировании позволяет создавать стали с высокой прокаливаемостью.
| Рис. 81. Схемы диаграмм изотермического распада аустенита, легированного карбидообразующими элементами: а – малоуглеродистая сталь; б – высокоуглеродистая сталь |
Легирующие элементы не влияют на кинетику мартенситного превращения, которая, по-видимому, похожа во всех сталях. Их влияние сказывается исключительно на положении температурного интервала мартенситного превращения, а это в свою очередь отражается и на количестве остаточного аустенита, которое фиксируется в закаленной стали.
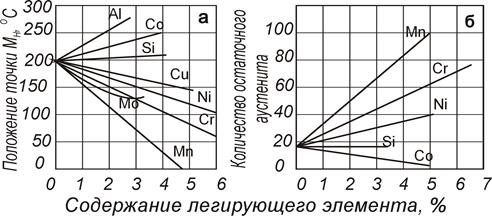 Рис. 82. Влияние ЛЭ на Мн и содержание остаточного аустенита в стали с 1 % углерода Рис. 82. Влияние ЛЭ на Мн и содержание остаточного аустенита в стали с 1 % углерода |
Некоторые элементы повышают мартенситную точку и уменьшают количество остаточного аустенита (алюминий, кобальт), другие не влияют на нее (кремний), но большинство снижает мартенситную точку и увеличивает количество остаточного аустенита (рис. 82). Из диаграммы видно, что 5% Мn снижает мартенситную точку до 0 оС, следовательно, при таком (или большем) содержании этого легирующего элемента можно зафиксировать аустенитное состояние посредством быстрого охлаждения..
Л 5.3. Влияние легирования на вязкость, прочность, Тх, размер зерна.
 2014-02-04
2014-02-04 4257
4257