Металлы во всех химических реакциях проявляют восстановительные свойства, отдают два валентных электрона, превращаясь в положительно заряженный катион:
M0 - 2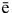
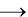 M2+
M2+
В качестве окислителей могут выступать простые вещества – неметаллы, оксиды, кислоты, соли, органические вещества.
Бериллий и магний по свойствам значительно отличаются от щелочно-земельных металлов. При комнатной температуре они устойчивы к действию кислорода и воды благодаря наличию очень тонкой оксидной пленки.
- Взаимодействие с простыми веществами
Бериллий сгорает на воздухе при температуре около 900°С, магний – при 650°С, щелочно-земельные металлы – около 500°С, в результате образуются оксиды и нитриды:
2Mg + O2 = 2MgO,
3Ca + N2 = Ca3N2.
Все металлы при нагревании реагируют с галогенами, серой и фосфором:
Be + Cl2 = BeCl2,
Mg + S = MgS,
3Ca + 2P = Ca3P2.
Бериллий с водородом не взаимодействует, магний реагирует лишь при повышенном давлении, щелочно-земельные металлы при нагревании образуют ионные гидриды:
Sr + H2 = SrH2.
При нагревании металлы реагируют с углеродом:
2Be + C = Be2C
M + 2C = MC2 (M – Mg, Ca, Sr, Ba)
- Взаимодействие с водой
Бериллий с водой не взаимодействует; магний реагирует с водой и водяным паром; кальций, стронций, барий энергично взаимодействуют с водой при комнатной температуре:
Mg + 2H2O = Mg(OH)2 + H2;
Ca + 2H2O = Ca(OH)2 + H2.
- Взаимодействие с кислотами
Все металлы реагируют с кислотами:
Mg + 2HCl = MgCl2 + H2;
4Ca + 10HNO3 (конц.)= 4Ca(NO3)2 + N2O + 5H2O.
- Взаимодействие со щелочами
Магний и щелочно-земельные металлы не реагируют со щелочами, бериллий довольно легко в них растворяется:
Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2.
- Восстановление металлов из оксидов и солей
Менее активные металлы и некоторые неметаллы могут быть получены восстановлением магнием и щелочно-земельными металлами:
2Mg + ZrO2 = Zr + 2MgO;
2Ca + SiO2 = Si + 2CaO.
 2014-02-02
2014-02-02 2316
2316








