В классической морфологии нелетальное повреждение клеток называется дистрофией (см. лекции 4—7). В большинстве случаев она относится к обратимым повреждениям.
Некроз наряду с апоптозом является одним из двух морфологических выражений смерти клетки (см. лекцию 8).
Апоптоз ответствен за многочисленные физиологические и патологические процессы, происходящие в организме.
1. В результате апоптоза происходят запрограммированное разрушение клеток в процессе эмбриогенеза (включая имплантацию, органогенез и инволюцию) и метаморфоз.
2. Посредством апоптоза развивается гормонозависимая инволюция тканей у взрослых, например атрезия фолликулов в яичниках во время менопаузы, регрессия лактирующей молочной железы после прекращения кормления ребенка.
3. Происходит уничтожение клеток в пролиферирующих клеточных популяциях, таких как эпителий крипт тонкой кишки.
4. Наступает смерть клеток в опухолях, как подвергающихся регрессии, так и с активным ростом клеток.
5. Это механизм смерти иммунных клеток — как В-, так и Т-лимфоцитов, после истощения цитокинов, а также уничтожения аутореактивных Т-клеток в развивающейся вилочковой железе.
6. Это механизм патологической атрофии гормонозависимых тканей, например атрофия предстательной железы после кастрации и исчезновение лимфоцитов в вилочковой железе после введения глюкопротеидов.
7. Это патологическая атрофия паренхиматозных органов после перекрытия протока, например, поджелудочной железы, околоушной слюнной железы, мочеточника.
8. Смерть клетки, вызванная цитотоксическими Т-клетками, например отторжение трансплантата.
9. Это гибель клеток при некоторых вирусных заболеваниях, например при вирусном гепатите (фрагменты клеток при апоптозе известны как тельца Каунсильмена).
10. Клеточная смерть, вызванная различными слабыми повреждающими воздействиями, которые в больших дозах приводят к гибели клетки (радиация, высокие или низкие температуры, цитотоксические противоопухолевые препараты и, возможно, гипоксия), также представляет собой апоптоз.
Механизмы апоптоза. Апоптоз начинается скорее всего в результате действия гормонов и других трофических факторов и является регулятором плотности клеточной популяции. Кроме того, апоптоз может быть одним из механизмов удаления аномальных клеток или клеток, поврежденных токсинами, радиацией и другими воздействиями.
Механизмы возникновения апоптоза различны и зависят от характера воздействия и типа клеток, однако последовательность событий, которые приводят к конечному результату, до конца не выяснена. Вместе с тем ряд механизмов уже установлен (схема 2).
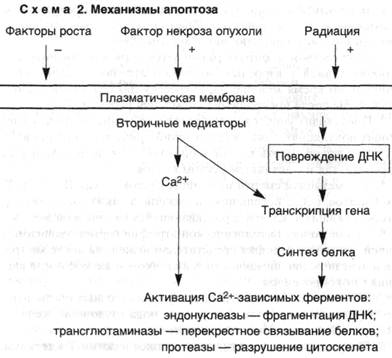
1. Конденсация хроматина. Она обусловлена расщеплением ядерной ДНК в участках связей между нуклеосомами и приводит к образованию фрагментов. Такие фрагменты создают характерную для апоптоза картину ядра, отличную от таковой при некрозе, когда ядро выглядит пятнистым. Эта интернуклеосомальная фрагментация ДНК развивается с участием кальцийчувствительной эндонуклеазы. Эндонуклеаза постоянно присутствует в клетках некоторых типов, например тимоцитах, где она активируется под влиянием цитозольного кальция, тогда как в других клетках фермент образуется перед началом апоптоза.
2. Нарушения объема и формы клеток. Эти процессы связывают с активностью трансглютаминазы, которая вызывает перекрестное связывание цитоплазматических белков, образующих оболочку под плазматической мембраной.
3. Фагоцитоз апоптозных телец макрофагами и клетками других типов. Обеспечивается рецепторами этих клеток, которые связывают и поглощают апоптозные клетки. Одним из таких рецепторов на макрофаге является витронектиновый рецептор δ3- интегрин, который обеспечивает фагоцитоз апоптозных нейтрофилов.
4. Зависимость апоптоза в большинстве случаев от активации гена и синтеза белка является одной из важных его особенностей. При этом индукция генов обеспечивается за счет "стимулов", вызывающих апоптоз, таких как стрессорные белки и протоонкоге-ны. Однако эти гены не связаны напрямую с началом апоптоза. Выявлены апоптозспецифические гены, которые стимулируют или тормозят смерть клетки.
5. Некоторые гены, участвующие в возникновении и росте злокачественной опухоли (онкогены и супрессорные гены), играют регуляторную роль в индукции апоптоза. Например, онкоген р53 в норме стимулирует апоптоз; р53 необходим для развития апоптоза после повреждения ДНК радиацией, хотя апоптоз, вызванный глюкокортикоидами или старением, не зависит от р53. ■ Таким образом, апоптоз является разновидностью смерти клетки, для которой характерна конденсация и фрагментация ДНК. Апоптоз обеспечивает уничтожение клеток при нормальном развитии, тканевом росте, органогенезе и в органах иммунной системы.
Апоптоз может быть также индуцирован под воздействием патологических стимулов. Некоторые из уже известных эффекторных механизмов включают активацию эндонуклеазы, вызванную содержащимся в цитозоле кальцием и приводящую к фрагментации ДНК. Активация трансглютаминазы частично влияет на изменение формы и размеров клеток. Апоптоз заканчивается рецепторнозависимым фагоцитозом апоптозных телец. В некоторых случаях в индукции апоптоза участвуют транскрипция генов и синтез белка, а процесс апоптоза регулируется группой генов, которые участвуют в нормальном росте и дифференцировке клеток.
 2014-02-03
2014-02-03 1123
1123
