Таблица 30
Рис. 118. Принцип определения антитромбина (AT) хромогенным методом
Обеспечение диагностики нарушений гемостаза в КДЛ
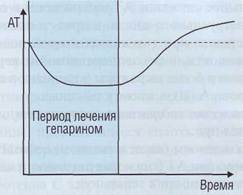
Рис. 119. Снижение уровня AT в плазме в период активного лечения нефракционированным гепарином
Лабораторная диагностика антифосфолипидного синдрома и волчаночного антикоагулянта (см. также «Тромбозы. Волчаночныи антикоагулянт»)
При антифосфолипидном синдроме в крови циркулируют антитела против фосфолипидов или фосфолипид-связанных белков. При этом синдроме возникает лабораторный феномен, при котором происходит удлинение времени свертывания крови в тестах, выполняемых на фосфолипидах (АЧТВ, ПВ). Этот феномен впервые был описан у пациентов с системной красной волчанкой и поэтому получил название волчаночного антикоагулянта. Клинически, однако, при антифосфолипидном синдроме и волчаночном антикоагулянте нет геморрагических проявлений, но есть выраженная тенденция к патологически усиленному тромбооб-разованию. Нельзя ставить знак равенства между
волчаночным антикоагулянтом и антифосфоли-пидным синдромом. В некоторых случаях при ко-агулологических признаках волчаночного антикоагулянта не находят иммунологических признаков антифосфолипидного синдрома, в свою очередь антифосфолипидный синдром не всегда сопровождается коагулологическими признаками волчаночного антикоагулянта.
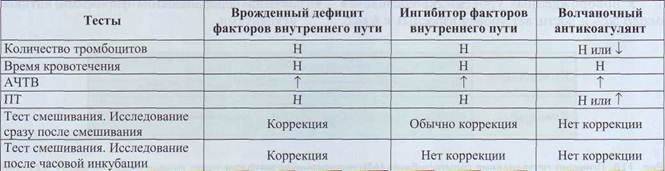
Антифосфолипидный синдром, сопровождающийся волчаночным антикоагулянтом, выявляют комбинацией фосфолипид-зависимых коагуляци-онных и иммунохимических методов, причем надежная диагностика обеспечивается только комплексным использованием группы тестов. Как правило, волчаночныи антикоагулянт распознается по удлинению фосфолипид-зависимых коагуляцион-ных тестов. Волчаночныи антикоагулянт является неспецифическим ингибитором. При подозрении на волчаночныи антикоагулянт необходимо начинать лабораторные анализы со екрининговых тестов и теста смешивания. В табл. 29 представлены данные екрининговых тестов при врожденном дефиците факторов VIII и IX, при наличии специфического ингибитора и волчаночном антикоагулянте. Важно помнить, что не все реактивы для проведения АЧТВ одинаково чувствительны к волчаночному антикоагулянту. Для анализа АЧТВ при подозрении на волчаночныи антикоагулянт необходимо применять реактивы, содержащие каолин, но не эллаговую кислоту.
Выявление волчаночных антикоагулянтов проводят последовательно: сначала в екрининговых методах, а затем в подтверждающих. На рис. 120 представлен алгоритм выявления вол-

 Таблица 29
Таблица 29
Изменения екрининговых тестов при врожденном дефиците факторов VIII и IX, наличии специфического ингибитора и волчаночном антикоагулянте
Обеспечение диагностики нарушений гемостаза в КДЛ
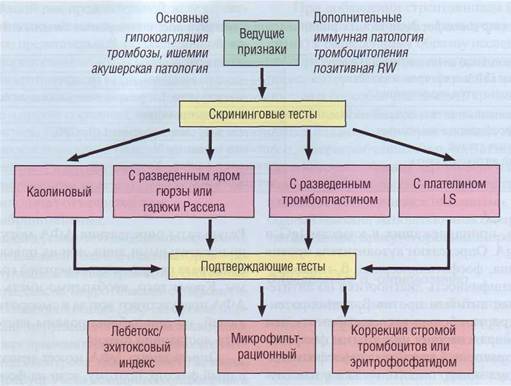 |
Рис. 120. Алгоритм выявления волчаночных антикоагулянтов
чаночного антикоагулянта (Баркаган З.С., Мо-мот А.П., 1999).
Еще одним подтверждающим тестом для определения волчаночного антикоагулянта является тест разведения. В серии последовательных разведений анализируемой плазмы буфером активность факторов свертывания крови, определяемая коагуля-ционным методом, относительно возрастает при наличии волчаночного антикоагулянта (табл. 30).
Эффект разведения на активность факторов
свертывания в присутствии волчаночного
антикоагулянта

Для подтверждения диагноза волчаночного антикоагулянта необходимо провести подтверждаю-
щие тесты, например тест нейтрализации на тромбоцитах. Проводится определение АЧТВ и активности факторов внутреннего пути плазмы больного до и после инкубации с тромбоцитами здорового донора или эритрофосфатидом. При наличии волчаночного антикоагулянта АЧТВ сокращается, а активность факторов возрастает за счет связывания части антифосфолипидных антител на тромбоцитах здорового человека. В группу подтверждающих внесены также индексы, основанные на сравнении результатов фосфолипид-зависимьгх и фосфолипид-не-зависимых тестов (лебетокс/эхитоксовый индекс).
Для уточнения диагноза антифосфолипидно-го синдрома необходимо провести определение кардиолипиновых антител с использованием метода ELISA. В табл. 31 представлен перечень антифосфолипидных антител, которые выявляются ИФА и коагуляционным методом.
Определение антифосфолипидных антител (АФА)
АФА, выявляемые твердофазным ИФА, представляют собой различные комбинации иммуно-
Обеспечение диагностики нарушений гемостаза в КДЛ
Таблица 31
Спектр антифосфолипидных антител, присутствующих в сыворотке больных А ФС
 |
глобулинов, принадлежащих к классам IgG и IgM, реже IgA. Определяют аутоантитела против кардиолипина, фосфатидилсерина, β2-гликопро-теина I. Специфичность диагностики по антителам различна: антитела против β2-гликопротеи-на I демонстрируют большую специфичность, чем антитела к кардиолипину или другим фосфоли-пидам. Лабораторный диагноз антифосфолипид-ного синдрома можно ставить только в том случае, если содержание диагностических аутоанти-тел в сыворотке крови, выявленных иммунофер-ментным методом, подтверждает патологию повторно с интервалом, по крайней мере, в 6 недель.
Результаты определения АФА могут считаться положительными лишь при их повышении в 2 и более раза по сравнению с верхней границей нормы. Кроме того, необходимо иметь в виду, что АФА присутствуют всегда в сыворотке здоровых людей, но они заблокированы гистонами и их титр достаточно низкий.
Определению АФА может мешать ревматоидный фактор, поэтому, если на фоне клинических признаков заболевания иммунохимические тесты на АФА дают отрицательный результат, то необходимо провести коагулянтные тесты на наличие волчаночного антикоагулянта.
 ■
■
.■.. ■ ■
Основным функциональным ферментом фиб-ринолиза является плазмин. При лизисе фибрино-вого сгустка плазминоген и его активаторы фиксируются на фибрине, где идет активное расщепление субстрата, тогда как в плазме фибринолиз слабо выражен, плазмин блокирован а2-антиплаз-мином.
Спонтанный эуглобулиновый лизис
Спонтанный эуглобулиновый лизис - традиционный метод оценки фибринолиза. В кислой среде при низкой температуре происходит осаждение эуглобулиновой фракции белков плазмы, содержащей фибриноген, факторы свертывания, плазминоген и его активаторы (рис. 121). Ингибиторы фибринолиза выпадают в осадок в незначительном количестве (около 2%). После растворения эуглобулиновой фракции и образования фиб-
ринового сгустка определяют время его лизиса, что отражает фибринолитическую активность плазмы. Укорочение времени лизиса эуглобулинов (активация фибринолиза) отмечается при:
• уменьшении концентрации фибриногена -
гипо- и дисфибриногенемия;
• увеличении содержания плазминогена и его ак
тиваторов - панкреатит, панкреонекроз, мета-
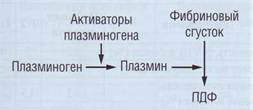
Рис. 121. Компоненты фибринолитической системы, которые определяют результаты метода «спонтанный эуглобулиновый лизис»
Обеспечение диагностики нарушений гемостаза в КДЛ
стазирующии рак предстательной железы, легкого, яичников, метастазы меланомы, операции на легких, предстательной, поджелудочной железе, гиперкатехоламинемия (стресс, тиреотоксикоз, гипертонический криз, введение адреналина), шок, патология беременности, терминальные и другие состояния, сопровождающиеся развитием ДВС-синдрома, цирроз, рак, метастатическое поражение печени (снижение ан-типлазминовой и антиактиваторной функции). Увеличение времени лизиса эуглобулинов (угнетение фибринолиза) отмечается при:
• гиперфибриногенемии;
• врожденной а-, гипо- или дисплазминогенемии;
• дефиците плазминогена и его активаторов - ре
цидивирующие венозные тромбозы, системные
васкулиты, сепсис, нефротический синдром, ги-
покоагуляционная стадия ДВС-синдрома, цир
роз печени (нарушение синтеза плазминогена).
Тест может применяться при фибринолитичес-
кой терапии для контроля эффективности лечения. Метод требует учета исходного содержания в плазме фибриногена, так как при снижении фибриногена время лизиса укорачивается, что трактуется ошибочно как гиперфибринолиз. При гиперфибриногенемии время лизиса удлиняется. Поэтому при отклонениях содержания фибриногена в плазме, а также неполноценной полимеризации фибрина и гепаринемии возможно получение ошибочных результатов. В связи с ориентировочным характером и недостаточной специфичностью в последнее время вместо теста спонтанного лизиса эуглобулинового сгустка начали использовать определение отдельных факторов фибринолиза, в первую очередь плазминогена.
Определение плазминогена
Дефицит плазминогена - один из потенциальных факторов риска тромбоза, хотя клинически это подтверждается не всегда.
При добавлении стрептокиназы (бактериальный препарат, который используется как тромбо-литик) к разведенному образцу исследуемой плазмы образуется плазминоген-стрептокиназный комплекс, который обладает ферментативной активностью и способен расщеплять хромогенный субстрат (рис. 122). Ферментативная активность комплекса плазминоген-стрептокиназа не подавляется α2-макроглобулином и α2-антиплазмином. Тесты, в которых сначала переводили плазминоген в плазмин, а затем пытались определить активность плазмина, не получились надежными, так как свободный плазмин мгновенно инактивируется α2-ан-типлазмином, присутствующим в пробе.
Определение α2 -антиплазмина
α2 -антиплазмин - самый быстрый «реактивный» ингибитор плазмина, он не позволяет присутствовать плазмину в крови в свободном виде. α2 -антиплазмин, помимо плазмина, ингибирует активаторы плазминогена - урокиназу (u-РА) и тканевой активатор (t-PA). Дефицит α2-антиплазмина встречается относительно редко, но если возникает, то это сопровождается тяжелым геморрагическим синдромом, проявляющимся диапедезными кровотечениями. Основной причиной кровотечений является присутствие свободного плазмина, который разрушает все тромбы и деградирует фибриноген.
Определение α2-антиплазмина вместе с определением ингибитора тканевого активатора плазминогена типа 1 (PAI-1), XIII фактора можно рассматривать как тесты 2-го уровня, которые необходимо выполнять, если скрининговые тесты (ПВ, АЧТВ, ТВ и определение функции тромбоцитов) нормальны, а больной страдает кровотечениями.
Уменьшение содержания (активности) α2 -ан-типлазмина наблюдается при:
• врожденном (наследственном) дефиците;
• заболеваниях печени (нарушается синтез α2-ан-
типлазмина);

 Рис. 122. Принцип определения плазминогена хромогенным методом. СК - стрептокиназа
Рис. 122. Принцип определения плазминогена хромогенным методом. СК - стрептокиназа
Обеспечение диагностики нарушений гемостаза в КДЛ
• ДВС-синдроме;
• лейкозах;
• нефротическом синдроме;
• интенсивной тромболитической терапии, ко
торая может вызвать потребление α2-анти-
плазмина.
После экстракорпорального кровообращения с использованием АИК может наблюдаться истощение α2-антиплазмина, что приводит к ги-перфибринолизу, сочетающемуся с истощением фибриногена, деградацией плазмином плазменных белков (в том числе факторов гемостаза), разрушением тромбоцитов и кровотечениями.
Принцип определения α2-антиплазмина подобен технологиям определения других ингибиторов (рис. 123). Так как происходит быстрая инактивация плазмина α2-антиплазмином, то стадия ингибирования и стадия измерения стартуют практически одновременно (что позволяет повысить специфичность метода при сниженной активности ингибитора в плазме).
Опрелеление ингибитора активатора плазминогена типа 1 (PAI-1)
PAI-1 в качестве основного ингибитора уро-киназы (u-РА) и тканевого активатора (t-PA) играет важную роль в контроле за активностью фибринолиза. Определение PAI-1 часто включа-
ется как один из тестов профиля (панели) оценки тромбофилии. У больных с кровотечениями неясного генеза с нормальными скрининговыми тестами дефицит PAI-1 может быть причиной патологии. Истинный дефицит выявляется относительно редко, но сопровождается тяжелыми кровотечениями.
Повышение PAI-1 встречается достаточно часто, так как PAI-1 - белок острой фазы. Это имеет клиническое значение, так как является причиной рецидивирующего венозного тромбоза и отмечается часто у мужчин в преклонном возрасте. PAI-1 повышается при:
инфекционных и воспалительных процессах;
послеоперационном периоде;
злокачественных опухолях;
ожирении;
гипертриглицеридемии;
лечении дексаметазоном.
У больных с инфарктом миокарда персисти-рующий подъем PAI-1 рассматривается как неблагоприятный прогностический признак.
Определение PAI-1 состоит из нескольких этапов. На первом этапе необходимо инактиви-ровать ингибиторы плазмина - α2-антиплазмин и α2-макроглобулин. Затем используется общий принцип определения остаточной активности добавленного в избытке фактора, который должен подавляться исследуемым ингибитором (рис. 124).
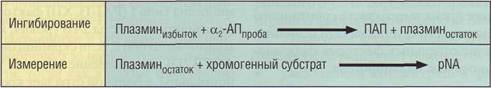 |
Рис. 123. Принцип определения α2-антиплазмина хромогенным методом. ПАП - комплекс плазмин-антиплазмин
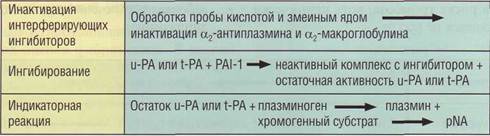
Рис. 124. Принцип определения ингибитора тканевого активатора плазминогена типа 1 (РАМ) хромогенным методом. u-PA - урокиназа, t-PA - тканевой активатор
 |
Обеспечение диагностики нарушений гемостаза в КДЛ
При использовании u-РА метод в техническом исполнении несколько проще, чем при использовании избытка t-PA, и может быть автоматизирован на современных анализаторах.
Содержание PAI-1 в системе циркуляции подвержено суточным ритмам, поэтому пробы при системном анализе необходимо брать в одно время, лучше по утрам. Кроме того, PAI-1 - один из самых неустойчивых белков плазмы, поэтому определение необходимо проводить сразу после взятия крови, транспортировка может привести к потере активности PAI-1 в пробе.
Завышенные результаты теста можно получить при увеличении активности PAI-2. Этот ингибитор повышается при беременности, поэтому в данном случае исследование PAI-1 описанным выше методом может дать ложные результаты. В последнее время активно используется определение PAI-1 методом ELISA или комбинацией им-мунохимических и функциональных методов.
Определение тканевого активатора плазминогена (t-PA)
Тканевой активатор плазминогена (t-PA) освобождается в кровоток из эндотелиальных клеток сосудистой стенки, где он синтезируется. Поэтому диагностика дефицита t-PA основывается не только на определении концентрации t-PA в крови, но и на способности освобождаться из сосудистой стенки при стрессовых воздействиях, в
частности при манжеточной пробе (дозированном пережатии вен). Сначала определяют базовый уровень t-PA, потом на 10-15 минут на предплечье накладывают жгут или раздувают манжетку, вызывающую венозный стаз, затем берут вторую порцию крови, в которой повторно определяют t-PA. Сравнивают результаты обеих проб. Из-за быстрой инактивации тканевого активатора плазминогена PAI-1 и другими ингибиторами пробы крови необходимо немедленно закислить, чтобы предупредить инактивацию t-PA in vitro. В настоящее время выпускаются специальные пробирки с кислым антикоагулянтом. t-PA имеет суточный ритм, поэтому его необходимо определять так же, как PAI-1.
t-PA обладает высокой амидазной активностью, позволяющей эффективно использовать для его определения метод хромогенных субстратов. Однако при низких концентрациях t-PA в плазме требуется проведение дополнительных процедур непрямого определения активности фермента через плазминоген и использование растворимого фибрина (рис. 125).
Определение t-PA проводится у больных с тромбофилией как часть панели тестов на выявление причины тромбофилии, особенно при нагрузочных манжеточных пробах. Повышение t-PA после инфаркта миокарда рассматривается как неблагоприятный фактор. Нарушение освобождения t-PA после венозного стаза описано у больных с тромбозами и патологией почек.
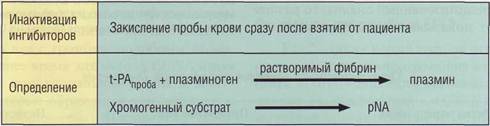 |
Рис. 125. Принцип определения тканевого активатора плазминогена (t-PA) хромогенным методом
Обеспечение диагностики нарушений гемостаза в КДЛ
Тесты активации свертывания крови
Определение D-димеров
D-димеры - это специфические продукты деградации фибрина, входившего в состав тромба. Они образуются в процессе лизиса сгустка крови под влиянием плазмина и некоторых неспецифических фибринолитиков (рис. 60). Концентрация D-димеров в сыворотке пропорциональна активности фибринолиза и количеству лизируемого фибрина. Этот тест позволяет судить об интенсивности процессов образования и разрушения фибриновых сгустков.
Определение D-димеров проводится иммуно-ферментным методом с использованием монокло-нальных антител, иммунодиффузии, методом тур-бидиметрии, латекс-агглютинации (табл. 32). Во всех методах исследования используются моно-клональные антитела к эпитопам на D-димере, которые образуются при расщеплении нерастворимого фибрина плазмином. Этих эпитопов нет на фибриногене и растворимых фибрин-мономерах, поэтому D-димеры - показатель того, что в процессе фибринолиза расщепляется именно фибрин, а не фибриноген или фибрин-мономеры. Поскольку эти антитела не взаимодействуют с фибриногеном, исследования могут проводиться как в плазме, так и в сыворотке.
Принцип теста, основанный на методе ELISA на твердой фазе (стриппированные планшеты), с нанесенными на поверхность пластика первичными антителами, показан на рис. 126. Так как D-димеры - не стандартизованный аналит, то разные методы могут показывать разные результаты,
несмотря на то, что используются специфические антитела и калибраторы.
На определение D-димеров практически не оказывает влияние техника взятия крови, примесь тромбоцитов, не требуется использования ингибиторов для подавления других факторов.
Повышение уровня D-димеров в крови определяется при возникновении венозных тромбозов, атеротромбозе, тромбоэмболии легочной артерии, ДВС-синдроме, после операций, особенно при большом операционном поле и других состояниях с повышенным образованием
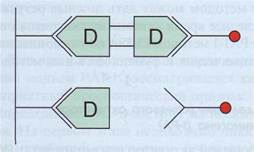
Рис. 126. Принцип метода ELISA для определения D-димеров. Специфические антитела нанесены на твердую фазу (пластик). С ними взаимодействует субъединица D из пробы и остается иммобилизованной на твердой фазе, Добавляются проявляющие антитела, конъюгированные с ферментом, которые могут взаимодействовать только с D-ди-мерами. Несвязавшиеся антитела отмываются, добавляется субстрат для фермента, по изменению окраски раствора определяется количество D-димеров, D-мономеры, формирующиеся при деградации фибриногена и входящие в состав ПДФ, не определяются тестом на D-димеры

 |
Характеристики методов определения D-димеров
Таблица 32
Обеспечение диагностики нарушений гемостаза в КДЛ
фибрина. D-димеры достаточно долго циркулируют в крови, время их полувыведения составляет более 24 ч, повышение D-димеров может персистировать в течение нескольких недель после острого тромбоза.
Уровень D-димеров повышен у больных с тромбозом глубоких вен бедра, с тромбоэмболией легочной артерии, он может повышаться после обширных хирургических вмешательств, травм, при онкологических заболеваниях. На значение D-димеров влияют такие факторы, как величина тромба, время от начала клинических проявлений до назначения антикоагулянтной терапии, прием антикоагулянтов, на фоне которых уровень D-димеров постоянно снижается. Поэтому более важной для исключения диагноза тромбоза является отрицательная диагностическая значимость теста. Причем для разных тестов отрицательная диагностическая значимость колеблется от 78 до 100%, она выше у более чувствительных методов, что характерно для ИФА-ди-агностики. D-димеры определяются в моче, но их появление интерпретируется как маркер почечной дисфункции.
Продукты деградации фибрина/фибриногена (ПДФ)
Продукты деградации фибрина/фибриногена определяются традиционно в общей группе с использованием поликлональных антител. При этом антитела могут взаимодействовать с эпито-пами фибриногена, поэтому требуется не только использование сыворотки, но и полное удаление фибриногена с добавлением к крови тромбина или змеиного яда с тромбиноподобным эффектом. В последнее время для метода ELISA стали использовать моноклональные антитела к нео-эпитопам, которые образуются при деградации фибрина или фибриногена под влиянием плазми-на. Тем не менее трудно отдифференцировать ПДФ, образующиеся при деградации фибрина из тромба, от ПДФ, сформировавшихся при деградации фибриногена, особенно при использовании активаторов фибринолиза. Для определения ПДФ широко распространен метод латекс-агглютинации. Этот метод легко автоматизируется на турбидиметрах, но характеризуется относительно низкой специфичностью.
Положительная проба - содержание ПДФ в плазме/сыворотке свыше 0,5 мкг/мл - указывает на:
• ДВС-синдром;
• тромбоз глубоких вен;
• тромбоэмболию легочной артерии;
• метастазы в легкие, рак яичников;
• фибринолитическую терапию.
Тромбин-антитромбиновый комплекс (ТАТ)
Определение ТАТ - новый тест в диагностике ДВС-синдрома, он активно внедряется в практику клинико-диагностических лабораторий. Клиренс ТАТ из системы циркуляции достаточно быстрый, он удаляется в течение нескольких минут. Поэтому присутствие ТАТ в плазме свидетельствует об образовании тромбина in vivo непосредственно в момент взятия крови на исследование и о возможности истощения антикоагулянтов.
В методе ELISA на твердую фазу нанесены антитела к тромбину. После отмывки проявляющие антитела связываются с антитромбином, присутствующем в ТАТ, оценка количества ТАТ проводится цветной реакцией. Определение ТАТ очень информативно в острой ситуации, непосредственно при тромбообразовании. В этом плане определение ТАТ по диагностическому значению схоже с определением фибринопептида А (ФПА), однако для ТАТ менее критичными являются требования к процедуре взятия крови. Иногда тест с некоторыми модификациями используется для определения антитромбина (AT).
Фрагменты протромбина F1 +2
F1+2 - также новый тест, он отражает активность превращения протромбина в тромбин с участием протромбиназного комплекса (фактор Ха, фактор Va, фосфолипиды и Са2+), который формируется при активации системы плазменного гемостаза (рис. 127).
Определение F1+2, так же как ТАТ, проводится с целью диагностики состояния гиперкоагуляции, которое может быть значимым при остром и хроническом ДВС, тромбозе глубоких вен бедра, эмболии легочной артерии, злокачественных опухолях и острых миелоидных лейкозах (протекающих с активацией системы свертывания), наличии факторов риска тромбоэмболии, остром инфаркте миокарда и
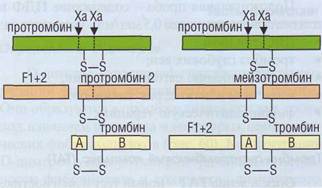 |
| Рис. 127. Образование фрагмента протромбина F1+2. Протромбин расщепляется протромбиназным комплексом в 2 участках в 2 этапа с образованием разных промежуточных продуктов, но обязательным формированием тромбина и фрагмента F1 + 2. Между количеством фрагментов F1 + 2 и количеством образующегося тромбина существует стехиометрическое соотношение |
| последующей тромболитической терапии. Исследование F1+2 полезно использовать при мониторинге лекарственной коррекции состояния гиперкоагуляции, в частности при лечении гепарином и концентратами антитромбина. Определение ТАТ и F1+2 характеризуется высокой аналитической чувствительностью, поэтому их увеличение можно зарегистрировать до появления клинических признаков ДВС- |
Обеспечение диагностики нарушений гемостаза в КДЛ
синдрома. F1+2, в отличие от ТАТ, имеют относительно продолжительный период циркуляции в системе кровотока. Состояние гиперкоагуляции можно зарегистрировать с помощью как ТАТ, так и F1+2, тогда как состояние гипокоагуляции можно выявить только по уменьшению F1+2. Поэтому определение F1+2 проводится иногда с целью мониторинга антикоагулянтов непрямого действия, эффективности профилактического подкожного или внутривенного введения гепарина.
Определение F1+2 можно использовать для решения вопроса о назначении/неназначении терапевтических вмешательств у пациентов с дефицитом антикоагулянтов и при беременности в случае риска возникновения тромбозов (табл. 33).
Фибринопептид А (ФПА, FPA)
ФПА отщепляется от молекулы фибриногена тромбином (рис. 44), поэтому при тромбинемии количество ФПА в плазме увеличивается. Определение ФПА достаточно давно используется как маркер активации гемостаза. В современных наборах используется метод ELISA с моноклональны-ми антителами. ФПА - очень чувствительный тест на потребление фибриногена, его концентрация повышается при различных заболеваниях с тром-
 2014-02-17
2014-02-17 1579
1579
