Оксидазный путь использования кислорода в клетке
Причины и последствия повреждений митохондрий
Метаболические и гомеостатические функции митохондрий
В митохондриях происходит: синтез АТФ и теплопродукция в реакция окислительного фосфорилирования; β-окисления жирных кислот; реакции ЦТК, через ЦТК протекают некоторые реакции глюконеогенеза, переаминирования, дезаминирования, липогенеза и синтеза гема, осуществляется интеграция белкового, липидного и углеводного обмена.
Повреждение внутренней мембраны митохондрий химическими и физическими факторами приводит разобщению окислительного фосфорилирования, нарушению синтеза АТФ, торможению анаболических реакций, межмембранного транспорта и всех видов обмена веществ.
Оксидазный путь потребления кислорода протекает в митохондриях, потребляет 90% О2 и обеспечивает процесс окислительного фосфорилирования.
Окислительным фосфорилированием называют синтез АТФ из АДФ и Н3РО4 за счет энергии движении электронов по дыхательной цепи. Окислительное фосфорилирование является основным источником АТФ в аэробных клетках. Хемиосмотическая теория Митчелла Для объяснения механизма окислительного фосфорилирования в 1961 году Митчеллом была предложена хемиосмотическая теория, которая включала четыре независимых постулата, касавшиеся функции митохондрий:1. Внутренняя мембрана митохондрий непроницаема для всех ионов.
2. Она содержит ряд белков-переносчиков, осуществляющих транспорт необходимых метаболитов и неорганических ионов.
3. При прохождении электронов по дыхательной цепи внутренней мембраны происходит перемещение Н+ из матрикса в межмембранное пространство.
4. При достаточно большом протонном градиенте протоны начинают «течь» через АТФ-синтетазу, что сопровождается синтезом АТФ.
Современные представления о механизме окислительного фосфорилирования В настоящее время открыты все основные компоненты окислительного фосфорилирования, изучено их строение и свойства. Открыты основные принципы окислительного фосфорилирования, регуляция и механизмы некоторых стадий. МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯОкислительное фосфорилирование состоит из процессов окисления и фосфорилирования, которые между собой сопряжены.
Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами.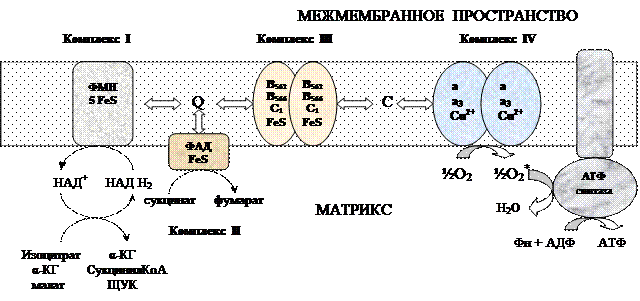 Комплекс I – НАДН2 дегидрогеназный комплекс – самый большой из дыхательных ферментных комплексов – имеет молекулярную массу свыше 800КДа, состоит из более 22 полипептидных цепей, в качестве коферментов содержит ФМН и 5 железо-серных (Fe2S2 и Fe4S4) белков. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железо-серный белок. Комплекс III – Комплекс b-c1 (фермент QH2 ДГ), имеет молекулярную массу 500КДа, состоит из 8 полипептидных цепей, и вероятно существует в виде димера. Каждый мономер содержит 3 гема, связанных с цитохромами b562, b566, с1, и железо-серный белок. Комплекс IV – Цитохромоксидазный комплекс имеет молекулярную массу 300КДа, состоит из 8 полипептидных цепей, существует в виде димера. Каждый мономер содержит 2 цитохрома (а и а3) и 2 атома меди. Коэнзим Q (убихинон). Липид, радикал которого у млекопитающих образован 10 изопреноидными единицами (Q10). Убихинон переносит по 2Н+ и 2е-.
Комплекс I – НАДН2 дегидрогеназный комплекс – самый большой из дыхательных ферментных комплексов – имеет молекулярную массу свыше 800КДа, состоит из более 22 полипептидных цепей, в качестве коферментов содержит ФМН и 5 железо-серных (Fe2S2 и Fe4S4) белков. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железо-серный белок. Комплекс III – Комплекс b-c1 (фермент QH2 ДГ), имеет молекулярную массу 500КДа, состоит из 8 полипептидных цепей, и вероятно существует в виде димера. Каждый мономер содержит 3 гема, связанных с цитохромами b562, b566, с1, и железо-серный белок. Комплекс IV – Цитохромоксидазный комплекс имеет молекулярную массу 300КДа, состоит из 8 полипептидных цепей, существует в виде димера. Каждый мономер содержит 2 цитохрома (а и а3) и 2 атома меди. Коэнзим Q (убихинон). Липид, радикал которого у млекопитающих образован 10 изопреноидными единицами (Q10). Убихинон переносит по 2Н+ и 2е-. 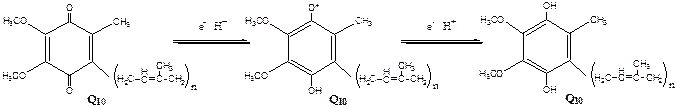 убихинон ↔ семихинон ↔ гидрохинон Цитохром с. Периферический водорастворимый мембранный белок с массой 12,5КДа, содержит 1 полипептидную цепь из 100 АК, и молекулу гема.Молекулярные соотношения между компонентами дыхательной цепи отличаются в разных тканях. Например, в миокарде, на 1 молекулу НАДН2 дегидрогеназного комплекса приходиться 3 молекулы комплекса b-c1, 7 молекул цитохромоксидазного комплекса, 9 молекул цитохрома С и 50 молекул убихинона. Электрохимический потенциал. Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии.I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла.
убихинон ↔ семихинон ↔ гидрохинон Цитохром с. Периферический водорастворимый мембранный белок с массой 12,5КДа, содержит 1 полипептидную цепь из 100 АК, и молекулу гема.Молекулярные соотношения между компонентами дыхательной цепи отличаются в разных тканях. Например, в миокарде, на 1 молекулу НАДН2 дегидрогеназного комплекса приходиться 3 молекулы комплекса b-c1, 7 молекул цитохромоксидазного комплекса, 9 молекул цитохрома С и 50 молекул убихинона. Электрохимический потенциал. Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии.I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла. 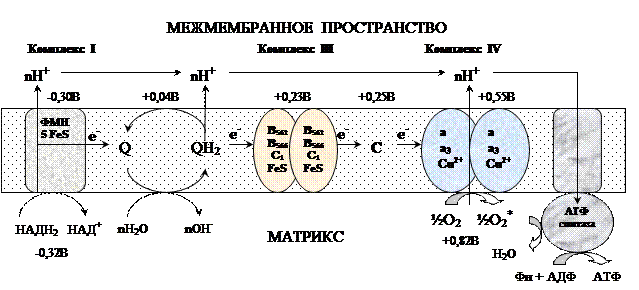 Этапы движения е- по дыхательной цепи 1. 2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).2. КоQ с 2е- забирает у воды 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II).3. КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство.4. Цитохром С переносит е- c III комплекса на IV комплекс.5. IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов ∆рН = 60 мВ (при ∆рН=1) (в матриксе рН выше, чем в цитозоле). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность потенциалов ∆V=160мВ, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который в типичной клетке составляет около 60+160=220 мВ. Механизм переноса Н+ через мембрану до конца не изучен. Вероятно, у разных компонентов дыхательной цепи существуют разные механизмы сопряжения транспорта е- с перемещением Н+. Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для:1) фосфорилирования АДФ в АТФ; 2) транспорта веществ через мембрану митохондрий; 3) теплопродукцию. Процесс фосфорилирования Процесс фосфорилирования осуществляется АТФ-синтетазой (Н+-АТФ-аза), которая потребляет 40-45% свободной энергии, выделившейся при окислении. Н+-АТФ-аза интегральный белок внутренней мембраны митохондрий, она состоит из 2 белковых комплексов F0 и F1.
Этапы движения е- по дыхательной цепи 1. 2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).2. КоQ с 2е- забирает у воды 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II).3. КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство.4. Цитохром С переносит е- c III комплекса на IV комплекс.5. IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов ∆рН = 60 мВ (при ∆рН=1) (в матриксе рН выше, чем в цитозоле). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность потенциалов ∆V=160мВ, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который в типичной клетке составляет около 60+160=220 мВ. Механизм переноса Н+ через мембрану до конца не изучен. Вероятно, у разных компонентов дыхательной цепи существуют разные механизмы сопряжения транспорта е- с перемещением Н+. Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для:1) фосфорилирования АДФ в АТФ; 2) транспорта веществ через мембрану митохондрий; 3) теплопродукцию. Процесс фосфорилирования Процесс фосфорилирования осуществляется АТФ-синтетазой (Н+-АТФ-аза), которая потребляет 40-45% свободной энергии, выделившейся при окислении. Н+-АТФ-аза интегральный белок внутренней мембраны митохондрий, она состоит из 2 белковых комплексов F0 и F1. 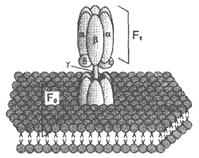 | Гидрофобный комплекс F0 погружён в мембрану и служит основанием, которое фиксирует АТФ-синтазу в мембране. Он состоит из нескольких субъединиц, образующих канал, по которому протоны переносятся в матрикс. Комплекс F1 выступает в митохондриальный матрикс. Он состоит из 9 субъединиц (3α, 3β, γ, δ, ε). Субъединицы α и β уложены попарно, образуя «головку»; между а- и β-субъединицами располагаются 3 активных центра, в которых происходит синтез АТФ; γ, δ, ε – субъединицы связывают комплекс F1, с F0. |
 2014-02-17
2014-02-17 2000
2000
