Взаимодействие химической промышленности с окружающей средой
Наиболее существенным фактором взаимодействия химической промышленности с окружающей средой являетсярост производства большого количества новых веществ, которые не синтезируются и не усваиваются в природном круговороте, в процессах саморегулирования окружающей среды.
Химические производства потребляют из окружающей среды воздух и воду, а выбрасывают различные твердые, жидкие и газообразные отходы производств.
В химической промышленности изначально применяются очень токсичные вещества. Например, в производстве аммиакаприменяются смеси сероводорода, серосодержащих кислот,оксид углерода, очень большие остатки сероводорода.В производстве перекиси водородаприменяетсянадсерная кислота (H2S2O8) и большиеостатки серной кислоты (H2SO4). В производстве мыла используются нефтепродукты, остатки кислого мыла – нерастворимогов воде (в определенной степени оно также токсично).
Потребителями химической продукции являются практически все отрасли промышленности, строительство, сельское и коммунально-бытовое хозяйства, поэтому загрязнение окружающей среды продукцией химических производств не ограничивается местом их расположения.
В основной химической промышленности - промышленности тяжелого неорганического синтеза - наибольшее влияние на окружающую среду осуществляют производства основных продуктов, которые являются исходными во многих других отраслях промышленности: производство серной кислоты, минеральных удобрений, кальцинированной соды.
Серная кислота используется для производства удобрений, очистки нефтепродуктов, в цветной металлургии, при пищеварении металлов. Особенно чистая кислота используется в производстве красителей, лаков, красок, лекарственных веществ, пластмасс, химических волокон, многих ядохимикатов, взрывчатых веществ, эфиров, спиртов и т.д.
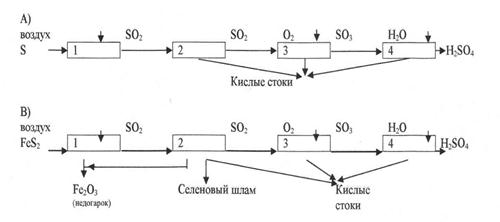
Функциональные схемы производства серной кислоты из серы (А)
и серного колчедана (В):1-обжиг серосодержащего сырья,2-очистка и промывка обжиговых газов,3-окисление SО2,4-абсорбция SО3.
Сырьевая база производства серной кислоты - серосодержащие соединения, из которых можно получить диоксид серы. В промышленности около 80% серной кислоты получают из природной серы и железного (серного) колчедана. Значительное место занимают отходящие газы цветной металлургии, получаемые при обжиге сульфидов цветных металлов, содержащих диоксид серы.
Чистый серный колчедан содержит 53,5% серы и 46,5% железа. Примеси (песок, глина, карбонаты, соединения As, Se, Ag, Au и др.) уменьшают содержание серы до 32-40%.
Выходной SО2 с обжигательной печи загрязнен огарковой пылью и другими примесями. Содержание в нем пыли зависит от качества и степени помола сырья, конструкции печей и других факторов и составляет 1-300г/м3. Химический состав пыли практически не отличается от состава огарка. Объемы обжиговых газов равны сотням тысяч кубометров в сутки, они несут с собой десятки тонн огарковой пыли. Перед переработкой на H2SO4 газы очищают в циклонах и сухих электрофильтрах до содержания пыли около 0,1 г/м3. Дополнительную очистку проводят последовательно промывкой охлажденной 60-75% (в пустых башнях) и 25-40% (в насадочных башнях) серной кислотой и улавливанием тумана, образующегося в мокрых электрофильтрах.
При обжиге серного колчедана отходы пиритных огарков составляют до 70% от массы колчедана. На 1т произведенной кислоты выход огарка составляет до 0,55 т.
Таким образом, отходами производства H2SO4 из серного колчедана являются пиритные огарки, пыль циклонов и сухих электрофильтров, шламы промывочных башен и шламы мокрых электрофильтров, а также отходящие газы, содержащие 0,02-0,03% SO3.
Для производства 1т H2SO4 необходимы:
Серы – 0,34 т (FeS2 - 0,82 т),
Электроэнергия – 85кВт * ч,
Вода – 70 м3,
Катализатор – 0,1 кг.
Лекция № 7
 2014-02-24
2014-02-24 3812
3812
