Все вещества могут существовать в различных агрегатных состояниях или в различных модификациях одного агрегатного состояния в зависимости от условий (Т, р и т.д.). Переход вещества из одного агрегатного состояния в другое, или изменение модификации агрегатного состояния вещества называется фазовым переходом первого рода. Фазовые переходы 1-го рода сопровождаются выделением или поглощением теплоты.
|
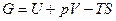 . (25)
. (25)
При динамическом равновесии выполняется уравнение:
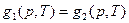 , (26)
, (26)
где g1 и g2 – удельные (относящиеся к единице массы вещества) термодинамические потенциалы 1-й и 2-й фаз.
Уравнение, связывающее между собой давление и температуру, при которых осуществляется фазовый переход первого рода, имеет вид

где 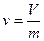 - удельный объем. Две любые фазы вещества могут находиться в равновесии лишь при определенном давлении, зависящем от температуры.
- удельный объем. Две любые фазы вещества могут находиться в равновесии лишь при определенном давлении, зависящем от температуры.
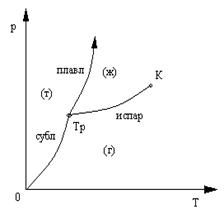
Максимально возможное число фаз вещества, находящихся в равновесии друг с другом равно трем, если это изобразить на плоскости p, T, то она получится разделена на три области: твердую фазу (т), жидкую (ж) и газообразную (г), рис.20
Границами соприкасающихся фаз являются кривые сублимации (испарение твердого тела), испарения и плавления, характеризующие двухфазные равновесные состояния.
|

|

Подобные диаграммы строят экспериментально для разных веществ, они позволяют предсказывать в каких равновесных состояниях может находиться вещество при тех или иных значениях давления и температуры, а также когда и какие оно будет испытывать фазовые превращения при том или ином процессе. Например, кривая испарения заканчивается в критической точке К, поэтому возможен непрерывный переход вещества из жидкого состояния в газообразное и обратно путем обхода точки К «сверху», в этом случае такой переход не сопровождается двухфазным состоянием.
 2014-02-24
2014-02-24 386
386








