С помощью хлоридов фосфора (III и V) или хлорокиси фосфора
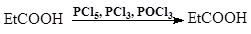
Метод применяется только тогда, когда продукт можно экстрагировать органическим растворителем или отогнать из реакционной массы.
5.Фторирование кислот четырехфтористой серой:
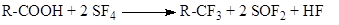
1. Галогеноводороды превращают спирты в хлор-, бром- и иодалканы и чаще всего по SN1-механизму. При этом активность галогенводородов возрастает в ряду HCl < HBr < HI, а спиртов – в ряду первичный < вторичный < третичный. Например, изоамилбромид в производстве барбамила получают исходя из бромида натрия в серной кислоты:
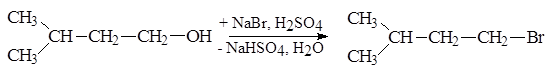
Недостатком такого способа является большой расход серной кислоты.
- Хлористый водород с вторичными и особенно первичными спиртами реагируют очень медленно. Для ускорения процесса повышают концентрацию хлористого водорода, проводят реакцию под давлением при повышенной температуре или используют катализаторы (серная кислота и хлорид цинка). Недостаток метода – процесс сопровождается перегруппировкой углеродного скелета.
2. Реакции спиртов и фенолов с галогенидами фосфора (PCl5, PHlg3, POCl3).
- В реакциях со спиртами трибромид и трииодид фосфораможно получить непосредственно в реакционной массе:
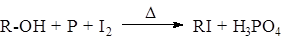
- Хлорокись фосфора обычно применяют для замены активированной –ОН группы в ароматических и гетероароматических соединениях. В качестве катализаторов можно использовать основания или кислоты.
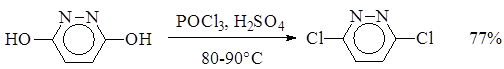
3. Реакции гидроксилсодержащих соединений с тионилхлоридом является самым распространенным методом синтеза хлоридов:
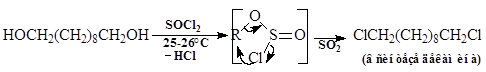
 2014-02-09
2014-02-09 1588
1588







