РАЗДЕЛ 6. КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ (лекции 11-12) 4 часа
Контрольные вопросы
1. Что такое закон? Каковы различия между законами природы и законами общества и есть ли сходство?
2. В чем проявляется единство природы и общества?
3. Как влияет природа на развитие общества и общество на природу?
4. В чем актуальность проблемы природы и общества?
5. Что Вы можете сказать о влиянии техногенной цивилизаций на жизнь людей? Позитивные и негативные моменты.
6. Что Вы можете сказать о «русском космизме»?
7. Каковы перспективы дальнейшего цивилизованного развития?
Что Вы можете сказать о многообразии культур и нужно ли использовать ценность диалога?
8. Какие новые стратегии Вы можете предложить для решения экологической проблемы.
9. Что такое коэволюция?
10. Что такое ноосфера?
11. Как связан экологический императив с нравственным?
Вопросы для самостоятельного изучения (СРС)
1. Отличие истории общества от истории природы.
2. Объективное и субъективное в истории общества.
3. Существуют ли универсальные законы истории?
4. Карл Маркс и Карл Поппер о законах истории
5. Существуют ли универсальные законы истории?
6. Человечество: для чего оно?
7. Мальтус воскреснет из мертвых?
8. Поиски стратегии экологического развития мировой цивилизации
9. Проблемы и перспективы Римского клуба.
10. Взаимодействие общества и природы в условиях глобальных проблем.
11. Способ производства как одна из социальнофилософских характеристик взаимодействия общества и природы
12. Проблемы коэволюции экологического и политического сознания в современной России.
13. Разоружение как глобальная проблема современности - рудимент прошлого или забота о будущем?
14. Можно ли помирить современную экономику с заботой об экологии?
15. Идеи В.И. Вернадского и цивилизационный выбор России.
16. Философские идеи В.И. Вернадского.
17. Глобальные проблемы современности.
Учебная, учебно-методическая и дополнительная литература
- Биоэтика: проблемы, трудности, перспективы: Материалы «круглого стола»// Вопросы философии.1992.№10.
- Вернадский В.И. Философские мысли натуралиста. – М., 1988.
- Ганди М.К. Моя вера в ненасилие//Вопросы философии.1992.№3.
- Замятин Е., Хаксли О., Оруэлл Дж. Антиутопии XX века. – М., 1989.
- Лоренц К. Восемь смертных грехов цивилизации// Вопросы философии.1992.№3.
- Моисеев Н.Н. Человек и ноосфера. – М.., 1990.
- Моисеев Н.Н. Грядущие десятилетия: трудности и перспективы//Социально-политический журнал.1994.№1-2.
- Печчен А. Человеческие качества. – М., 1985.
- Предупреждение человечеству. Декларация ученых по глобальным проблемам //Человек. 1993.№5.
- Сахаров А.Д. Мир через полвека//Вопросы философии.1989.№11.
- Фромм Э. Иметь или быть? – М., 1996.
- Швейцер А. Благоговение перед жизнью. – М., 1992.
6.1 Основы металловедения. Классификация металлов. Строение и свойства металлов. Кристаллизация металлов
Металлы – класс конструкционных материалов, характеризующийся следующим набором свойств:
ü «металлический блеск» (хорошая отражательная способность);
ü пластичность;
ü высокая теплопроводность;
ü высокая электропроводность.
Свойствами металлов обладают около 80 элементов периодической системы Д.И. Менделеева.
По объему и частоте использования:
ü технические (железо Fe, медь Си, алюминий Аl, магний Mg, никель Ni, титан Ti, свинец РЬ, цинк Zn, олово Sn) и редкие (ртуть Hg, натрий Na, серебро Ag, золото Аи, платина Pt, кобальт Со, хром Сг, молибден Мо, тантал Та, вольфрам W).
ü железоуглеродистые (Fe-C) сплавы — стали и чугуны, которые образуют группу черных металлов. Все остальные представляют группу цветных металлов. На долю черных металлов приходится - 85 % всех производимых металлов, а на долю цветных -15 %.
По физико-химическим свойствам металлы можно разделить на шесть основных групп.
Магнитные — Fe, Co, Ni обладают ферромагнитными свойствами. Сплавы на основе Fe (стали и чугуны) являются главными конструкционными материалами; сплавы на основе Fe, Co и Ni являются основными магнитными материалами (ферромагнетиками).
Тугоплавкие — металлы, у которых температура плавления выше, чем у Fe (1539 °С); это W (3380 °С), Та (2970 °С), Мо (2620 °С), Сг (1900 °С), Pt (1770 °С), Ti (1670 °С) и др. Применяют их как самостоятельно, так и в виде добавок в стали, работающие, в частности, при высокой температуре.
Легкоплавкие — имеют Тпл ниже 500 °С; к ним относятся: Zn (419 °С), РЬ (327 °С), кадмий Cd (321 °С), таллий Т1 (303 °С), висмут Bi (271 °С), олово Sn (232 °С), индий In (156 °С), Na (98 °С) и др. Назначение их самое различное: антикоррозионные покрытия, антифрикционные сплавы, проводниковые материалы.
Легкие металлы имеют плотность не более 2,75 Мг/м3; к ним относится Аl, плотность — 2,7, бериллий Be — 1,84, Mg —1,74, Na — 0,97, Li — 0,53 Мг/м3 и др. Эти металлы применяют для производства сплавов, используемых в конструкциях с ограничениями в массе.
Благородные — в электротехнике применяют Аи, Ag, Pt, палладий Pd, а также металлы платиновой группы: иридий Ir, родий Rh, осмий Os, рутений Ru. Эти металлы и сплавы на их основе обладают высокой химической стойкостью, в том числе и при повышенных температурах. их используют в производстве ответственных контактов, выводов интегральных микросхем и других полупроводниковых приборов, термометров сопротивления и термопар, нагревательных элементов, работающих в особых условиях.
Редкоземельные — лантаноиды; их применяют как присадки в различных сплавах. Сплавы (RM) металлов группы железа (М) с редкоземельными элементами (R) являются весьма перспективными магнитотвердыми материалами.
6.2 Основы теории сплавов. Особенности строения, кристаллизации и свойств сплавов. Фазовые превращения в сплавах. Основные типы диаграмм состояния
Основы теории сплавов
Сплавом называется вещество, получаемое путем сплавления нескольких простых веществ, называемых компонентами сплава.
Возможны другие способы приготовления сплавов: спекания, электролиз, возгонка. В этом случае вещества называются псевдосплавами.
Псевдосплав – спеченная смесь двух порошков, один из которых является более тугоплавким. При этом более легкоплавкая компонента может расплавиться в процессе работы, но наличие каркаса из тугоплавкой компоненты удерживает жидкость за счет капиллярных сил. Легкоплавкая компонента обычно является более тепло- и электропроводной. Используют следующие псевдосплавы: серебро-окись кадмия, серебро-графит, серебро-никель, серебро-вольфрам, медь-графит, медь-вольфрам.
Сплав, приготовленный преимущественно из металлических элементов (более 50%) и обладающий металлическими свойствами, называется металлическим сплавом.
В металлическом сплаве основным компонентом (более 50%) должен быть металл. У сплавов можно получить более высокие механические, физические и химические свойства, чем у чистых металлов, поэтому их так широко применяют в технике.
Сплавы обладают более разнообразным комплексом свойств, которые изменяются в зависимости от состава и метода обработки.
Сплавы на основе железа и особенно железоуглеродистые сплавы – стали и чугуна – являются важнейшими конструкционными материалами.
Все сплавы железа с углеродом принято делить на стали и чугуны.
К сталям формально относятся сплавы, содержащие менее 2,14% углерода, остальные сплавы причисляются к чугунам.
Для правильного понимания природы свойств разнообразных марок современных сталей и чугунов, включая и специальные, так называемые легированные стали необходимо изучить диаграмму состояний железо-углерод.
Основные понятия в теории сплавов
Система – группа тел выделяемых для наблюдения и изучения. В металловедении системами являются металлы и металлические сплавы. Чистый металл является простой однокомпонентной системой, сплав – сложной системой, состоящей из двух и более компонентов.
Компоненты – вещества, образующие систему. В качестве компонентов выступают чистые вещества и химические соединения, если они не диссоциируют на составные части в исследуемом интервале температур.
Фаза – однородная часть системы, отделенная от других частей системы поверхностью раздела, при переходе через которую структура и свойства резко меняются.
Вариантность (C) (число степеней свободы) – это число внутренних и внешних факторов (температура, давление, концентрация), которые можно изменять без изменения количества фаз в системе.
Если вариантность C = 1 (моновариантная система), то возможно изменение одного из факторов в некоторых пределах, без изменения числа фаз.
Если вариантность C = 0 (нонвариантная cистема), то внешние факторы изменять нельзя без изменения числа фаз в системе.
Существует математическая связь между числом компонентов (К), числом фаз (Ф) и вариантностью системы (С). Это правило фаз или закон Гиббса
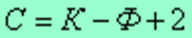
Если принять, что все превращения происходят при постоянном давлении, то число переменных уменьшится
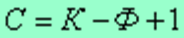
где: С – число степеней свободы, К – число компонентов, Ф – число фаз, 1 – учитывает возможность изменения температуры.
Особенности строения, кристаллизации и свойств сплавов
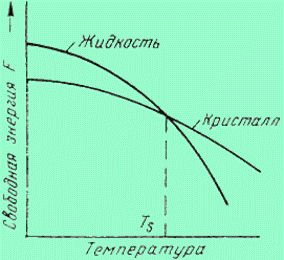
Кристаллизация – это процесс образования участков кристаллической решетки в жидкой фазе и рост кристаллов из образовавшихся центров.
При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго. Температура ТS – равновесная или теоретическая температура кристаллизации.
В зависимости от характера взаимодействия компонентов различают сплавы:
ü механические смеси;
ü твердые растворы.
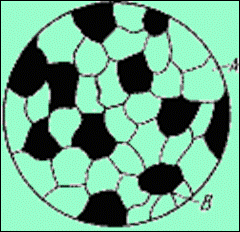
Сплавы механические смеси образуются, когда компоненты не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения.
Образуются между элементами значительно различающимися по строению и свойствам, когда сила взаимодействия между однородными атомами больше чем между разнородными. Сплав состоит из кристаллов входящих в него компонентов. В сплавах сохраняются кристаллические решетки компонентов.
Сплавы химические соединения образуются между элементами, значительно различающимися по строению и свойствам, если сила взаимодействия между разнородными атомами больше, чем между однородными.
Особенности этих сплавов:
1. Постоянство состава, то есть сплав образуется при определенном соотношении компонентов, химическое соединение обозначается Аn Вm.
2. Образуется специфическая, отличающаяся от решеток элементов, составляющих химическое соединение, кристаллическая решетка с правильным упорядоченным расположением атомов
3. Ярко выраженные индивидуальные свойства
4. Постоянство температуры кристаллизации, как у чистых компонентов
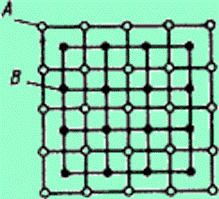
Сплавы твердые растворы – это твердые фазы, в которых соотношения между компонентами могут изменяться. Являются кристаллическими веществами.
Характерной особенностью твердых растворов является наличие в их кристаллической решетке разнородных атомов, при сохранении типа решетки растворителя.
Твердый раствор состоит из однородных зерен.
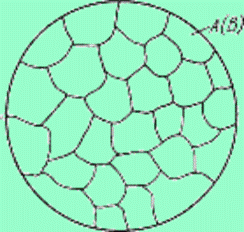
По степеням растворимости компонентов различают твердые растворы:
• с неограниченной растворимостью компонентов;
• с ограниченной растворимостью компонентов.
Фазовые превращения в сплавах
Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа. В результате получают серию кривых охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба и температурные остановки.
Температуры, соответствующие фазовым превращениям, называют критическими точками. Некоторые критические точки имеют названия, например, точки отвечающие началу кристаллизации называют точками ликвидус, а концу кристаллизации – точками солидус.
По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс –концентрация компонентов, по оси ординат – температура.
Шкала концентраций показывает содержание компонента В. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии соответствующие фазовым превращениям в твердом состоянии (3, 4).
По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава, приблизительно, свойства сплава, виды обработки, которые можно применять для сплава.
Основные типы диаграмм состояния
Диаграмма состояния представляет собой графическое изображение состояния любого сплава изучаемой системы в зависимости от концентрации и температуры.
Диаграммы состояния показывают устойчивые состояния, т.е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы.
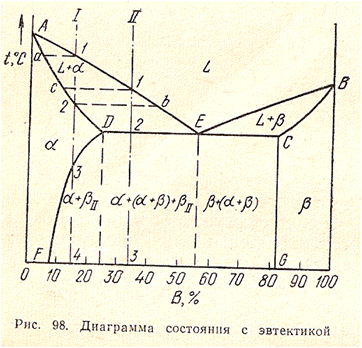
Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов(I рода)
Оба компонента в жидком состоянии нерастворимы и не образуют химических соединений;
Компоненты: вещества А и В(к=2);
Фазы: жидкость L, кристаллы А и кристаллы В (макс. Значение f=3).
I – доэвтектический сплав
II – эвтектический сплав
III – заэвтектический сплав
Эвтектика – механическая смесь 2х или более видов кристаллов, одновременно кристаллизовавшихся из жидкости.
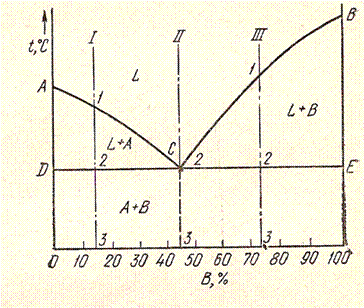
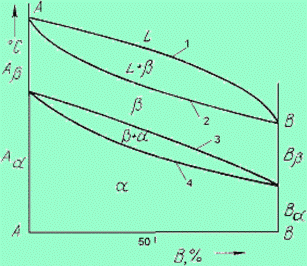
Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии (II рода)
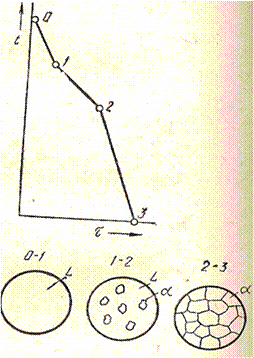
Кривая охлаждения сплава при образовании твердого раствора и схема структур
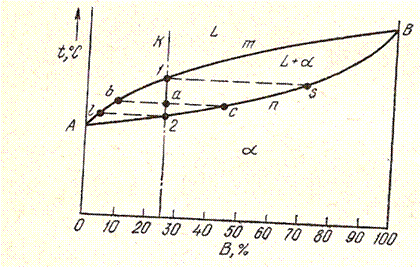
Оба компонента неограниченно растворимы в жидком и в твердом состояниях и не образуют химических соединений;
Компоненты: А и В;
Фазы: L,α.
Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III рода)
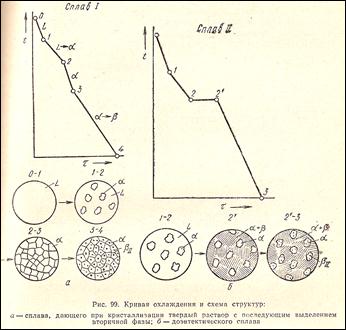
Оба компонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений;
Компоненты: А и В;
Фазы: L,α,β.
Эвтектическая реакция: L→ α+β.
Диаграмма состояния для сплавов, образующих химические соединения
(IV рода)
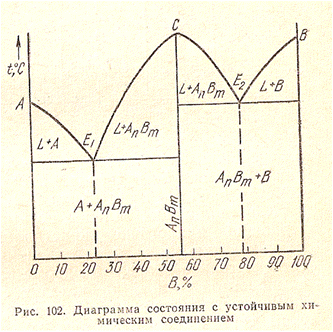
Диаграмма с устойчивым химическим соединением;
Диаграмма с двумя устойчивыми химическими состояниями;
Диаграмма с твердым раствором на базе химического соединения;
Диаграмма с неустойчивым химическим соединением.
Диаграмма с устойчивым химическим соединением
6.3 Железоуглеродистые сплавы. Диаграмма состояния железо-углерод. Перлитное, мартенситное и бейнитное превращения стали. Классификация и маркировка сталей и чугунов. Легированные конструкционные стали
Железоуглеродистые сплавы
Сплавы, содержащие углерода менее 0,02 % (точка Р), называются техническим железом.
Основными сплавами железа являются его сплавы с углеродом – стали и чугуны.
Стали и чугуны различаются в первую очередь содержанием углерода. Сплавы с концентрацией С < 2,14 % (точка Е - максимальная растворимость углерода в железе) называются сталями, а сплавы с концентрацией С > 2,14 % - чугунами.
В результате различного содержания углерода в сплаве образуются разные структуры, что определяет различие в механических и физико-химических свойствах сплавов, а следовательно, и в их применении. Так, стали после затвердевания не содержат хрупкой составляющей - ледебурита, а следовательно, они более пластичные и ковкие. В то же время чугуны по сравнению со сталью обладают значительно лучшими литейными характеристиками, так как их температуры плавления существенно ниже.
Диаграмма состояния железо-углерод
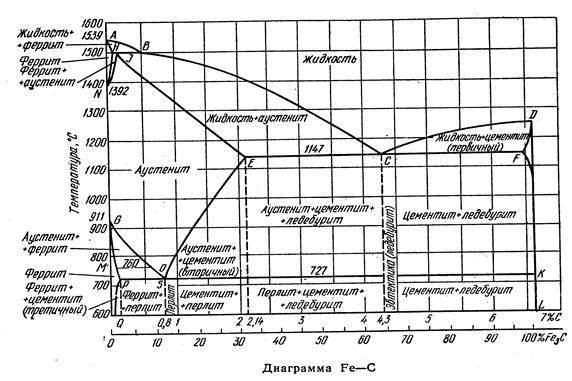
Перлитное, мартенситное и бейнитное превращения стали
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит.
1. Железо – переходный металл серебристо-светлого цвета. Имеет высокую температуру плавления – 1539 ° С
2. Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 °С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000 ° С).
3. Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода.Аллотропических превращений не испытывает.
На диаграмме Fe-FезС выделяются следующие характерные температуры:
Ао = 210 ºС: Fe3C (ферромагнитный) -> Fe3C (парамагнитный);
А1 = 727 ºС: эвтектоидное превращение аустенита (твердый
раствор углерода в y-Fe) в феррит + цементит с образованием пла
стинчатой двухфазной структуры - перлита;
более мелкодисперсные структуры эвтектоидного состава, получаемые при больших переохлаждениях, называют сорбитом (среднедифференцированный перлит)
и трооститом (тонкодифференцированный перлит);
А2 = 768 °С: ферромагнитный α-Fe -> парамагнитный β-Fe;
А3 = 910 °С: (β -Fe —> γ -Fe, для сплавов это соответствует линии GS;
1147 °С: эвтектическое превращение жидкого раствора железа
с углеродом в аустенит + цементит с образованием структуры ледебурита. Температуры, соответствующие линии SE на диаграмме
Fe-Fe3C, обозначают также Аm.
А4 = 1392°С: γ-Fe -> δ-Fe.
Если характерная точка фиксируется при нагреве, к ней добавляется индекс - с, а при охлаждении - r.
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит.
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит (Ф)– твердый раствор внедрения углерода в α-железо.
Углерод располагается в дефектах решетки.
При температуре выше 1392° С существует высокотемпературный феррит. Свойства феррита близки к свойствам железа. Он мягок и пластичен, магнитен до 768° С.
3. Аустенит – твердый раствор внедрения углерода в γ-железо.
Углерод занимает место в центре гранецентрированной кубической ячейки.
Аустенит имеет переменную предельную растворимость углерода: минимальную – 0,8 % при температуре 727° С (точка S), максимальную – 2,14 % при температуре 1147° С (точка Е).
Аустенит парамагнитен.
При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.
4. Цементит – характеристика дана выше.
В железоуглеродистых сплавах присутствуют фазы: цементит первичный (ЦI), цементит вторичный (ЦII), цементит третичный (ЦIII). Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Перлит – механическая смесь тонких пластинок цементита и находящихся между ними более толстых пластинок феррита. Он образуется при 727 ºС из аустенита, содержащего 0,8% углерода.
Ледебурит – механическая смесь (эвтектика) аустенита и цементита; ниже температуры 727˚С аустенит превращается в перлит, при этом образуется смесь перлита и цементита – превращённый ледебурит. Ледебурит содержит 4,3% углерода.
Классификация и маркировка сталей и чугунов
Классификация сталей
По химическому составу: углеродистые и легированные.
По содержанию углерода:
- низкоуглеродистые, с содержанием углерода до 0,25 %;
- среднеуглеродистые, с содержанием углерода 0,3…0,6 %;
- высокоуглеродистые, с содержанием углерода выше 0,7 %
Содержание углерода существенно влияет на свойства стали, поскольку от него зависят относительные количества находящихся в стали мягкого и пластичного феррита и очень твердого, но хрупкого цементита. В связи с этим тесно переплетается классификация сталей по содержанию углерода и назначению:
- низкоуглеродистые стали (до 0,25% углерода) очень пластичны, но сравнительно малопрочны и используются для изготовления слабонагруженных изделий;
- среднеуглеродистые стали (0,3-).6% углерода) сочетают в себе достаточно высокий комплекс вязкостно-прочностных свойств и являются основными конструкционными машиноподелочными материалами;
- высокоуглеродистые стали (0,7-1,3% углерода) обладают очень высокой твердостью, низкими пластичностью и вязкостью. Из них изготавливаются режущий и другой инструмент, а также изделия с высокой износостойкостью.
По равновесной структуре: доэвтектоидные, эвтектоидные, заэвтектоидные.
По назначению углеродистые стали делятся на:
- конструкционные – применяются для изготовления деталей машин и механизмов;
- инструментальные – применяются для изготовления различных инструментов;
- специальные – стали с особыми свойствами: электротехнические, с особыми магнитными свойствами и др.
По способу выплавки:
- в мартеновских печах;
- в кислородных конверторах;
- в электрических печах: электродуговых, индукционных и др.
В зависимости от характера и величины нагрузки, прикладываемой к изготавливаемым из стали изделиям и конструкциям, стали принято делить на стали обыкновенного качества и качественные.
По качеству. (Количественным показателем качества является содержания вредных примесей: серы и фосфора):
– углеродистые стали обыкновенного качества;
– качественные стали;
В сталях обыкновенного качества допускается большее количество серы, фосфора, газов, и других примесей, чем в качественных.
Стали обыкновенного качества делятся на три группы, свойства которых гарантируются ГОСТ 380-71.
У группы А гарантируются только механические свойства. Химический состав не гарантируется. Поэтому из нее можно делать изделия только применяемые механическую обработку (снятие стружки). Нагревы, сварку применять нельзя, так как изменяющиеся при этом свойства можно восстановить только термической обработкой, но для этого надо знать содержание углерода в стали т.е. ее химический состав.
Стали этой группы маркируются так: Ст0,Ст1, …., Ст6. Гарантируемая прочность σв находится в пределах 300-625 МПа, а пластичность δ=22-14%.
Сталь группы Б (БСт0, БСт1,…,БСт6) выпускается с гарантируемым химическим составом. Поэтому при изготовлении изделий ее можно нагревать, например для ковки, а потом при помощи термической обработки исправлять нарушенную структуру и придавать необходимые свойства.
Стали группы В (ВСт0, ВСт1,…,ВСт6) поставляются по механическим свойствам и химическому составу. Они идут для изготовления сварных конструкций.
Качественные углеродистые конструкционные стали выплавляются при более строгом соблюдении технологии выплавки. А содержание вредных примесей серы и фосфора в них не должно превышать 0,03% каждого. Их маркировка состоит из двузначного числа, означающего содержание углерода в сотых долях процента: сталь05, 08,10,15,20,,,,,40,45,…, 85. Из-за высокой хрупкости конструкционные углеродистые стали не содержат углерода свыше 0,85%. Буква А в конце марки свидетельствует об улучшенном металлургическом качестве стали. Из этих сталей делаются детали ответственного назначения.
Инструментальные углеродистые стали являются высокоуглеродистыми (0,7-1,3% углерода). Это гарантирует им высокую твердость необходимую для придания инструменту режущих свойств и износостойкости. Их маркируют У7,У7А,…., У13,У13А. Цифра означает содержание углерода в десятых долях процента, а буква А – улучшенное металлургическое качество.
Маркировка сталей
Принято буквенно-цифровое обозначение сталей
Стали содержат повышенное количество серы и фосфора
Маркируются Ст.2кп., БСт.3кп, ВСт.3пс, ВСт.4сп.
Ст – индекс данной группы стали.
Цифры от 0 до 6 - это условный номер марки стали. С увеличением номера марки возрастает прочность и снижается пластичность стали.
По гарантиям при поставке существует три группы сталей: А, Б и В. Для сталей группы А при поставке гарантируются механические свойства, в обозначении индекс группы А не указывается. Для сталей группы Б гарантируется химический состав. Для сталей группы В при поставке гарантируются и механические свойства, и химический состав.
Индексы кп, пс, сп указывают степень раскисленности стали: кп - кипящая, пс - полуспокойная, сп - спокойная.
 2014-02-13
2014-02-13 1219
1219