- Коррозионностойкие стали.
Коррозия – разрушение метала под воздействием окружающей среды. В зависимости от характера физико-химического воздействия среды различают:
- химическую коррозию, обусловленную воздействием сухих газов и жидкостей, не являющихся электролитами;
- электролитическую коррозию, обусловленную воздействием электролитов.
Химическая коррозия – это чаще всего окисление металлов в газовой среде, усиливающееся при повышении температуры. Защита от окисления металлов основана на образовании защитной окисной плёнки на поверхности. Плёнка должна быть прочной, хорошо сцепляться с поверхностью металла, а главное быть сплошной. Материал будет стоек к химической коррозии, если объём образующегося окисла больше объёма металла его образовавшего. Это и есть условие сплошности плёнки окисла. Этим требованием удовлетворяет плёнка оксида хрома Cr2O3, образующая на поверхности сталей с высоким (более 12%) содержанием хрома.
Электрохимическая коррозия – наиболее распостранённый вид коррозии. Разнородные металлы (или участки различных фаз в сплавах), контактируя с электролитом, образуют гальванический элемент. Металл, имеющий более низкий потенциал (анод) отдаёт ионы в электролит и растворяется (корродирует). Чем ниже электродный потенциал металла по отношению к стандартному водородному потенциалу, тем ниже его коррозионная стойкость. Электрохимическая неоднородность поверхности сплава является причиной коррозии. Чем больше различия электродных потенциалов отдельных структурных состовляющих, тем более сплав склонен к коррозии. Более коррозионно-стойкими являются сплавы со структурой однородного твёрдого раствора.
Различные виды электрохимической коррозии представлены на рис.1.
Равномерная коррозия (а) развивается на поверхности чистых металлов или однородных твердых растворов.
В гетерофазных сплавах развивается местная коррозия (б), охватывающая отдельные участки поверхности с низким электродным потенциалом. К местной коррозии относятся питтинг или точечная коррозия, пятнистая, язвенная. Очаги такий коррозии являются концентраторами напряжения.
В некоторых сплавах границы зерен, обогощенные примесями, имеют низкий электродный потенциал. В них развивается наиболее опасная межкристаллитная коррозия.
Устойчивость против коррозии повышается при введении в состав стали хрома, алюминия, кремния. Алюминий и кремний повышают хрупкость стали, их применяют редко.
Сталь, содержащая более 12% хрома устойчива в атмосфере, морской воде, ряде кислот, щелочей и солей. Примерами таких коррозионностойких сталей являются хромистые стали: 08Х13, 20Х13, 40Х13, 65Х13, 95Х18.
Низкоуглеродистые хромистые стали применяют для изготовления деталей конструкций, высокоуглеродистые (40Х13, 65Х13, 95Х18) для различных инструментов (ножи, скальпели). Помимо хрома коррозиостойкие стали могут содержать никель, эти стали называют хромоникелиевые и они весьма распростронены в качестве конструкционных (12Х18Н10Т, 12Х18Н9, 04Х18Н10, 10Х17Н13М2Т). Эти стали более коррозионностойки чем хромистые и сохроняют эту стойкость при нагреве в отличие от хромистых. Послезакалки хромоникелевые стали имеют структуру однородного аустенита, обеспечивающую их повышенную стойкость.
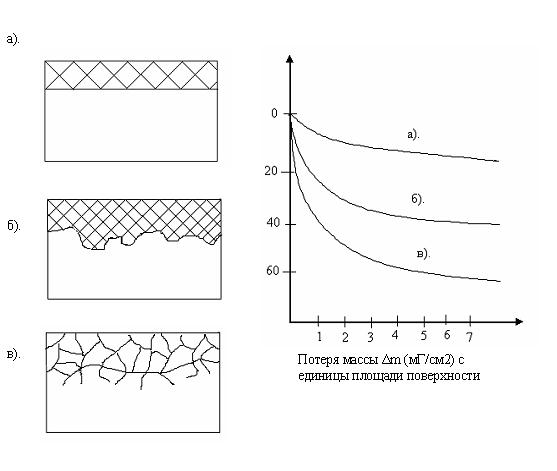
Рис. 1 Основные разновидности электрохимической коррозии (схемы) и их относительное влияние на прочность листового дуралюминия (графики):
а). равномерная коррозия; б). местная коррозия; в). межкристаллитная коррозия
- Жаростойкие и жаропрочные стали.
Способность материала сопротивляться химической коррозии при высоких температурах называется жаростойкостью.
Способность материала сопротивляться деформации и разрушению при высоких температурах называется жаропрочностью. Жаропрочность в сталях достигается легированием тугоплавкими элементами (хром, ванадий, вольфрам, молибден). Эти элементы затрудняют диффузионные процессы и повышают температуру рекристаллизации. Жаропрочностью обладают также хромоникелевые стали аустенитного класса (диффузия в плотноупакованной решетке ГЦК существенно затруднена). Примеры жаропрочных сталей: 12ХМФ. 08Х12ВНМФ, 12Х18Н10Т, 08Х18Н9.
Общим для всех инструментальных сталей является повышенное содержание углерода, обеспечивающее их прочность, твердость, износостойкость. По назначению они делятся на стали для режущего инструмента, штамповочного и измерительного.
Стали для режущего инструмента различают по теплостойкости – способности сохранять твердость при нагреве: низкой теплостойкости (углеродистые и инструментальные стали У7 … У13) для инструмента, не испытывающего нагрева (Т<2000С напильники, зубила, топоры); полу теплостойкими являются среднелегированные стали (9Х5ВФ, 3Х4В3М3Ф2) с теплостойкостью до 4000С; теплостойкие стали сохраняют свои режущие свойства при температурах до 6000С (быстрорежущие стали Р18, Р9, Р6М5).
Стали для штампового инструмента делят на стали для холодного деформирования (отличаются повышенным содержанием углерода Х6ВФ, Х12, Х12М, ХВГ) и стали для горячего деформирования (5ХНМ, 4ХМФС, 3Х2В2Ф, 4Х2В5МФ как правило среднеуглеродистые, легированные хромом, молибденом, вольфрамом, ванадием).
Стали для измерительного инструмента должны обладать высокой твердостью, износостойкостью, стабильностью формы и размеров (У8 … У12, Х, ХГС, ХГВ, 9ХС).
- Медные сплавы.
Медь – металл с ГЦК решеткой, высоким удельным весом (8,95 г/см3), температурой плавления 10830С. Это пластичный материал с высокой электро- и теплопроводностью, низкой твердостью и прочностью. Обладает высокой коррозийной стойкостью. Из-за низкого предела текучести не применяется в чистом виде как конструкционный материал. В чистом виде медь применяют для изготовления электропроводов (высокая электропроводимость) и теплообменников (высокая теплопроводность). Медь широко применяют как основу конструкционных сплавов: латуней и бронз.
Латунь – двойной или многокомпонентный сплав меди, где основным легирующим элементом является цинк. Латуни подразделят на деформируемые и литейные по способу получения заготовок и изделий. Деформируемые отличаются меньшим количеством легирующих элементов и обладают высокой прочностью на ряду с достаточной прочностью. Из них изготавливают трубы, проволоку, профили, листы. Литейные латуни применяются для получения отливок сложной формы литьем в землю, кокиль, под давлением. Для усиления тех или иных свойств латуни помимо цинка легируют железом, оловом, марганцем, кремнием, алюминием, свинцом.
Деформируемые латуни от литейных легко отличить по маркировке: деформируемая ЛАЖ 60-1-1 (после буквы Л подряд начальные буквы русского названия легирующего элемента (кроме цинка), затем подряд идут группы цифр, указывающие процентное содержание меди и по порядку легирующих элементов (кроме цинка); литейная ЛЦ4ОМ\цЗЖ (после буквы Л идут начальные буквы русского названия легирующего элемента (начиная с цинка) и за буквой цифры, отражающие содержание этого элемента в процентах).
Бронзы – многокомпонентные сплавы меди с другими элементами, где цинк не является основным. Подразделяют бронзы аналогично латуням на деформируемые (БрОЦС 4-4-2,5) и литейные (БрО6Ц6С2). Отличия маркировки деформируемых и литейных бронз такие же как у латуней.
- Алюминий и его сплавы.
Алюминий – металл с ГЦК решеткой, низким удельным весом (2,7 г/м3) и температурой плавления 6600С. Обладает высокой электро- и теплопроводимостью, коррозийной стойкостью, пластичностью. Из-за низкого предела текучести алюминий в чистом виде как конструкционный материал не используют, а используют для изготовления электропроводов. Широкое применение нашли алюминиевые сплавы.
Деформируемые алюминиевые сплавы, не упрочняемые термической обработкой.
В этих сплавах содержание легирующих элементов меньше предела растворимости при комнатной температуре (зона I рис. 2). Сплавы эти обладают высокой пластичностью, наибольшей коррозийной стойкостью, но невысокой прочностью. Примерами сплавов этой группы являются сплавы систем Al – Mn и Al – Mg (АМц3, АМг6).
Деформируемые алюминиевые сплавы, упрочняемые термической обработкой.
В этих сплавах содержание легирующих элементов больше предела растворимости при комнатной температуре (зона II рис. 2). Примерами сплавов этой группы являются сплавы систем Al – Сu - дуралюмины (Д1, д16). Эти сплавы достаточно пластичны в состоянии перенасыщенного твердого раствора, а при последующей старении (естественном или искусственном) приобретают высокую прочность. Наибольшей прочностью обладают высокопрочные алюминиевые сплавы системы Al – Zn – Mg – Cu (В95, В96). Самыми легкими являются сплавы системы Al – Mg – Li (1420).
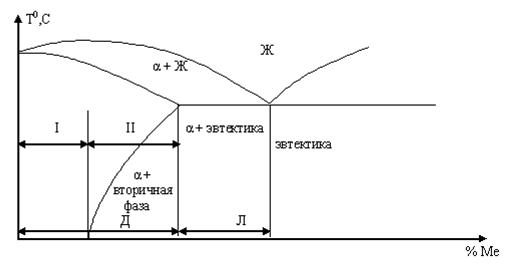
Рис. 2 Типовая диаграмма (схема) состояния системы Al – легирующий элемент (Ме).
Д – деформируемые сплавы, Л – литейные.
I – деформируемые сплавы, не упрочняемые термической обработкой; II - деформируемые сплавы, упрочняемые термической обработкой.
 2015-01-30
2015-01-30 1154
1154
