Схема данного гальванического элемента
(-)Fe|Fe2+||Ag+|Ag(+).
ОВ-пара Fe|Fe2+ имеет меньший потенциал (-0,44 В), чем ОВ-пара Ag+|Ag (+0,80 В), поэтому железо выполняет роль анода, серебро - роль катода.
Анод: Fe-2 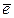 = Fe2+ 1 (окисление)
= Fe2+ 1 (окисление)
катод: Ag+ + 1 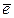 = Ag 2 (восстановление)
= Ag 2 (восстановление)
_____________________________________________
Суммарный процесс: Fe + Ag+ = Fe2+ + Ag
Чтобы определить ЭДС гальванического элемента, нужно рассчитать потенциалы электродов при данных концентрациях ионов
φ (Fe2+ / Fe) = -0,44 + (0,059/2)lg 0,1 = -0,44- 0,029 = -0,469 В;
φ (Ag+/ Ag) =0,80 +(0,059/1)lg0,1 = 0,80-0,118 = 0,682 В;
ЭДС = φк- φА = φ (Ag+ /Ag)- φ (Fe2+/Fe)= 0,682-(-0,469) = 1,151 В.
Ответ: 1,151 В.
 2015-01-30
2015-01-30 493
493








