Изотермическим процессом называется процесс, протекающий при постоянной температуре: Т= const.
На рис. 10 показана диаграмма изотермического процесса. Процесс расширения газа на диаграмме соответствует переходу из состояния 1 в состояние 2, процесс сжатия — переходу из состояния 2 в состояние 1.
Поскольку в изотермическом процессе Т = const, то уравнение состояния газа pv = RT = const.
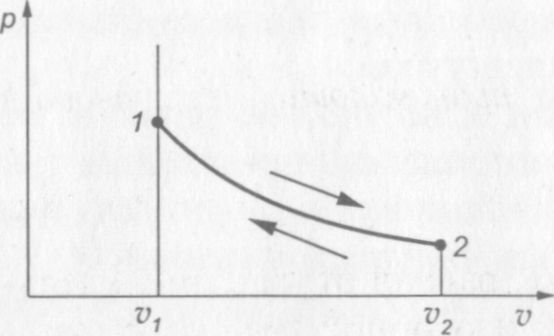
Рис. 10. р— v диаграмма изотермического процесса
В изотермическом процессе в соответствии с законом Бойля—Мариотта справедливо следующее соотношение:
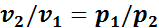 (1.11)
(1.11)
или
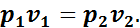
Соотношение (1.11) показывает, что в изотермическом процессе объемы при различных состояниях газа обратно пропорциональны давлениям, соответствующим этим состояниям.
При вычислении внутренней энергии, используя общую формулу (1.6), получим
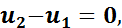
так как
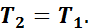
Следовательно, в изотермическом процессе изменение внутренней энергии равно нулю, т. е. внутренняя энергия в течение всего процесса остается постоянной.
Удельная работа изменения объема в изотермическом процессе определяется уравнением
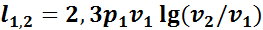
или
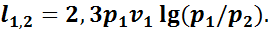 (1.12)
(1.12)
На основании первого закона термодинамики
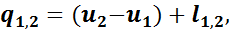
а так как u 2 - u 1 = 0, то
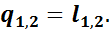
Таким образом, в изотермическом процессе расширения вся подведенная теплота расходуется на внешнюю работу, а при изотермическом процессе сжатия внешняя работа полностью превращается в теплоту.
 2015-01-30
2015-01-30 670
670