Пример 1. Энтальпия образования воды:
2H2(г) + O2(г) =2H2O(г) 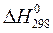 = - 484кДж.
= - 484кДж.
Отсюда следует, что энтальпия образования воды в газовой фазе равна - 484кДж: 2моль = -242 кДж/моль
ЭНТАЛЬПИЯ РЕАКЦИИИ рассчитывается из следствия закона Гесса: «Энтальпия химической реакции равна сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом стехиометрических коэффициентов».
ΔНр = ∑(n∙ΔH)прод. - ∑(n∙ΔH) исх.,
где n – число молей.
Пример 2. Рассчитать тепловой эффект реакции. Указать эндо- или экзотермическая реакция при стандартных условиях.
4NH3(г) + 5O2(г) = 4NO(г) + 6H2O(г)
Число молей,n 4 5 4 6
Энтальпия, 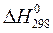 -46,0 0 +91,0 -242,0
-46,0 0 +91,0 -242,0
∆Н0реакции = [4(+91)+6(-242)]-[4(-46)+5·0]= -904кДж.
Так как ∆ Н< О, данный процесс сопровождается выделением тепла, т.е. является экзотермическим.
Таблица № 1
Значения термодинамических функций в стандартных условиях
| Вещество | Агрегатное состояние | 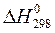 кДж/моль кДж/моль
| 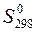 Дж/моль оК Дж/моль оК
| 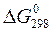 кДж/моль кДж/моль
|
| 1 | 2 | 3 | 4 | 5 |
| Al Fe O2 H2 C Al2O3 CO CO2 CH4 C2H2 C3H8 C4H10 CaO Ca(OH)2 CaCO3 Fe2O3 Fe3O4 Na2CO3 MgO MgCO3 H2O H2O H2S SO2 SO3 P2O5 NO NH3 | ТВ. ТВ. Г. Г. Графит ТВ. Г. Г. Г. Г. Г. Г. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. Ж. Г. Г. Г. Г. ТВ. Г. Г. | - 1676,8 - 110,6 - 393,8 - 74,9 - 226,8 - 95,4 - 101,2 - 635,0 - 986,8 - 1207,0 - 822,7 - 1117,9 - 1137,5 - 601,8 - 1113,0 - 286,4 - 242,0 - 20,9 - 297,2 - 376,2 - 1492,0 91,0 - 46,0 | 28,4 27,2 205,0 130,7 5,7 50,9 197,6 213,6 186,4 - - - 39,7 83,4 91,7 87,5 146,3 136,4 26,9 65,7 70,0 188,9 193,2 248,2 256,4 114,5 210,5 192,6 | -1563,3 -137,2 -394,4 -50,9 — — — -603,6 -899,2 -1128,4 -740,8 -1014,8 -1047,5 -569,6 -1029,3 -237,4 -228,8 -33,8 -300,4 -370,0 -1348,8 86,6 -16,6 |
Термодинамика устанавливает также направление самопроизвольного протекания процессов в данных условиях. При выяснении природы самопроизвольного протекания реакции было установлено, что самопроизвольные реакции сопровождаются экзотермическим эффектом (∆Н<Ο). Однако связь между снижением энтальпии системы и самопроизвольностью протекания процесса является недостаточным фактором.
|
|
|
Другим фактором определения самопроизвольности протекания процессов является термодинамическая функция называемая энтропией (S). Энтропия является мерой упорядоченности состояния системы. В ходе химической реакции энтропия системы изменяется. Это изменение называется энтропией реакции.
ЭНТРОПИЯ РЕАКЦИИ также рассчитывается по следствию закона Гесса.
∆Sp = ∑ (n · S) прод.— ∑ (n ∙ S) исх.
Пример 3. Рассчитать изменения энтропии системы при реакции в стандартных условиях.
N2(г) + О2(г) = 2NO(г)
Число молей, n 1 1 2
Энтропия 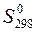 192 205 211
192 205 211
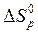 = 2 · 211—(1 · 192 + 1·205) =14 Дж/моль. К
= 2 · 211—(1 · 192 + 1·205) =14 Дж/моль. К
Все процессы, которые протекают с уменьшением порядка системы, сопровождаются увеличением энтропии и наоборот. Самопроизвольно протекают процессы, идущие с увеличением энтропии. Для процессов протекающих в изобарно - изотермических условиях (p = const, T = const) движущей силой самопроизвольного процесса является стремление системы перейти в состояние с наименьшей энтальпией (энтальпийный фактор), либо с увеличением энтропии (энтропийный фактор). Устойчивому состоянию системы соответствует равенство этих факторов.
|
|
|
∆Н ═ Т ∙ ∆S
Термодинамическая функция, показывающая насколько система в данном состоянии отклонилась от равновесного, называется энергией Гиббса (G).
∆G = ∆Н − Т ∙ ∆S
Если: ∆G < 0, процесс может протекать самопроизвольно в прямом направлении;
∆G = 0, процесс в состоянии равновесия;
∆G > 0, процесс самопроизвольно в прямом направлении
проходить не может.
Из соотношения ∆G = ∆Н − Т ∙ ∆S видно, что самопроизвольно могут протекать процессы:
1. экзотермические: (∆Н < 0). Для которых: ∆S > 0.
2. эндотермические: (∆Н > 0). Для которых: ∆S > 0, но /Т·∆S/>/∆Н /,т.е. при высоких температурах.
ЭНЕРГИЯ ГИББСА РЕАКЦИИ также рассчитывается по следствию закона Гесса.
∆Gp = ∑ (n · ∆G) прод.— ∑ (n ∙ ∆G) исх.
Пример 4. Указать возможность самопроизвольного протекания реакции при стандартных условиях.
СО2(г) +С(графит) = 2СО(г)
Число молей, n 1 1 2
Энергия Гиббса, 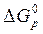 -394 0 -137
-394 0 -137
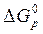 = [ 2 · (-137)] − [1 · (-394) + 1 · 0 ] = + 120 кДж/моль
= [ 2 · (-137)] − [1 · (-394) + 1 · 0 ] = + 120 кДж/моль
Так как 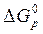 > 0, в данных условиях процесс невозможен.
> 0, в данных условиях процесс невозможен.
 2015-01-30
2015-01-30 554
554








