Катализаторы – это особые вещества, увеличивающие скорость химической реакции, не влияющие при этом на положение равновесия. Помимо увеличения скорости превращения исходных реагентов, катализаторы должны обладать в ряде случаев селективным воздействием по отношению к одной или группе реакций, т.е. преимущественно увеличивать скорость целевой реакции.
Ускоряющее воздействие объясняется тем, что в отличие от некаталитической реакции, требующей для преодоления большего активационного барьера, в присутствии катализатора меняется путь реакции, т.е. катализатор образует с реагентами ряд промежуточных соединений. Энергия активации образования каждого их них меньше энергии активации некаталитической реакции.
Рассмотрим энергетическую картинку реакционной системы для реакции
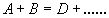 , проходящей в отсутствии катализатора по схеме
, проходящей в отсутствии катализатора по схеме
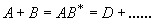 через образование активного комплекса.
через образование активного комплекса.
В присутствии катализатора реакция идет по другому пути: через несколько элементарных стадий:
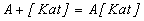 ;
;
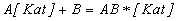 ;
;
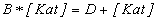 .
.
Технологическими параметрами катализатора являются: температура зажигания, селективность, износоустойчивость, отравляемость и т.п. Основной характеристикой катализатора является активность А, которая определяется отношением констант скорости 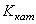 и
и 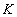 :
: 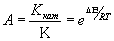 .
.
При всех различиях в механизмах гетерогенно-каталитических реакций, обилии твердыйх катализаторов имеющих разные структуры, методы приготовления, математической описание, в подавляющем большинстве случаев основано на рассмотрении двух типов процессов: на непористом и пористом зерне катализатора
 2014-09-02
2014-09-02 374
374








