Титрование – один из методов определения концентрации, основанный на измерении объемов растворов, вступающих в реакцию веществ.
В основе определения временной жесткости воды лежит способ титрования воды соляной кислотой в присутствии индикатора метилоранжа. Это возможно, так как вода, содержащая растворимые гидрокарбонаты кальция и магния - Ca(HCO3)2 и Mg(HCO3)2, имеет щелочную среду (рН>7). Метилоранж в ней окрашен в желтый цвет. В кислой среде (при рН < 7) он изменяет свой цвет на красный, а в точке перехода от щелочной среды к кислой имеет оранжевый цвет. При титровании такой воды раствором HCl протекает реакция нейтрализации:
OH– + Н+ = Н2О
Выполнение опыта
С помощью мензурки отмерьте 100см3 воды и перенесите ее в коническую колбу, в которой в дальнейшем будете проводить титрование. Далее, в воду добавьте 2-3 капли индикатора – метилоранжа (обратите внимание на окраску раствора).
В бюретку налейте раствор HCl с эквивалентной концентрацией 0,1 ммоль-экв/дм3 и установите уровень кислоты на нулевом делении. После этого приступайте к титрованию.
Титрование проводите следующим образом: в колбу с водой осторожно, по каплям, приливайте раствор HCl при постоянном перемешивании. Наблюдайте за изменением окраски раствора от желтой до оранжево-розовой. При достижении заданной окраски раствора титрование прекратите и определите, какой объем раствора HCl был израсходован на титрование воды.
Аналогично проведите титрование еще в двух параллелях (каждый раз колбу после титрования тщательно ополаскивайте дистиллированной водой). Следует отметить, что при титровании эксперимент можно считать успешным, если расхождение в параллелях не превышает 0,05 см3.
Запись результатов опыта
Экспериментальные данные представьте в виде таблицы
| № опыта | Объем воды, (VH2О , см3) | Объем раствора HCl, (VHCl , см3) | Средний объем HCl (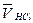 , см3) , см3) | Эквивалентная концентрация раствора HCl (Сэкв ) |
Рассчитайте временную жесткость воды, используя соотношение:
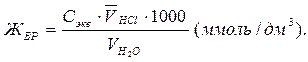 |
В выводе дайте понятие временной жесткости и укажите способы ее устранения.
 2015-02-27
2015-02-27 5610
5610








