Концентрационная коагуляция происходит под действием индифферентного электролита, при этом потеря устойчивости вызывается сжатием диффузной части ДЭС при неизменном потенциале ядра.
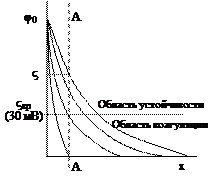

Добавление в золь идифферентного электролита приводит к сжатию ДЭС и снижению ς-потенциала за счет подавления диффузии и перемещения ионов из диффузного в адсорбционный слой.
Например, концентрационную коагуляцию положительного золя хлорида серебра
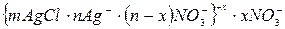
будет вызывать индифферентный электролит KNO3.
При 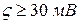 система устойчива: силы электростатического отталкивания преобладают над силами притяжения. Зависимость скорости коагуляции от концентрации электролита представлена на рис. Как видно, коагуляции не наблюдается и скорость ее равна нулю (участок I).
система устойчива: силы электростатического отталкивания преобладают над силами притяжения. Зависимость скорости коагуляции от концентрации электролита представлена на рис. Как видно, коагуляции не наблюдается и скорость ее равна нулю (участок I).
 При снижении ς-потенциала до критического значения
При снижении ς-потенциала до критического значения 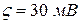 происходит ослабление сил электростатического отталкивания. В результате частицы подходят друг к другу на более близкое расстояние и за счет сил межмолекулярного притяжения слипаются. Начинается медленная коагуляция (участок II). Скорость медленной коагуляции зависит от концентрации электролита. Чем выше концентрация электролита, тем меньше ς-потенциал и больше скорость коагуляции.
происходит ослабление сил электростатического отталкивания. В результате частицы подходят друг к другу на более близкое расстояние и за счет сил межмолекулярного притяжения слипаются. Начинается медленная коагуляция (участок II). Скорость медленной коагуляции зависит от концентрации электролита. Чем выше концентрация электролита, тем меньше ς-потенциал и больше скорость коагуляции.
При достижении изоэлектрической точки (ς = 0) скорость коагуляции перестает зависеть от концентрации электролита (участок III). Начинается быстрая коагуляция. Минимальная концентрация электролита, при которой начинается видимая коагуляция (концентрация электролита, при которой ς = 0), называют порогом коагуляции Ск.
Величина, обратная порогу коагуляции называется коагулирующей способностью. Коагулирующая способность Vк – это объем золя, который коагулирует под действием 1 моля электролита:
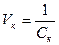 .
.
Чем меньше порог коагуляции, тем выше коагулирующая способность электролита.
Коагулирующим действием обладает не весь электролит, а только тот ион, заряд которого совпадает по знаку с зарядом противоиона мицеллы гидрофобного золя. Этот ион называется ионом-коагулятором.
Коагуляция электролитами подчиняется нескольким эмпирическим правилам.
1. Коагулирующая способность иона-коагулятора тем больше, чем больше заряд иона(первое правило Шульце-Гарди):
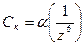 ,
,
где α – постоянная для данной системы величина: при z = 1 α = Ск;
z – заряд иона-коагулятора.
2. При одинаковом заряде коагулирующая способность иона тем выше, чем больше его кристаллический радиус (второе правило Шульце-Гарди). В соответствии с этим правилом коагулирующая способность иона определяется его положением в лиотропном ряду (см. п. «Адсорбция электролитов»):
одновалентные катионы: Li+ < Na+ < К+ < Rb+ < Cs+
двухвалентные катионы: Mg2+ < Ca2+ < Sr2+ < Ba2+
 одновалентные анионы: Сl– < Br– < NQ3– < I– < CNS–.
одновалентные анионы: Сl– < Br– < NQ3– < I– < CNS–.
коагулирующая способность возрастает
 2015-02-27
2015-02-27 1250
1250