Числовое значение молярной газовой постоянной определим из формулы (42.4), полагая, что моль газа находится при нормальных условиях (ро= 1,013 105 Па,
Т0=273,15 К, Vm=22,41.10-3 м3/моль): R=8,31 Дж/ДмольК).
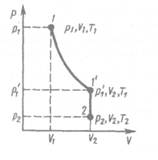
От уравнения (42.4) для моля газа можно перейти к уравнению Клапейрона — Менделеева для произвольной массы газа. Если при некоторых заданных давлении и температуре один моль газа занимает молярный объем Vm, то при тех же


|
|
условиях масса т газа займет объем V= (m/M) Vm, где М — молярная масса (масса
одного моля вещества). Единица молярной массы — килограмм на моль (кг/моль). Уравнение Клапейрона — Менделеева для массы т газа
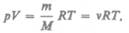 (42.5)
(42.5)
где 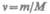 — количество вещества.
— количество вещества.
Часто пользуются несколько иной формой уравнения состояния идеального газа, вводя постоянную Больцмана:

 2015-02-04
2015-02-04 222
222








