Жалпы ашу процесімен адам баласы өте ертеден таныс болған. Ашу процесінің микроорганизмдер көмегімен жүретінін алғаш Л. Пастер (1860ж.) зерттеді. Бұдан кейінгі зерттеулер ашу процесінің микроорганизмдер ферменттеріне байланысты екенін дәлелдеді.
Ашу процесі. Тотығу-тотықсыздану процесін ашу процесі деп атайды. Процестің жүру кезінде АИФ түзіледі. Ашу процесі кезінде сутегі доноры және акцептор қызметін ашу процесі нәтижесінде түзілетін органикалық қосылыстар атқарады.
Ашу процесінің қоздырғыштары – облигатты анаэробты микро-организмдер. Ол тек қана анаэробты жағдайда жүреді. Ашу процесінің оттегінсіз жағдайда жүретінін 1860 жылы Л. Пастер ашқан.
Спирт алуда қолданылатын ашытқылар негізінде Saccharomyces туысына жатады. Saccharomyces туысына жататын ашытқылардың жеті түрі бар:
Sacch. cerevisiae, Sacch. kluyveri, Sacch. exiguous, Sacch. dairensis, Sacch. serrazzii, Sacch. tellustris, Sacch. unisporus. Sacch. cerevisiae туысының синонимі болып, Sacch. bayanus, Sacch. carisbergensis және де басқа өнеркәсіпте маңызды бірқатар ашытқыларда бар.
Sacch. cerevisiae штамының маңызы зор. Бұл түріне нан ашытқысында, спирт өндірісінде, шарап және сыра қайнатқанда, квас өндірісінде қолданылатын ашытқылар жатады.
Saccharomyces cerevisiae Hansen.Үш күн солод сусласында 280С темпертурада культивирлегенде жасуша формасы сфера тәрізді, эллипс тәрізді немесе ұзарған пішінді болып келеді; кейде жалғыз немесе жұбымен орналасып қысқа тізбек болып орналасады.Штамның жасушасының өлшеміне қарай үш морфологиялық топқа бөлінеді. Бірінші топқа ең ірі жасушалар (3,5-10,5 ´ 5,0-21,0 мкм, екінші топқа сәл кішірек жасушалар (2,5- 7,0 ´ 11,0-19,0 мкм), үшінші топқа аралық жасушалар (3,5-8,0 ´ 5,0-11,5-18,0 мкм) жатады. Ал кейбір жасушалар ұзарып 30 мкм және одан да астам болады, бұл ашытқылардың ішінде паста тәрізді, крем не қоңыр крем тәрізділеріде болады, былайша тегіс жылтыр кейде біраз көбіршіктенген немесе беті жылтыраған нүктелермен жабылған болып келеді.
Аско тәрізді көбейетін ашытқыны ацетатты агарға отырғызғанда оңай пайда болады. Аско тәрізді бір - бірден төртке дейін шар немесе элипс тәрізді формада спора түзіледі.
Штамдар әртүрлі қабілеттілікте витаминсіз өсе алады.Sacch. cerevisiae штамы төменгі және жоғарғы ашытушы болып бөлінеді.
Тамақ өндірісіндегі ашытқы сахаромицетке жатпайтындар технологиялық процесті бүлдіріп теріс қызмет атқарады және дайын өнімнің, шикізаттың бұзылуын тудырады.
Түптік ашу жүрген кезде түбіне тығыз тұнба жиналып, берік тұнба қалыптасады, ал беттік ашу жүрген кезде – қалпақша бетіне үрленіп шығып, «қалпақ» түзеді. Жасуша бүршіктенгеннен кейін тізбек құрайды да ішіндегі көмір қышқыл газын жоғары шығарады. Ашытқы ашыған ортада жүргенде сондай-ақ мақта қауашағы тәрізді бөлінеді. Осы бөлу негізінде оның флокуляциялық қасиетінде айырмашылығы болады. Мақта қауашағы тәрізді ашытқы ашудың соңында түйіршіктеліп жабысады және әлде түбіне тұнады, ашытқы беткі жағына көтеріліп флокулирленеді, түптік ашу сияқты және сондай-ақ беттік ашу процесі жүреді.
Ашыту іс жүзінде қолданғанда түптік және беттік ашытқылар деп ажыратады. Беттік ашытқыны өсіру үшін 18 –300С температура жылылық қажет. Мұнда көмір қышқыл газы көп бөлінеді де, қоректік орта көпіріп кетеді. Сол кезде ашытқылар өздері ашыған сұйықтың бетіне көтеріледі. Бұларды спирт және нан өндіруде қолданады.Түптік ашытқының ашу процесі 4-100С температурада жүреді. Сонда ашу процесі біршама тыныштықта өтеді де, ашытқылар ыдыс түбіне тұнады.
Ашытқының топтары көп. Олардың кейбіреулері адамға зиянын тигізеді. Олар түрлі тағамдарды, шараптарды бүлдіреді.Ашытқылар табиғатта кеңінен тараған. Ашытқыларды топырақтан, судан, өсімдіктен табуға болады.
Жаңа ашытқы рассасын таңдау. Штамды бөліп алу лабораториялық және өндірістік жағдайда зерттеледі. Расса ашудың жақсы көрсеткішін беретін өндірістік болады және іс жүзінде кеңінен қолданылады.
Селекционерлердің ашытқы рассасын жасанды әрекетінің әсерінен жасалған мутагенді факторлардың көптеген тәжірибесі сәтсіз аяқталды. Лабораториялық жағдайда бағалы қасиетке ие болатын мутанттар, былайша өндірістік жағдайда бәсеке таластықты ұстай алмайды және ығыстырылды.Бірқатар өндіріс салалары үшін соңғы жылдары ашытқы рассасының селекциясы кезінде (мелассадан алынатын спирт өндірісі үшін, күлше нан үшін) гибридизация әдіс сәтті қолданылды. Гендік инженерия әдісі арқылы жоғары эффективті ашытқы рассасын алуға болады. Спирт ашу процесінің негізгі ашытқылары адам баласының өмірінде үлкен мәнге ие. Ашытқыларды нан пісіруде, спирт алуда және тағы басқа өнімдерді алуда қолданады.
Ашытқылар қантты анаэробты жағдайда ашытқанда одан спирт, көмір қышқыл газы және энергия бөлінеді.
Спирттік ашу процесі кезінде этил спиртінен басқа сірке альдегиді, глицерин, сірке және янтарь қышқылдары, сивуш майлары түзіледі. Сивуш майларының түзілуі ортадағы аминқышқылдарының ыдырауына байланысты. Мұнда аминқышқылдарынан бөлінетін аммиакты ашытқылар азоттың қоректік көзі ретінде пайдаланып, ортада сивуш майларының жиналуына көмектеседі. Спирттік ашу процесін қоздыратын сахаромицет туысына жататын ашытқылар. Егерде ортада ауа көп болса, ашытқылар көмірсуларды тотықтырып, ашу процесін тыныс алу процесіне қарай бағытайды. Мұнда көмірсуларды пайдалану коэффициенті артады. Сондықтан ашытқылардың массасын көптеп алу үшін оларға ауа үрлейді. Осындай әдісті нан және мал азықтық ашытқыларды өндіруде кеңінен қолданады. Ал спирт алуда процесс анаэробты жағдайда жүреді.
Ашытқылар кез келген көмірсуды ашытпайды. Мұның себебі оларда амилаза ферменті болмайды. Сондықтан крахмалды өндірісте алдын ала фермент көмегімен моно және дисахаридтерге айналдырады. Ал ашытқылар клеткасындағы мальтоза ферменті, дисахарид мальтозаны глюкозаға айналдырады. Глюкозадан көптеген ферменттердің көмегімен ашытқылар спирт пен көмір қышқыл газын түзеді.
Бұл процесс мынадай схемамен жүреді: крахмал + амилаза ферменттері →мальтоза қанты + мальтоза ферменті → глюкоза; глюкоза қанты + зимаза ферменті → этил спирті және көмір қышқыл газы.
Ашытқылардың қантты ашытып, этил спиртін және көмір қышқыл газын түзуі Эмбден-Мейергоф-Парнас схемасы бойынша жүзеге асады.
Спирттік ашу процесі қышқылды ортада (рН 4,5-50) жақсы жүреді. Егерде қоректік орта реакциясы сілтілі болса (рН 8,0), онда негізгі өнімдердің бірі ретінде глицерин пайда болады. Мұнда спирттік ашу процесі мына реакция бойынша жүреді:
2С6Н12О6+Н2О=СН3 СООН+СН3 СН2ОН+2СН2ОНСНОНСН2ОН+2СО2
Егерде қоректік ортаға натрий сульфаты қосылса глицерин өнімі арта түседі. Мұнда сірке альдегиді сульфитпен қосылады да, сутегі көмегімен этил спиртіне дейін тотықсыздана алмайды. Кейбір жағдайда спирттік ашу процесінің көмегімен глицерин және амин спиртін алуға тура келеді. Ондайда көрсетілген реакция қолданылады.
Егерде гексоза қантын ашытқылар жақсы ашытса, пентоза қантын олардың кейбір топтары ғана сіңіре алады. Кейбір ашытқылар жай декстринді ашытады, бірақ крахмалға әсер етпейді. Көпшілік спирт зауттарында қант алу мақсатында клетчатканы алдын ала қышқылмен әсер ету арқылы ыдыратады. Мұндай заттың көзі мол болғандықтан, спирт алудың осындай тәсілі арзанға түседі.
Азот көзі ретінде ашытқылар ақуызды, аминқышқылдарын, пептонды және аммоний тұздарын пайдаланады. Өніп-өсу барысында ашытқылар бірқатар витаминдерді, кейбір өсуді қолдаушы заттарды түзеді. Қолайлы жағдайда ашытқылардың 10 млрд. клеткасы 20-24 мг азотты сіңіре алады. Егерде өндірісте ашытқылардың өзін көбейтіп алу мақсаты көзделсе, онда қолайлы қоректік ортада 6 сағат ішінде бұл процесс аяқталады. Мұнда ортаға ашытқылар мөлшерін көп етіп салу керек.
Фосфор қоректік заттың қажетті құрамы болып есептеледі. Ол цитоплазма және көптеген ферменттер құрамына кіреді. Ашытқыларды өсіретін қоректік ортаға фосфор көзі ретінде техникалық фосфорды (0,5%) немесе 10% суперфосфат қосады. Қоректік ортаға ауа үрлегенде ашытқылар фосфорды жақсы пайдаланады.
Ашу барысында пайда болған заттар олардың тіршілігін тежейді және ашыту қабілетін тым төмендетіп жібереді. Ортада спирт көбейген сайын ашу процесі баяулайды. Спирт концентрациясы 12-16%-ке жеткенде ашытқылар тіршілігі тоқталады. Егер ашытқы өскен қоректік орта жаңартылмаса олардың тіршілігі спирт концентрациясы 5 %-ке жеткенде тоқтайды. Қоректік орта өне бойы ауысып, жаңарып отырса ашытқылар қантты ашытып ортада 7 %-ке дейін спирт жиналғанша тіршілік ете алады.
 |
 |
|
 культурасын дайындау
культурасын дайындау
 |
|

Басты өнім

|
 Сивуш майы
Сивуш майы Лютерлі су


Барда
 | |||
| |||
ашытқы
 құрғақ
құрғақ
 ашытқы
ашытқы


|
 екіншілік бу
екіншілік бу
|
 | |||
 |
|
49 сурет- Мелассадан спирт алу өндірісінің технологиялық сызба нұсқасы
Ашытқылар тіршілігі барысында түзілетін көмір қышқылы да олардың дамуын тежейді. Көмір қышқыл газы көп бөлінгенде қоректік орта көбіктеніп кетеді. Бұл ашу процесіне технологиялық тұрғыдан зиянды.
Ашытқы ақуыздары аминқышқылдарына бай. Олардың ішінде организмге қажетті алмастырылмайтын амин қышқылдары да бар.
Мелассадан спирт алу өндірісінің технологиялық сызба нұсқасы құрамында крахмалы бар шикізаттан спирт алуға қарағанда қарапайым, себебі мелассаны қанттың өзі құрайды. Оны ашытқымен ашытуға болады.
Осының арқасында ашытуға дайындайтын құрамында крахмалы бар шикізатты дайындау үшін қайнату және қанттандыру процесі болмайды.
Мелассалы бардада ашытқы, тыңайтқыш және басқа өнімді алу үшін қолданылатын бағалы заттар құрайды. Соның ішінде мелассадан спирт алу өндірісінің технологиялық сызба нұсқасымен құрамында крахмалы бар шикізат бидайдан, картоптан спирт алудан негізгі айырмашылығы дайындау сатысы.
Мелассаны ашытуға дайындауда алдымен залалсыздайды және қоректік заттармен байытады, гомогенизациялайды, содан соң түссіздендіреді. Мелассаны антисептирлеудің мақсаты – ашытқыны өсуі үшін қолайлы жағдай жасау және бөгде микрофлораны залалсыздау температурасына дейін қыздырады, сосын ұстайды, салқындатады және күкірт қышқылмен қышқылдайды.
Сонымен қатар арнайы антисептикті қолданады. Мелассаның құрамында ашытқының өсуіне қажетті қоректік тұздарды азот пен фосфорды қосады. Өңделген мелассаны жинағышқа салады, сол жерде араластырады және 8-10 сағат сақталады, сосын сумен араластырады. Мелассаның құрамында ұсақ бөлшектерді жою үшін тұндырғыш центрифугадан (сепаратор) өткізіледі, сосын ашыту бөліміне жібереді.
Үздіксіз әдіспен мелассалы сусланы ашыту процесінде қант гидролизденеді де, глюкозаға және фруктозаға айналады және ол жерде спиртке айналады.
Құрамында крахмалы бар шикізаттан спирт алу өндірісіндегі технологиялық процестің негізгісі болып қайнату қаттандыру, ашыту саналады. Қайнатудың алдында дайындық операциялары жүргізіледі, жуу, шикізатты дайындау.
Спирт өнімін алуда технологиялық талаптарға сай келетін картоп өнімі өзінің эффективтілігінің арқасында сәйкес келеді. Картоптан бидайға қарағанда 3-4 есе крахмал артық алынады. Картоп крахмалы жылдам қайнатылады, сусла жасауға қолайлы. Суслада азот және фосфор өнімі бар. Бұл өнім ашытқыны қоректендіруге тиімді, осыдан өте жоғарғы дәрежелі спирт алуға мүмкіндік туғызады. Картопты қайта өңдеу процесі кезінде спиртті шығару өнімділігі бидайды өңдеуге қарағанда 10%-ке артады, ал отынның шығымы 12% -ке төмендейді.
Картоптан спиртті өндіруде негізгі кемшілігі болып картопты өңдеу процесінің қиындығы, ылғалда сақталу төмендігі және алыс жолға тасмалдағанда шыдамсыздығы болып табылады.
Алдымен крахмалдың концентрациясына, картоп бөлшектерінің өлшемдеріне және қайнату жылдамдығына байланысты болады.
Толық ісіну және клейстеризация процесі орындалады. Сондықтан да қоспаны 60-650С температурада қайнату процесін барлық өндіріс орындары жүргізеді. Қайнату процесі аппаратта 95-970С температурада жүреді.
Картоп немесе бидайдан жасалған қайнатылған массаны 58-600С температурада суытылғаннан кейін қанттандырады (гидролездейді), бұл процесс бізге суслоны алу үшін қанттандырушы материал ферменттер көмегімен жүзеге асырылады.
 | |
 |
|
 | |||
 |
|
 | |||
 |
термамил
 | |||
 |
|
 | |||||
 | |||||
 |
|
|
 | |||||
 | |||||
 | |||||
| Ашуы жетілген ашытпаны айдауға жіберу |
50 сурет-Картоптан этил спиртін алудың технологиялық сызба нұсқасы
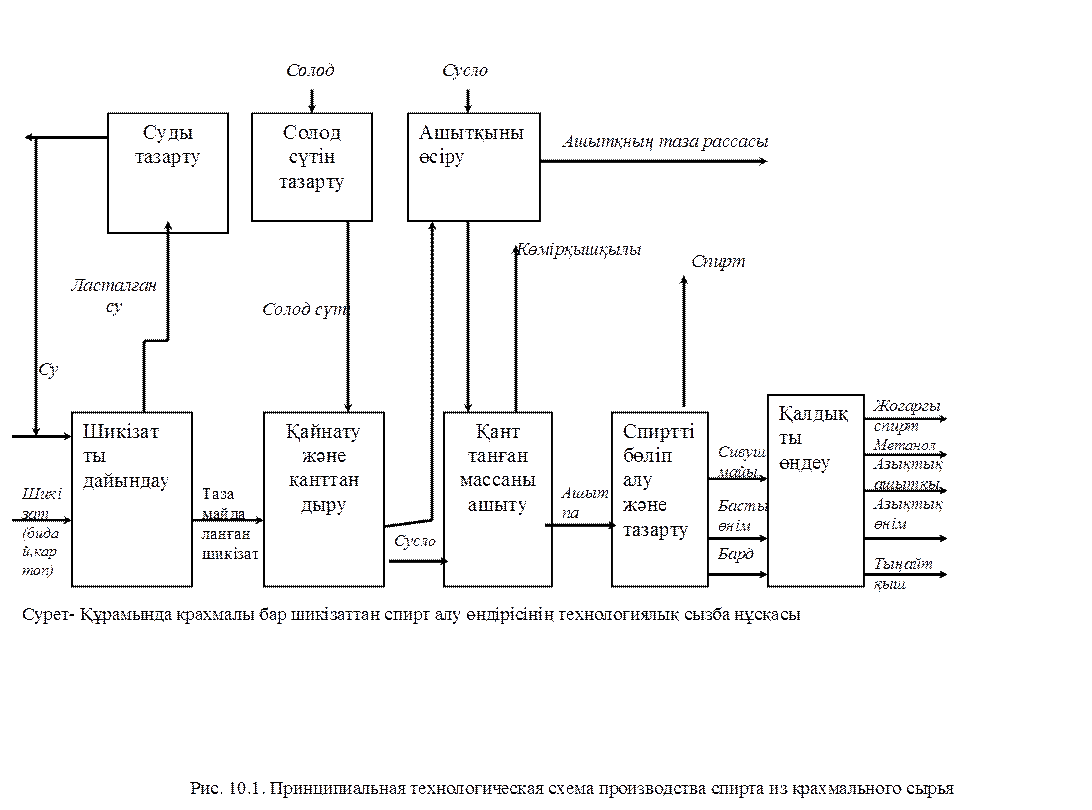
Қанттандырушы материалды дайындау. Бидайлы-картопты крахмалды қанттандыру үшін сұлы қоспасы (50%), арпа (25%) немесе уыт (25%) қолданылады. Арпа және уыт 30% мөлшерде болу керектігін ескерген жөн. Уыттың негізінде екі қоспасын қолдану мүмкіндігі бар: сұлы және арпа немесе арпамен уыттың өзін алады, егер бұл қоспалар дайын болмаған жағдайда уытты қолдануға болады.
Бидай және картоп крахмалының массасын қанағаттандыратын беттік культуралар құрайды. Бұл культурада аз ғана мөлшерде а- амилаза бар болады. Ашу процесінің ұзақтығы 72 сағат ашуда а- амилаза шығыны болады. Ашыту чанына ашытқыларды қанттандырғыш аппараттан береді. Мұнда ашытылған сусла көлеміндегі ашытқы шығыны 6-8% құрайды. Ашуы жетілген ашытқыны айдағанға дейінгі ашу процесінің ұзақтығы 72 сағатты құрайды.Ашуы жетілген ашытпадан ректификациялық бағаналар арқылы спирт алынады. Этил спирті түссіз, жеңіл сұйықтық, оның өзіне тән иісі және дәмі болады.
Еріткіштердің биотехнолгиялық өндірісі
Органикалық еріткіштер – ацетон және бутанол тек химия өндірісінде ғана емес бір қатар өндіріс салаларының халық шаруашылығында кеңінен қолданылады.
Ацетон-бутилдің ашу процесі анаэробты болып келеді және Clostridium acetobutylincum бактериясын немесе соған жақын май қышқылы тәрізді бактериясын тудырады оны ацетон және бутанолды өндірістік масштабта алуға қолданады. Химиялық синтездеу жолмен алған микробиологиялық синтездеу жолымен алғаннан екі есе күрделі. Клостридиннің көмегімен 30 жылы академик В.Н.Шапошников алғаш рет ТМД-да ацетонды және ацетон – бутанолды микробиологиялық синтездеу жолымен алуды ұйымдастырған. Ацетонды және бутил спиртін дәннің және мелассаның ашумен алған. Сульфидті сілтіден және ағаш гидролизатыннан ацетонды және бутил спиртін алу әдісін өңдеді.
Ацетон-бутилдің ашу процесі. Май қышқылының ашу процесі кезінде онда бутил спиртінің, ацетонның, аз мөлшерде этил спиртінің болатынын Л. Пастер 1861 жылы анықтаған болатын. Міне, ашудың осындай түрін ацетон-бутилдің ашу процесі деп атаған. Бұл процесте ацетон, бутил спиртінен басқа май қышқылы, сірке қышқылы, сутегі және көмір қышқыл газы пайда болады. Бұл реакцияның жалпы бағыты мына төмендегідей:
12С6Н1206 = СН3СН2СН2СН2ОН + 4СН3СОСНз +
бутил спирті ацетон
+ СН3СН2ОН + СН3СН2СН2СООН + 18Н2 + 2Н20 + энергия
этил спирті май қышқылы
Белгіленген атомдарды қолдана отырып зерттегенде, сірке қышқылының белгіленген атомын қолданғанда, оның 50 % бутил спиртінен, 15% ацетоннан, 10% көмір қышқыл газынан табылған. Ал май қышқылының белгіленген атомдарының 85% бутил спиртінен табылғаны анықталды. Міне, бұл зерттеулерден бутил спиртінің түзілуі үшін аралық өнім май қышқылы деген қортынды шығаруға болады. Сонымен қатар ацетонда сірке қышқылының қатысуымен түзіледі.
Ацетон-бутилдің ашу процесінде екі кезең бар екені байқалады. Біріншісі — қышқылдық кезең. Мұнда бактериялар көбейіп, ортада май және сірке қышқылдары түзіледі. Ал екінші кезең — ацетон-бутил кезеңінде орта қышқылдылығы азайып, ацетон-бутил және этил спиртінің түзілуі күшейеді. Сонда ацетон-этил ашу процесінің май қышқылының ашу процесінен айырмашылығы болады. Май қышқылының ашу процесінде ортада жиналған қышқыл, одан әрі қышқылдың жиналуын тежейді, тіпті кейде тоқтайды. Ал ацетон-бутилдің ашу процесінде пайда болған қышқылдарды басқа бактериялар қолданып, одан басқа заттар түзеді.
Бұл процесс Клостридиум ацетонбутиликум микроорганизмінің көмегімен жүреді. Оның қозғалғыш мөлшері 3,5 — 5 мкм болатын, таяқша, анаэробты, спора түзетін, клеткалары қосақтала немесе тізбектеле орналасқан бактериялар. Олар дайын аминқышқылдары мен витаминдерді қажет етеді.
Қазіргі кезде өндірісте ацетон-бутил процесіне жүгері ұны немесе басқа да крахмалға бай шикізаттарды қолдана отырып, ацетон және бутил спиртін алады. Ацетон халық шаруашылығының кеңінен саласында қолданылады. Ал бутил спирті автомобиль, самолет, ағаштан үй жиһаздарын жасауда қолданылады. Ацетон-бутилдің ашу процесі барысында түзілетін газдан метил спиртін (СН3ОН) жасайды.
Сүт қышқылы бактериялары ацетон-бутилдің ашу процестеріне көп зиянын тигізеді. Олар ортада сүт қышқылын түзіп, ацетон-бутилдің ашу процесін тежейді. Сондықтан ацетон-бутилдің ашу процесінде микробиологиялық бақылау жасалуы керек.
Органикалық заттардың трансформациясы
Микробтық трансформация – микроорганизм ферментінің әсерінен органикалық қосылыстың толық емес өзгеруі осы өзгергеннен ортада өнімнің жиналғанын тудырады.
Микроорганизмді қолданудың синтетикалық аумағын шартты екі бағытқа бөлуге болады.
- биологиялық активтік заттың және өнімнің микроорганизммен толық биосинтезі (антибиотик, фермент, витамин, стерин, аминқышқылы және т.б.), қоректік орта компонентінің көмегімен іске асырылатын:
-микробиологиялық трансформация, демек халық шаруашылығының өніміне арналған дәрілік препараттың көп сатылы синтезінде микробиологиялық сатыны және жеке химиялық сатыны бірлесе қолдануды айтады.
Активті полифенол жүйесінде тасымалдағыш ретінде микроорганизмді қолдану, әртүрлі қажет өнімге және физиологиялық активті затқа экзогенді органикалық қосылысты ауыстыруға синтез кезінде 20 химиялық сатыны қажет ететін, бір сатыда маңызды өзгеріске ұшырауын олар іске асыратыны негізделген. Одан басқа да қиын және химиялық әдіспен іске асырылмайтын реакцияның жүруін оңайлатады, соңғы он жылдықта химиялық реакцияға қарағанда микробиологиялық өзгеріске ұшырау әдісінің артықшылығы анық көрсетілді; күрделі молекулалық қайта өңдеу мүмкіндігі, технологиялық процестің экономикалық жағынан тиімділігі және қолайлығы. Бұл әдістердің артықшылығы стероидтар химиясының аумағында анық көрінді. Стероидтың молекуласының көлемділігі және күрделілігі олардың химиялық жолмен аз ғана модификациясы қиындатады. Микроорганизмдер дәрілік препараттардың синтезінде ерекше реакция іске асырады, ол 1,2- дегидрирлеу, 11 β- гидроксилирлеу. Өндірістік синтез мынадай күшті дәрілерде, гидрокортизон, преднизон, преднизолон, дексаметазон сияқтыларды микробиологиялық әдіспен өңдегеннен соң оларды алу мүмкіндігі бар. Бұл препараттар ауыр аурулармен ревматиз, бронхиальды астма, суықтаған процестерге және созылмалы тері ауруымен ауыратынды емдеуде кеңінен қолданылады. Соңғы жылдары органикалық заттардың құрылысы қарапайым микробиологиялық өзгергенін бірқатар зерттеушілер көрсетті, сонымен қатар іс жүзінде қызығушылық көрсетті. Органикалық қосылыстардың негізгі класына арналған микробтық және типтік ферменттік өзгеруі көрсетілген.Микробиологиялық трансформацияның көптеген процестері субстраттың бір немесе бірнеше іске асырылатын молекуласының шамалы өзгеруіне әкеледі. Бірақ та тасымалдаушы қосылыстардың құрылысын әжептеуір өзгертетін микробиологиялық процестер бар. Микробиологиялық трансформацияның барлық процесі болып тасымалдаушы de novo молекуласының синтезі емес заттың молекулярлық құрылысының өзгеруі оның қорытындысы болып саналады. Микробиологиялық трансформацияға сонымен қатар предшественниктен метаболизм синтезі жатады, егерде мұндай кезде реакция өнімінің құрылысы анықталса, негізінде предшественниктің (мысалы, гетероциклді негізден, пентоздан кейбір нуклеид синтезінен) молекуласының негізі. Қазіргі кезде микробтың трансформация процесінің келесі типтерін бөліп алады: тотықтыру, тотықсыздандыру, декарбоксилирлеу, дезаминирлеу, глюкозидтің түзілуін, гидролиз, метилирлеу, этерификация, дегидратация. Өндірістік процесте тотығу реакциясы кеңінен қолданады және тереңірек меңгерген. Олар гидроксилдеуді активтелмеген көміртегімен біріктіреді, шексіз байланыстың тотығуы, ароматты сақинаны гидроксилдеу, дегидрирлеу май қышқылының β тотығуы мысалға, мынадай реакция суықтаған ауруға қолдануға алынған преднизонның стероидты препараты, преднизалон және оның туындысы стероидты дегидрлеу болып саналады:
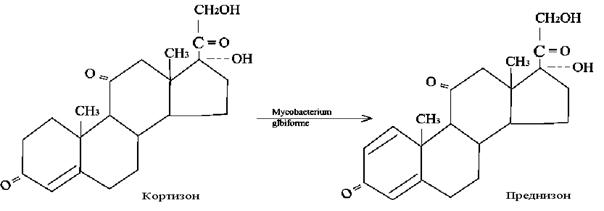
Микробтық тотықсыздану осындай түрдегі көптеген химиялық реакцияның алдындағы артықшылығы болып табылады. Мысалы микробтық ферменттің әсерін селективтілігі стероидтың белгілі кето-тобының тотықсыздануына мүмкіндік жасайды (химиялық жолмен бұл болмайды). Белгілі мысалдар ферментативті декарбоксилдеу негізінде кето қышқылы және аминқышқылының декарбоксилдеуіне жатады.

Аспаралиновая кислота β –Аланин
Микробтық процесс химиялықпен салыстырғанда «жайлы» жағдайда өнімнің жақсы шығыммен жүреді.Микробтық дезаминирлеу аминқышқылының пурин және пиримидин негізінде және нуклеотидтің өзгеруі үшін жоғарғы мәнге ие, мысалы:
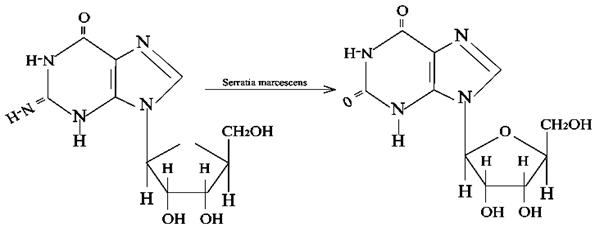
Гуанозин Ксантозин
Гидролиз реакциясы микробтық химияда барынша кең таралған. Олар эфирдің, амидтің және басқа да қосылыстың гидролизін қосады. Көптеген бұл реакция стероид өндірісінде және антибиотик өндірісінде қолданылады. Пенициллиннің қазіргі заманғы өндірісі 6-аминпеницил қышқылының әртүрлі туындысының синтез негізінде (6- АПК) Бензилпенициллиннен ферментативті гидролизбен қышқылды алады:
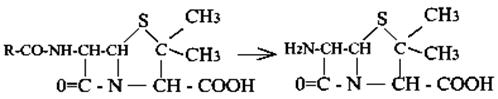
Бензилпенициллин 6-Аминопенициллин қышқылы
Конденсация реакциясы - әртүрлі микробтық ферменттің көмегімен екеу немесе одан да көп фрагменттен органикалық заттың молекулалық синтезі. Реакция жаңа антибиотик – пенициллин және цефалоспорин туындысын алуда кеңінен қолданылады:
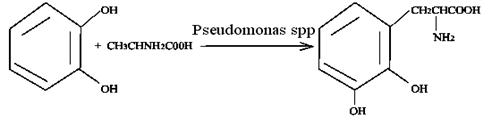
Пирокатехин L- аланин L-диоксифенилаланин
Изомеризация реакциясының іс жүзінде жоғарғы мәні бар. Оған қолданылғаны негізделген, мысалы, фруктозаны глюкозадан алған сияқты маңызды өнеркәсіптік процесс саналады.
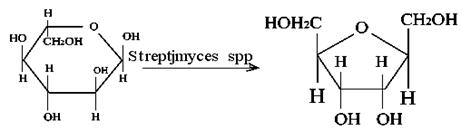
Глюкоза Фруктоза
Тест сұрақтар
1.Кальций цитратын ыдырату-бұл өндірістің сатысының бірі:
А) лимон қышқылы;
Б) сүт қышқылы;
В) сірке қышқылы;
Д) лизин;
Е)глутамин қышқылы;
2. Органикалық еріткіштерді тұндыруда тұндырғыш болып саналады:
А) ацетон, этил спирті;
В) күкірт қышқылы;
С) тұз қышқылы;
Д) бензол, метан;
Е) фосфор қышқылы;
ІҮ МОДУЛЬ. МИКРОБИОЛОГИЯЛЫҚ СИНТЕЗ ӨНІМДЕРІН АЛУ
10-сабақ. Амин қышқылы өндірісі
Сабақ жүргізу формасы: Проблемалы
Проблема: Амин қышқылы продуценттері қандай
талаптарға жауап береді, оларды қандай мақсатта алады.
Жоспары:
1 Аминқышқылы өндірісі
2 Лизин және триптафан алу
3 Глутамин қышқылы өндірісі
Аминқышқылы өндірісі
Аминқышқылы – бір немесе бірнеше аминқышқылдарынан тұратын карбонды қышқылдар, олар табиғатта кең таралған.Олар табиғи ақуыздардың құрылымдық элементі болып табылады. Аминқышқылдарының жалпы формуласы RCH (NH2) COOH (пролин мен оксипролиннен басқа).
Ақуыз құрамына кіретін 20 аминқышқылдарының сегізі адам мен жануардың организмінде синтезделе алмайды, сондықтан оларды алмастырылмайтын аминқышқылдары деп аталады. Оған фенилаланин, изолейцин, лейцин, лизин, метионин, треонин, триптофан және валин кіреді. Адам және жануарлар организміндегі зат алмасу процесі тек алмастырылмайтын аминқышқылдарының жеткілікті мөлшерде және белгілі бір ара қатынаста болғанда ғана жүреді. Алмастырылмайтын аминқышқылдарының біреуінің жетіспеуі организміндегі зат алмасу процесінің күрделі бұзылуына әкеліп соқтырады, сөйтіп организміның өсуі мен дамуы баяулайды.
Тағамның құндылығын жоғарылату үшін тағам өнімдерін алмастырылмайтын аминқышқылдармен байыту қажет. Жануарлар рационына 10 % мөлшерінде жетіспейтін аминқышқылдарын енгізсе азықтық ақуыздың бағалылығы 2 есеге жоғарылайды. Қазіргі уақытта азықты байытуға көптеген елдерде лизинді кеңінен қолданады.
Ауылшаруашылығынан басқа аминқышқылдарын ең басты тамақ өнеркәсібі қажет етеді. Аминқышқылдары азықтық өсімдік өнімдерінің қоректік бағалылығын жоғарылататын байытушы ретінде қолданылуы мүмкін, сонымен қатар приправа ретінде қолданылуы мүмкін, өйткені ол белгілі бір дәмдік қасиеттерге ие және өнімге белгілі бір аромат пен дәм бере алады. Аминқышқылдары және оның өнімдері беттік активті заттар мен полимерлер синтезінде, маторлық жылытқыштарға қосымша ретінде, электрохимияда, медицинада және т.б.жерлерде қолданылуы мүмкін.
Аминқышқылдарының мәні мен перспективтілігіне қарамастан, өндірістің көптеген салалары оларды кеңінен қолданылуын көлемі кіші өндіріс екенімен және бағасы жоғары болуымен шектеледі.
Қазіргі уақытта аминқышқылдарын алудың 3 әдісі бар: табиғи ақуыз гидролизаттарынан бөліп алу, химиялық синтез және микробиологиялық синтез жолымен бөліп алуға болады.
Табиғи ақуыз гидролизін қышқылмен, сілтімен немесе ферменттің көмегімен жүргізуге болады. Бірақ бастапқы шикізатты (ет өндірісінің қалдықтары, жұмыртқа ақуызы, сүт казейні және т.б.) қымбаттылығы мен тапшылығы, сонымен қатар аминқышқылдарының бөлінуі мен тазалануының қиындығы – бұл әдісті кеңінен қолдануға мүмкіндік бермейді.
Аминқышқылдарының химиялық синтезіне D және L формасының рацемикалық қоспасы түзіледі, оны бөлу өте қиын. Биологиялық активті L және D-аминқышқылдары адам және жануарлардың ағзасында сіңірілмейді. Синтетикалық аминқышқылдарының және оның өнімдерінің халық шаруашылығының әртүрлі салаларында кеңінен қолданылуы аминқышқылдарының синтезі мен экономикалық жағынан тиімді технологиясын құрғанда ғана, оның рацемикалық қоспасын бөлу мүмкін.
Аминқышқылдарын микроорганизмдердің көмегімен алу әдісі біздің жүз жылдықтың 60-шы жылдары пайда болды. Қазір аминқышқылдарын продуцирлеуге қабілетті микроорганизмдердің жүзден астам түрлері мен штаммдары алынған және селекционирленген. Бұл әдістің үлкен жетістігі – аминқышқылдарын биологиялық активті L –формада түзілуі оның бөлінуі мен тазалануын едәуір жеңілдетуі болып табылады.
Аминқышқылдарының микробиологиялық синтезінде ауксотрофты мутанттарды қолданады, яғни мутагендік факторлардың әсерінен (сәулелену, химиялық әсер және тағы басқалар) аминқышқылының өсуі мен дамуына керекті қандайда бір қажеттілікті өздігінен синтездеу қабілетіне жұмсайтын бактериялар мысалы, гомосерин, бірақ олар басқа аминқышқылының жоғары синтезі қабілетіне ие болады.
Мұндай бактериялардың өсуі мен көбеюі үшін қоректік ортада белгілі аминқышқылдарының құрамы болуы тиіс: гомосерин, треонин, метионин және тағы басқалар. Көп жағдайда мутанттарға биотин қажет. Мұндай бактериялар гомосериндефицит деп аталады. Табиғатта кездесетін кейбір бактериялар өсу процесінде, ортада 2-5 г/л дейін бос аминқышқылдарын жинауға қабілетті, ал ауксотрофты мутанттар оны 20-100 г/л дейінгі үлкен мөлшерде продуцирлей алады.
Аминқышқылдарының микробиологиялық синтезі көптеген елдерде меңгерілген. Өндірістік масштабта L- лизин алынады, басқа аминқышқылдарын алуға арналған зерттеулер кеңінен жүріп жатыр. Аминқышқылының ферментативті синтез реакциясы клетка ішінде жүреді.
4 кесте- Экспоненциальды фазасының ортасында жүріп, соңында максимум мәнге жетеді.
| Аминқышқылы | Өндіру тәсілі | Өндіру көлемі т/г |
| Аланин Аргинин Аспарагин қышқылы Аспарагин Цитруллин Цистеин Цистин Глицин Глутамин қышқылы Гистидин Гомосерин Оксипролин Глутамин Изолейцин Лейцин Лизин Метионин L-Метионин Орнитин Фенилаланин Пролин Серин L-Треонин D L-,L-триптофин Тирозин Валин ДОФА | Ф,х М,Х,Г Ф Х,Г М,Х Г Г Х М М,Г М Г М М,Г М,Г М Х М М,Г М,Х М,Г М,Г М Х,Ф М,Г М Ф | 150-200 100-300 10-50 10-50 1-10 100-200 5000-6000 100 000 100-200 10-50 10-50 200-300 10-50 50-100 60 000-70 000 100-200 10-50 50-100 10-50 10-50 50-100 10-100 50-100 0,1 |
Белгіленуі: Ф-ферментативтік синтез, Х-химиялық синтез,
М-микробиологиялық синтез, Г-жануар және өсімдік шикізатының ақуыз гидролизатынан экстракция жолымен алу. ДОФА-3,4 -диоксифенилаланин
Алғашында аминқышқылы клетка ішінде бос аминқышқылдары түрінде жиналды. Культивирлеудің алдынғы сатыларына кіретін периодты культивирлеуде аминқышқылының активті жиналуы және оның өсуі.
Лизин алу өндірісі
Лизин (a,e - диаминокапрон қышқылы) С6Н14N2O2
 NH2
NH2
 NH2-CH2-CH2-CH2-CH2 - CH
NH2-CH2-CH2-CH2-CH2 - CH
COOH
Екі оптикалық активті D және L- формасы белгілі. Адам және жануарлар организмінде лизин бірқатар маңызды биохимиялық функцияларды орындайды. Жасушадағы кальцийдің тасымалдануына және асқорыту ферментерінің секрециясына қатысады, жалпы азоттық балансты жақсартады және тағы басқада жануарлар азығында лизин ең дефицит аминқышқылы болып табылады. Лизиннің микроорганизм-продуценті гомосериндефицит мутанттар ауксотрофты бактериялар Brevibacterium, Micrococcus, Corynebacterium және тағы басқа тұқымдары жатады. Елімізде лизин продуценті ретінде Brevibacterium тұқымының бактериялары қолданылады.Лизин продуценті-ауксотрофты болғандықтан, биотин, тиамин, треонин және метионинді қажет етеді. Лизин және басқа да аминқышқылдарын өндірісте алғанда қатал асептикалық жағдайларды және қоректік орталардың залалсыздығын қатаң қадағалауы қажет. Сонымен қатар, таза культураның продуценті қолданылады.
Лизин алудың технологиялық процесі келесідей сатылардан тұрады:
1.егіс материалын алу;
2.қоректік ортаны залалсыздау және дайындалу;
3.барлық аппаратура мен коммуникация үшін ауаны залалсыздау
дайындау;
4.ферментация;
5.дайын өнім – L- лизинді бөліп алу;
Егіс материалын алу. Лизин шығаратын биохимиялық зауыттарда егілетін культураны дайындау периодты әдіспен жүргізіледі. Бастапқы культураны ет пептонды агар – агарда қатты қоректік ортасы бар пробиркаға егеді және тәулік бойы 29-30°С температурада өсіреді. Өскен культурадан микроорганизмдер суспензиясын алады. Оны аналық егіс материалы дайындалған колбаға залалсыздалған сұйық қоректік ортаға енгізеді де, тәулік бойы тербелмелі шайқағышта (180-200 айн/мин) 29-30°С температурада өсіреді. Аналық егіс материалы дайындалған колбадан алынған культураны егіс материалына арналған колбаларына қоректік ортаның көлемін 5% есеппен бір тәуліктік аналық культураны егеді. Егіс материалына арналған колбалардағы культураны да шайқағышта тәулік бойы 30°С температурада өсіреді. Содан соң егіс материалын колбалардан инокуляторға ауыстырады. Инокуляторда культураны 29-30°С-температурада тәулік бойы аэрациялау және араластырумен өсіреді.
Көбінесе егіс материалын алу үшін меласса (3-5%), жүгері экстракты 2,5-3% және ас тұзы бар қоректік орталар қолданылады. рН - 7-7,2 мәнін 20%-тік күйдіргіш натрий ерітіндісімен тұрақтандырады. Инокулятордағы культураның құрамы ферментациялық қоректік ортаға біршама жақын болуы керек.
Қоректік ортаны залалсыздау және дайындау. Лизин продуцентін өсіруге арналған қоректік орта залалсыздаумен дайындалады немесе басқада өсіретін заттар бар, культураның өсу көзі ретінде қоректік ортада мелассадан тұратын, жүгері экстракты немесе басқа өсуге арналған зат бор қолданылады. Көміртегінің негізгі көзі ретінде – меласса құрамында термолабильдік компонент сахароза болады, сондықтан оны жеке бөлек залалсыздайды. Мелассаны реакторға салып, араластырып тұрып, 80°С температураға дейін қыздырады да, қантты қажет концентрацияға дейін сумен араластырады.Алынған меласса ерітіндісін 120-122°С температураға дейін арнаулы аппаратта бумен тез қыздырып және осы температурада белгілі бір уақытқа дейін ұстайды. Лизин продуцентін өсіру үшін меласса, жүгері экстракты құрамы қолданылады.
Қалған компоненттерді араластырып, қыздырып тұратын және араластырғышы бар реакторда ерітеді, содан соң залалсыздау температурасына дейін арнаулы аппаратта қыздырады да белгілі бір уақытқа дейін ұстап суытады.
Көбік сөндіргіш көбінесе бөлек залалсызданады, бірақ басқа қоректік орта қатаң режимде залалсызданады. Ауаны залалсыздаудың сызба нұсқасы бойынша залалсыздау режимінде орындайды. Аппаратура мен коммуникация өткір бумен қысымда, 135-140°С температурада залалсызданады. “Мұздай” залалсыздау әдісін де қолдануға болады, онда бактерицидтік газ (этилен) және химиялық реагент ерітінділері (формалин, хлорлы қосылыстар және т.б.) қолданылады. Мұздай залалсыздаудан соң химиялық реагенттердің қалдықтарын залалсызданған сумен жуады.
Ферментация. Лизин продуцентін өндірісте культивирлеу процесі көлемі 50 және 100м3 болатын ферментерде периодтық әдіспен жүргізіледі. Ферментер залалсызданған қоректік ортамен толтырылады.
Ферментерге қоректік ортаның көлемінен 5-6% мөлшерде егіс материалы залалсызданған тізбегі бойынша келіп түседі. Ферментерді толтыру коэфиценті 0,75 құрайды. Егілгеннен кейін, тез арада ферментерге залалсызданған ауа беріледі. Ауа 50°С температураға дейін қыздырлады және есеп бойынша бір көлемде ауа, бір көлемде қоректік орта бір минутта 0,12-0,13 МПа қысымда беріледі.
Ферментация процесі 48-72 сағат бойы араластыру және аэрациялау процесі бойынша 29-30°С температурада жүргізеді. Периодты түрде көбік сөндіргіш беріледі, ал қоректік ортаға рН-тың мәні қалыпты болуы үшін белгілі бір уақыт аралығында 25% аммиакты немесе 15% күйдіргіш натрий ерітіндісін қосып отырады. Ферментация процесі 58-72 сағаттан кейін аяқталады, сосын культуральды сұйықтықты дайын өнімді бөліп алуға жібереді.
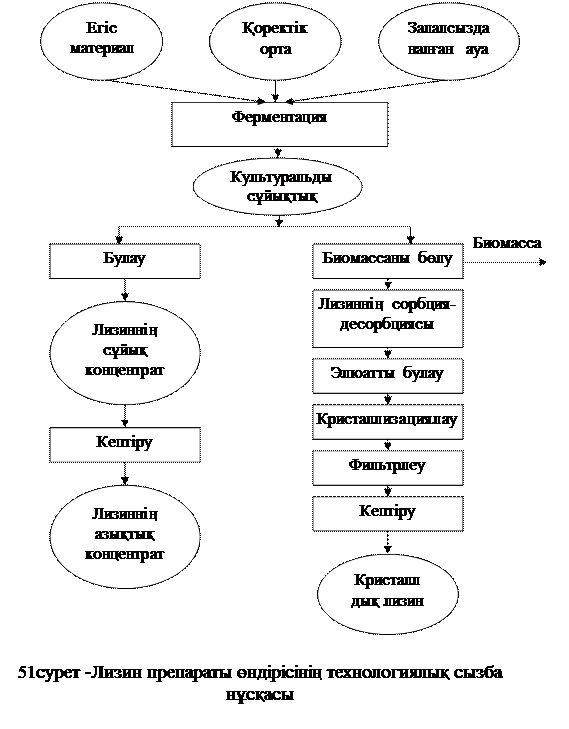
Дайын өнім L-лизиннің бөлінуі. Культуральды сұйықтықтан қолданылуына қарай әр түрлі микробиологиялық препараттарды алуға болады: лизиннің сұйық концентраты (ЖКЛ), лизиннің құрғақ азықтық концентраты (ККЛ), кристалды лизин. Әрбір препарат белгілі бір технологиямен алынады.
Суретте барлық үш препараттың алынуының технологиялық сызба нұсқасы көрсетілген: ЖКЛ, ККЛ, және кристаллды лизин.
 |
Микробиологиялық концентрат ЖКЛ және ККЛ алу үшін құрамында 10-13% құрғақ затты құрайтын культуральды сұйықтықты рН 5,0 болғанша, тұз қышқылымен қышқылдайды да, лизиннің тұрақты болуы үшін 0,15% бисульфат натрий ерітіндісін қосады. Содан соң тұрақты культуральды сұйықтықтағы құрғақ заттың концентрациясы 35-40% дейін вакуум- буландырғышта булайды. Алынған лизиннің сұйық концентратын мал азығының құнарлылығын арттыру үшін қосуға болады.
Құрғақ концентратты ККЛ алу үшін сұйық концентратты кептіргіште ылғалдығы 5-6% болғанға дейін ұстайды. Құрғақ (ККЛ) өте гигроскопиялық болып келеді, сондықтан кептірілгеннен соң тез арада оны полиэтилен қапшықтарға қаптайды. Гигроскопиялығы төменді және үгілгіш ККЛ алу, ЖКЛ толықтырғыш пен сүйектің ұнымен, азықтық ашытқымен бидай кебегімен бірге кептіреді.
Кристалдық лизинді культуральды сұйықтықтан ион алмасу әдісі арқылы бөліп алады. Культуральды сұйықтықтан биомассаны фильтрлеу арқылы және центрифугирлау арқылы бөліп алады.
Лизинді маркасы КУ-2 немесе КБ-4П-2 ион алмасу шайырында фильтраттан сорбциялаумен бөліп алады. Ион алмасу бағанасын сумен жуғаннан соң лизинді 0,5-5,0 % аммиакты сумен элюирлейді.
Құрамында 1-2% лизині бар элюатты рН 4,9-5,0-ге дейін жеткенше тұз қышқылымен қышқылдандырады және лизин концентрациясын 30-50%-ке жеткенше вакуум-буландырғыш қондырғыда булайды. Лизин тұз қышқылының әсерінен лизиннің монохлоргидраты пайда болады, ол 10-12°С температураға дейін салқындағанда сарғыш кристалдар түрінде түседі. Лизиннің монохлоргидратын аналық ерітіндіден фильтрлеу арқылы бөліп алады және этил спиртімен жуылып, кептіріледі. Мұндай лизин мал шаруашылығында мал азығы ретінде қолданылады.
Жоғары тазаланған лизинді алу мақсаты монохлоргидрат лизин кристалдарын бояғыш заттардан және қоспадан көп сатылы тазалаумен және этил спиртін кристализациялаумен алынады.
Тазартылған лизинді көбінесе тамақ өнеркәсібінде, медицинада және тағы басқа мақсаттарға қолданады. Кристалды лизинді картон қораптарға салып буып қаптайды.
Глутамин қышқылы өндірісі
Глутамин (α- аминоглутар) қышқылы
HOOC-CH2-CH2-CH-COOH
׀
NH2
Алмастырылмайтын аминқышқылға жатпайды, бірақ өсімдік және жануар ақуыздарының ең маңызды амин қышқылы болып табылады. Соның негізінде адам организмінің қалыпты өмір сүруіне қажет, көптеген физиологиялық активті қосылыстар синтезделеді.
Глутамин қышқылы бауыр және бүйректің әртүрлі уланулардан қорғаныш фактор қызметін атқарады, дәрі-дәрмектердің фармакологиялық әрекетін күшейтеді, әртүрлі заттардың токсиндік әрекетін төмендетеді. Глутамин қышқылының мононатрий тұзы глутамат натрий одан да кеңірек қолданылуда. Бұл қосылыс тағам өнімдерінің дәмін күшейтеді, сонымен қатар консервіленген өнімдердің дәмінің сапасының ұзақ сақталуына мүмкіндік жасайды. Көптеген елдерде натрий глутаматы жемістерді, балықтарды, ет өнімдерін консервілеуде кеңінен қолданылады.
Глутамин қышқылы өндірісінің ең кеңінен және перспективті әдісі микробиологиялық синтез болып табылады.
Глутамин қышқылын продуцирлейтін белгілі микроорганизмдердің ішінде Micrococcus, Brevibacterium және тағы басқада бактериялардың маңызы зор.Бұл ұсақ, грамм оң, дөңгелек немесе сопақша тәрізді бактериялар,олардың арнайы ерекшелігі биотин мен тиаминді тұтынуы болып табылады.
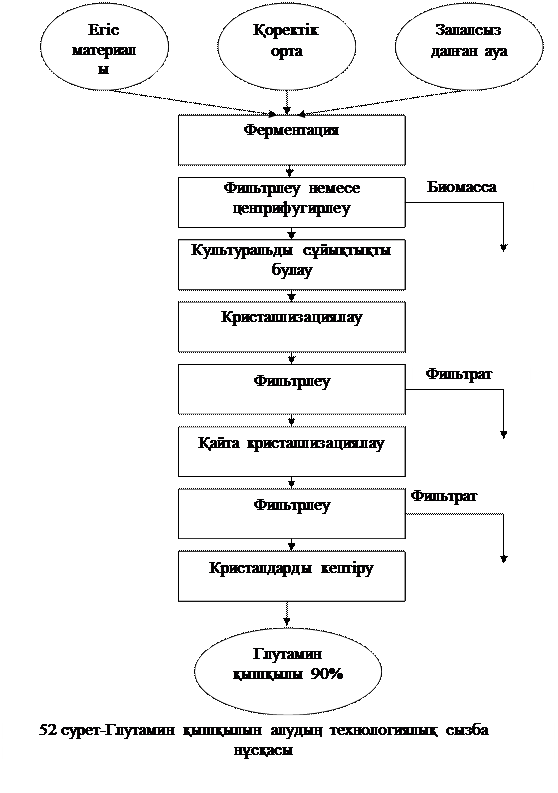 |
Глутамин қышқылы өндірісінің технологиялық процесі лизин өндірісінің процесі сияқты ұқсас. Ол келесі сатылардан тұрады (сызба-нұсқа):
1.егіс материалын алу;
2.қоректік ортаны дайындау және залалсыздандыру;
3.ферментация;
4.дайын өнімді кристалл түрінде бөліп алу;
5.кептіру, буып түю.
Глутамин қышқылын алу үшін көміртегі көзі ретінде көбінесе глюкозаны, сахарозаны, крахмал гидролизатын, мелассаны, гидролды қолданады. Көмірсулардан басқа шикізат ретінде көмірсутектер (метан, этан, мұнайдың н-парафині), сонымен қатар сірке, фумар қышқылдары және бірқатар өнімдер қолданылады.
Қоректік ортаға азот көзі ретінде 1,5-2,0% мочевина қолданылады, бірақ оны ортадағы мочевина құрамы 0,8%-ке дейін қажет мөлшерде ғана бөліп қосады. Кейбір жағдайларда мочевинаға азот көзін толықтырғыш ретінде (NH4)2 SO4 аммоний сульфаты, NH4Cl аммоний хлоридін 0,5% мөлшерде немесе аммиактың сулы ерітіндісін қолданады.
Культураның қалыпты өсуі үшін ортаға 10 немесе 100 % калий (KH2PO4- түрінде), магний (Mg SO4 ·7H2O), марганец (Mn SO4 ·4H2O), сонымен қатар ортаның рН мәнін ұстап тұру үшін бор қосады.
Глутамин қышқылының биосинтезіне биотин, тиамин, кейбір антибиотиктер (пенициллин, тетрациклин) спирттер және БАЗ (беттік активтік заттар) тұрақтандыру үшін қосады. Бірақ та биостимулятор концентрациясын қатаң бақылап отыру керек, өйткені жоғарғы концентрацияда мысалы, биотин биомассасының өсуін күшейтеді, бірақ глутамин қышқылының шығымын төмендетеді.
Зертханада егіс материалын алу тізбегімен жүргізеді: микроорганизм продуцентін пробиркада, одан кейін тербеткіште колбада, содан соң көлемі 2 және 5м3 көлемдегі егіс ферментерлерде іске асырады. Культивирлеу процесі температурасы 28-300 С температурада, рН ортасы 6,8-7,5, әр сатыдағы культивирлеу сатысының ұзақтығы 24 сағат болады.
Ферментация процесін көлемі 50м3 ферментерде қарқынды аэрациялаумен және 28-300 С температурада жүргізеді. Культивирлеу процесі 2-3 тәуліке созылады. Осы уақыт ішінде ортада 50г/л глутамин қышқылы жиналады.
Культуральды сұйықтықтан биомассаны бөліп алу, фильтрлеумен және центрифугирлеумен жүргізіледі, ал культуральды сұйықтықты вакуум –буландырғыш қондырғыда буландырумен іске асырылады. Кристаллизациядан кейін глутамин қышқылын бөліп алады. Тазалығы жөғары өнімді алу үшін қайта кристаллизациялау жүргізіледі.
КУ-2 шайырда сорбцияда культуральды сұйықтықтан глутамин қышқылын бөліп алу ион алмасу әдісімен орындалады. Глутамин қышқылы шайырда сорбирленгеннен кейін, бағанада жуылғаннан кейін 0,5-5,0% аммиакты сумен элюирлейді. Алынған элюатты активтелген көмірмен өңдейді және көлемі 3-5 есеге дейін төмендегенше 400С температурада вакууммен концентрлейді.
Тұз қышқылымен рН мәнін 3,2 дейін қышқылдағаннан кейін ерітіндіні 40С температураға дейін салқындатады, сол кезде глутамин қышқылы кристаллизацияланады. Қайта кристаллизацияланғаннан кейін негізгі зат (глутамин қышқылы) 99,6 % өнімін құрайды.
Натрий глутаматын алу. Натрий глутаматын техникалық глутамин қышқылынан алады HOOC-CH2-CH2CH (NH2) -COONа.
Қышқыл кристаллын суда ерітеді, сулы ерітіндіні активтелген көмірмен толығымен түссізденгенше 60-700С температурада өңдейді. Содан соң глутамин қышқылын 45-50% NaОН ерітіндісімен бейтараптайды, рН м|
 2015-02-18
2015-02-18 11336
11336








