Определить сколько кг динитротолуола сгорело в герметичном объеме 100м3, если содержание кислорода в продуктах сгорания составило 12%.
Решение: Так как в продуктах горения содержится кислород, то горение протекало в избытке воздуха, коэффициент избытка которого определим по формуле (1.10). Для этого запишем уравнение горения:
С7Н6(NO2)2+6,5O2+6,5∙3,76N2=7CO2+3H2O+N2+6,5∙3,76N2
Молекулярная масса горючего-182.Теоретический объем воздуха равен:
V0B= 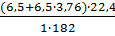 =3,8 м3/кг
=3,8 м3/кг
Теоретический объем продуктов горения (формула1.14):
V0пr= 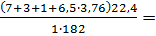 4,4 м3/кг
4,4 м3/кг
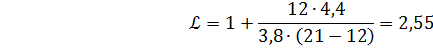
Практический объем воздуха, пошедший на горение:
VB= 2,55 ∙3.8=9,7 м3/кг
Тогда массу сгоревшего динитротолуола Р определим из соотношения:
Рr = 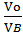 , Рr =
, Рr = 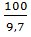 =10,3 кг
=10,3 кг
 2015-03-22
2015-03-22 1709
1709








