Статистика показывает, что большая часть пожаров от самовозгорания обусловлено самовозгоранием промасленных волокнистых и сыпучих материалов. В промышленности и в быту применяется огромное количество жиров и масел, которые по своему происхождению можно подразделить на природные, искусственные и синтетические.
Природные масла - добываются из тканей наземных, морских животных и рыб (животный жир), из семян и мякоти плодов различных растений (растительные масла). К ним же относятся некоторые продукты их переработки. Например, олифа.
Искусственные масла - получают из нефти (это минеральные масла) или из смолы полукоксования каменных углей (каменноугольные масла).
Синтетические масла - получают полимеризацией и поликонденсацией низших алкенов, гликолей и их эфиров, силоксанов и других мономеров.
Все они по применению подразделяются на пищевые, технические, (производство высыхающих пленкообразующих для лаков и красок, ПАВ, глицерина, жирных кислот и другие), смазочные (моторные, индустриальные, трансмиссионные и другие) и промышленные (электроизоляционные, гидравлические, шпалопропиточные и т.д.) масла.
Большинство из них имеют температуру вспышки в пределах 170-350 °С, температуру самовоспламенения 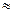 300 °С, поэтому относительно пожаробезопасны. В чистом виде жиры и масла не склонны к самовозгоранию. Но при попадании на волокнистые, пористые и сыпучие вещества и материалы с большой удельной поверхностью многие из них приобретают исключительно высокую способность к окислению кислородом воздуха даже без нагревания. К ним относятся растительные высыхающие масла, подвергавшиеся нагреву минеральные, например, моторные, цилиндровые, закалочные масла и т.п. Рассмотрим их поведение на примере природных жиров и масел.
300 °С, поэтому относительно пожаробезопасны. В чистом виде жиры и масла не склонны к самовозгоранию. Но при попадании на волокнистые, пористые и сыпучие вещества и материалы с большой удельной поверхностью многие из них приобретают исключительно высокую способность к окислению кислородом воздуха даже без нагревания. К ним относятся растительные высыхающие масла, подвергавшиеся нагреву минеральные, например, моторные, цилиндровые, закалочные масла и т.п. Рассмотрим их поведение на примере природных жиров и масел.
Растительные масла (льняное, конопляное, хлопковое, подсолнечное другие), а также животные жиры (тресковый, тюлений, китовый, бараний,
говяжий и т.д.) представляют собой смесь сложных эфиров, глицерина и жирных предельных и не предельных кислот общей формулы
СН2ОН О CH2-OCO-R
½ \\ -ЗН2О ½
СНОН + 3C - R ——® CH-OCO-R
½ / ½
СН20Н НО CH2-OCO-R
Глицерин Кислота Глицерид
В состав глицеридов входят, например,, углеводородные остатки таких ненасыщенных кислот:
олеиновой С17Н33СООН, содержит одну двойную связь;
линолевой C17H31COOH, содержит две двойные связи;
линоленовой C17H29COOH, содержит три двойные связи.
Фрагменты углеводородов непредельного ряда способны к реакциям присоединения по месту двойных связей. Именно поэтому глицериды склонны к окислению кислородом воздуха, а значит и к самовозгоранию. Механизм окисления жиров и масел имеет сложный, многостадийный характер. На начальной стадии процесса кислород воздуха присоединяется по месту двойной связи с образованием нестойкого пероксида, который распадается на два активных радикала, продолжающих далее цепь окисления до промежуточных и конечных продуктов. В общем виде схема зарождения цепи выглядит следующим образом:
О—О
½ ½
R-CH=CH-R' + О2 ¾® R-CH-CH-R' -> R-HCO& + &OCH-R¢. Глицерид Пероксид
Ненасыщенные соединения по месту двойных связей, помимо кислорода, легко присоединяют галогены, в том числе и йод:
-СН=СН- + J2 ¾® -CHJ-CHJ-.
Эта реакция протекает количественно, поэтому ее используют для оценки непредельности соединений. За меру количества двойных связей принимается йодное число.
Йодное число - это количество йода (в граммах), поглощенное 100 граммами вещества.
Оно может быть использовано для оценки склонности масел и жиров к самовозгоранию (табл.1). Практика показала, что к самовозгоранию склонны жиры и масла с йодным числом выше 50.
Таблица 1
 2015-04-17
2015-04-17 1202
1202
