Число протонов в атоме химического элемента численно равно порядковому номеру в таблице Менделеева, а так же заряду ядра, так как заряд протона равен единице. Число нейтронов равно разности атомной массы и числа протонов. Ядра с одинаковым количеством протонов, но разным количеством нейтронов называются изотопами. Ядра с одинаковым массовым числом, но разным зарядом называются изобары. Например, 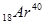 и
и 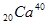 . Ядра с одинаковым числом нейтронов называются изотонами. Например, 6С13 и 7N14. Есть такие атомы, ядра которых могут распадаться как альфа-распадом, так и бета-распадом. Тогда естественно периоды полураспада будут разными. Ядра всех элементов до 82 в таблице имеют стабильные изотопы, кроме технеция и прометия.
. Ядра с одинаковым числом нейтронов называются изотонами. Например, 6С13 и 7N14. Есть такие атомы, ядра которых могут распадаться как альфа-распадом, так и бета-распадом. Тогда естественно периоды полураспада будут разными. Ядра всех элементов до 82 в таблице имеют стабильные изотопы, кроме технеция и прометия.
Весь положительный заряд сконцентрирован в центре атома. Если представить что ядро шарик с диаметром один сантиметр, то до первой Боровской орбиты будет 1 километр. Размеры атомных ядер.
1 ангстрем (А)=10-10 м – размеры атома
1 ферми (Ф)=10-15 м = 1 фемтометр (ФМ) – размеры ядра
Известно примерно 1500 ядер, из них примерно 300 стабильны.
Почти вся масса атома сконцентрирована в ядре.
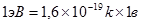
 2015-04-30
2015-04-30 442
442








