(Повторение лекционного материала).
В пламени одновременно протекают химические и физические процессы, между которыми существуют определенные причинно-следственные связи.
К химическим процессам в пламени относятся:
на подходе к зоне горения:
- термическое разложение исходных веществ с образованием более легких продуктов (водорода, оксидов углерода, простейших углеводородов, воды и т.д.);
во фронте пламени:
- термоокислительные превращения с выделением теплоты и образованием продуктов полного (диоксида углерода и воды) и неполного горения (оксида углерода, сажи, копоти, смол и др.);
- диссоциация продуктов горения,
- ионизация продуктов горения.
К физическим процессам в пламени относятся:
- тепломассоперенос во фронте пламени;
- процессы, связанные с испарением и доставкой летучих горючих веществ в зону горения.
Скорость переноса (диффузии) веществ имеет решающее значение, например, в неоднородных системах, где она гораздо меньше скорости химических реакций окисления. Соотношение скорости химических превращений и физических процессов определяет режим процесса горения.
Полное время горения tг, складывается из длительности физических и химических процессов:
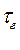 =
= 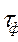 +
+ 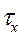
Кинетический режим горения характеризуется длительностью
tг» tх, поскольку в этом случае физических процессов подготовки (перемешивания) не требуется, т.е. tф» 0
Диффузионный режим горения, наоборот, зависит в основном от скорости подготовки однородной горючей смеси, т.е. длительность его
tг» tф. В этом случае tф >> tх, и поэтому последним можно пренебречь.
Если tф» tх, т.е. они соизмеримы, то горение протекает в так называемой промежуточной области.
Вспомним, что для процесса горения необходимы горючее вещество, окислитель и источник тепла (зажигания).
Горючие вещества и материалы классифицируют по химической природе, происхождению, агрегатному состоянию, дисперсности и т.д.
По химической природе горючие вещества и материалы подразделяются на два основных класса: органические и неорганические (рис.1.). Такое подразделение весьма условно, поскольку многие органические вещества содержат как в химически связанном, так и в виде примесей неорганические компоненты, нелетучая часть которых остается в виде золы, шлаков и.т.п.
Органические горючие вещества – это все вещества на основе углерода, представляющие собой материалы растительного и животного происхождения, или же ископаемые вещества, т.е. добываемые из недр земли. Все они применяются как в натуральном виде, так и после соответствующей обработки.
Неорганические горючие вещества и материалы представляют собой все простые и сложные вещества неорганической природы, способные к реакциям горения. По современной химической классификации это металлы и неметаллы, их различные производные.
К горючим металлам и их производным относятся все щелочные и щелочноземельные металлы, а также металлы других групп периодической системы Д.И. Менделеева и их производные - карбиды, сульфиды и т.п.
К горючим неметаллам и их производным относятся бор, кремний, фосфор, мышьяк, сера, селен, теллур, их карбиды, гидриды, сульфиды и т.д.
По агрегатному состоянию горючие вещества и материалы подразделяются на газообразные, жидкие и твердые.
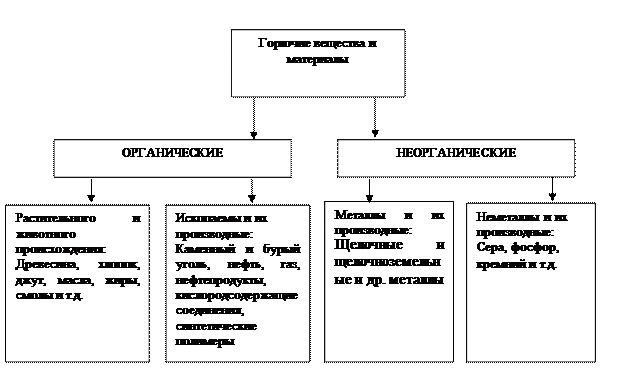
Рис. 1. Классификация горючих веществ и материалов.
Все индивидуальные вещества могут быть охарактеризованы коэффициентом горючести.
Коэффициент горючести К является безразмерным коэффициентом и служит для определения горючести вещества. Рассчитанный коэффициент горючести может быть использован для приближенного вычисления температуры вспышки вещества, а также величины нижнего концентрационного коэффициента распространения пламени.
Коэффициент горючести рассчитывается по следующей формуле:
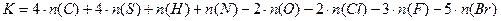 где:
где:
n(C), n(S), n(H), n(N), n(O), 2 n(Cl), n(F), n(Br) – число атомов углерода, серы, водорода, азота, кислорода, хлора, фтора и брома в молекуле вещества.
Если коэффициент горючести К больше единицы (К ³ 1), то вещество является горючим; при значении К меньше единицы (К < 1) – вещество негорючее.
| Расчет коэффициента горючести | Пример 1. Рассчитать коэффициент горючести анилина С6Н5NH2 и хлорной кислоты HClO4. |
Решение:
1. В молекуле анилина
n(C) = 6; n(Н) = 7; n(N) = 1;
К = 4 × 6 + 7 + 1 = 32
К > 1, следовательно, анилин – горючее вещество.
2. В молекуле хлорной кислоты
n(Н) = 1; n(Cl) = 1; n(О) = 4;
К = 1 – 2 × 4 – 2 × 1 = - 9
К < 1, хлорная кислота – негорючее вещество.
Окислители - это вещества, атомы которых в химических превращениях принимают электроны. Среди простых веществ к ним относятся все галогены и кислород.
Наиболее распространенным в природе окислителем является кислород воздуха. Именно ему человечество обязано широким распространением пожаров на Земле. Воздух содержит 21 % по объему кислорода и 79 % азота. На один объем (моль) кислорода в воздухе приходится 79/21 = 3,76 объема (моля) азота, который не вступает в реакции горения. Однако его приходится учитывать при составлении уравнения материального и теплового баланса процессов горения, поскольку часть теплоты расходуется на его нагревание.
Горение в воздухе - основной процесс на пожаре, однако во многих технологических процессах используется воздух, обогащенный кислородом, и даже чистый кислород (например, металлургические производства, газовая сварка, резка и т.д.). С атмосферой, обогащенной кислородом, можно встретиться в подводных и космических аппаратах, доменных процессах и т.д. Такие горючие системы имеют повышенную пожарную опасность. Это необходимо учитывать при разработке систем пожаротушения, пожарно-профилактических мероприятий и при пожарно-технической экспертизе пожаров.
Помимо кислорода воздуха и галогенов окислителями в реакциях горения могут выступать и сложные вещества, например, соли кислородсодержащих кислот - нитраты, хлораты и т.п., применяемые в производстве порохов, боевых и промышленных взрывчатых веществ и различных пиротехнических составов.
Состав продуктов горения зависит от состава исходного вещества.
| Элементы, входящие в состав горючего вещества | Продукты горения |
| Углерод С | Углекислый газ СО2 |
| Водород Н | Вода Н2О |
| Сера S | Оксид серы (IV) SO2 |
| Азот N | Молекулярный азот N2 |
| Фосфор Р | Оксид фосфора (V) Р2О5 |
| Галогены F, Cl, Br, I | Галогеноводороды HCl, HF, HBr, HI |
|
Решение:
Составление реакций горения веществ в воздухе аналогично составлению реакций горения в кислороде. Особенность состоит только в том, что азот воздуха при температуре горения ниже 20000С в реакцию горения не вступает и выделяется из зоны горения вместе с продуктами горения.
Горение водорода в воздухе
Н2 + 0,5(О2 + 3,76N2) = Н2О + 0,5×3,76N2 b = 0,5.
Обратите внимание, что стехиометрический коэффициент перед кислородом
b = 0,5 необходимо поставить и в правой части уравнения перед азотом.
Горение пропанола в воздухе
С3Н7ОН + 4,5(О2 + 3,76N2) =3СО2 + 4Н2О +4,5×3,76N2
b = 4,5.
В составе горючего есть кислород, поэтому расчет коэффициента b проводят следующим образом: 10 – 1 = 9; 9: 2 = 4,5.
Горение анилина в воздухе
С6Н5NН2 + 7,75(О2 + 3,76N2) =6СО2 + 3,5Н2О + 0,5N2 +7,75×3,76N2
b = 7,75.
В этом уравнении азот в правой части уравнения встречается дважды: азот воздуха и азот из горючего вещества.
Горение угарного газа в воздухе
СО + 0,5(О2 + 3,76N2) =СО2 + 0,5×3,76N2
b = 0,5.
Горение хлорметана в воздухе
СН3Сl + 1,5(О2 + 3,76N2) =СО2 + НСl + Н2О +1,5×3,76N2
b = 1,5.
Горение диэтилтиоэфира в воздухе
(С2Н5)2 S + 7,5(О2 + 3,76N2) =4СО2 + 5Н2О + SO2 + 7,5×3,76N2
b = 7,5.
Горение диметилфосфата в воздухе
(СН3)2НР О4 + 3(О2 + 3,76N2) =2СО2 + 3,5Н2О + 0,5Р2О5 + 3×3,76N2
b = 3.
В процессах горения исходными веществами являются горючее вещество и окислитель, а конечными - продукты горения.
 2015-05-05
2015-05-05 7459
7459
