Поверхностные явления в коллоидах играют первостепенную роль, т.к. являясь микрогетерогенными системами, они обладают колоссальной поверхностью раздела между частицами дисперсной фазы и дисперсионной среды. Наличие сильно развитой поверхности в коллоидных растворах объясняет многие физико-химические особенности этих систем. Поэтому можно сказать, что коллоидная химия – это физическая химия дисперсных систем и поверхностных явлений.
Адсорбция
Концентрирование вещества, равномерно распределенного в одной из фaз дисперсной системы, на границе раздела фаз называется адсорбцией.
Адсорбция обусловлена наличием адсорбционных сил, имеющих различную природу. Различают межмолеклярные (ван-дер-ваальсовы) ихимические (ионные, ковалентные) силы.
Иногда адсорбция, начавшись на поверхности, распространяется в глубь частицы. Такой процесс называют абсорбцией, если такое поглощение сопровождается химическим взаимодействием, то такой процесс носит название хемосорбции.
Вещество, способное адсорбировать на своей поверхности другое вещество или ионы, называется адсорбентом. Адсорбируемое вещество называется адсорбтивом.
Явления адсорбции, абсорбции и хемосорбции объединены общим понятием сорбции.
Процесс адсорбции обратим. Частицы в адсорбционных слоях совершают колебательные движения, то приближаясь к адсорбенту, то удаляясь от него. Некоторые из них могут выходить за пределы действия сил притяжения адсорбента. В этом случае наблюдается обратный процесс – десорбция,
Со временем система приходит в состояние адсорбционного равновесия:

Адсорбция носит избирательный характер. Так, например, активированный уголь хорошо поглощает хлор, но не адсорбирует окись углерода.
Процесс адсорбции экзотермичен и, следовательно, в соответствии с принципом Ле-Шателье, с ростом температуры адсорбция падает, и равновесие сдвигается в сторону процесса десорбции.
Все растворимые вещества по их способности адсорбироваться на границе раздела фаз делятся на две группы: поверхностно-активные (ПАВ) вещества и поверхностно-неактивные. Характерной особенностью ПАВ является то, что молекулы ихсодержат две части: полярную гидрофильную (растворимую в воде) и неполярную гидрофобную (в воде нерастворимую). При растворении таких веществ в воде они погружают свои гидрофильные группы в воду, а гидрофобная часть располагается выше уровня воды, т.е. как бы «торчит» из воды.

Рис.1.3. Ориентация ПВА на границе раздела фаз
Если же поверхностно-активное вещество равномерно распределено в одной из двух неcмешивающихся жидкостей, то оно концентрируется на границе раздела этих двух фаз:
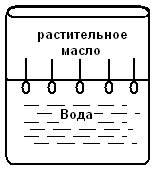
Рис.1.4. Концентрация частиц на границе раздела фаз (адсорбция)
Обычно углеводородный радикал гидрофобный, а функциональные группы -ОН, -CООH, -NH2 и т.д. – гидрофильные Чем длиннее углеводородный радикал, тем меньше растворимость его в воде, но тем выше становится его способность к адсорбции. Эта закономерность получила название правила Траубе-Дюкло. Это правило применимо к разбавленным растворам.
Процессы адсорбции происходят ив живых организмах. Роль твердого тела играют здесь мембраны и коллоидные частицы. Так, вещества, образующиеся после переваривания в желудочно-кишечном тракте белков, углеводов и т.д. (это соответственно аминокислоты, глюкоза и т.д.), попадают в кровь и адсорбируются из крови на внешней мембране клеток. Только после этого процесса клетка поглощает эти питательные вещества (служащие либо источником энергии, либо строительным материалом клеток).
Одним из главных свойств абсорбции является её избирательность. На способности избирательного поглощения адсорбентами растворенных веществ основаны хроматографические методы анализа, позволяющие разделять сложные смеси на отдельные фракции. Впервые это метод был использован русским ботаником М.С.Цветом (1903 г.) для разделения зеленого вещества растений – хлорофилла на составные части. Хроматография широко применяется при разделении и очистке лекарственных веществ, витаминов, аминокислот, ионов, углеводородов нефтяных фракций и др.
Впоследние годы широкое распространение получили методы ионообменной хроматографии.
 2015-04-30
2015-04-30 500
500







