Cr Х Сl 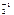 Сr
Сr 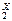 O
O 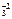
Х + (–1) ∙ 2 = 0 Х ∙ 2 + (–2) ∙ 3 = 0
Х = +2 Х = +3
K 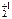 Cr
Cr 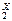 O
O 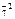
(+1) ∙ 2 + Х ∙ 2 + (–2) · 7 = 0
Х = +6
K2Cr 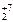 O7 – Cr
O7 – Cr 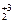 O3 – Cr+2Cl2.
O3 – Cr+2Cl2.
2. Составить уравнения для следующих процессов и назвать их:
а) Ni0 → Ni+2
б) 2I- → I2
в) Cu+2 → Cu0
Ответ:
а) Ni0 – 2е = Ni+2 – процесс окисления;
б) 2I 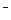 – 2е = I20 – процесс окисления;
– 2е = I20 – процесс окисления;
в) Cu+2 + 2е = Cu0 – процесс восстановления.
3. Какие свойства (окислительные или восстановительные) проявляют PbO2 ; H2S; KMnO4 ?
Ответ: окислители – атомы, молекулы или ионы, присоединяющие электроны, а восстановители – отдающие электроны. Поэтому чем выше степень степень окисления иона, тем сильнее он проявляет окислительные свойства, а чем ниже степень окисления иона – тем сильнее его восстановительные свойства.
Pb+4O2 – окислитель H2S-2 – восстановитель
KMn+7 O4 – окислитель
 2015-05-10
2015-05-10 314
314








