Флуоресценция и фосфоресценция различаются природой квантовых переходов. В структуре энергетических уровней молекулы параллельно существуют две системы уровней: синглентные и триплетные (рис. 6.). Эти уровни различаются мультиплетностью. Мультиплетность рассчитывается как величина 2S+1, где S – спиновое квантовое число, спин электрона равен ± 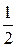 . Мультиплетность синглетных уровней равна 1. Два электрона на этих уровнях характеризуются противоположно направленными спинами: 2 (+
. Мультиплетность синглетных уровней равна 1. Два электрона на этих уровнях характеризуются противоположно направленными спинами: 2 (+ 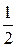 -
- 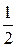 )+1=1. Мультиплетность триплетных уровней равна 3. Два электрона на этих уровнях характеризуются сонаправленными спинами: 2 (+
)+1=1. Мультиплетность триплетных уровней равна 3. Два электрона на этих уровнях характеризуются сонаправленными спинами: 2 (+ 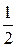 +
+ 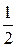 )+1=3. Основной уровень молекулы является синглетным, а возбужденные уровни могут быть и синглетными, и триплетными. Флуоресценция соответствует квантовым переходам с возбужденных синглетных уровней на основной синглетный уровень, а фосфоресценция – с возбужденных триплетных уровней на основной синглетный. Вероятность переходов между уровнями различной мультиплетностью (последний случай) очень мала. На возбужденном триплетном уровне электрон может находиться длительное время. Такой уровень называется метастабильным. И поэтому длительность фосфоресценции велика (более 10-3 с), по сравнению с длительностью флуоресценции (@10-8 с).
)+1=3. Основной уровень молекулы является синглетным, а возбужденные уровни могут быть и синглетными, и триплетными. Флуоресценция соответствует квантовым переходам с возбужденных синглетных уровней на основной синглетный уровень, а фосфоресценция – с возбужденных триплетных уровней на основной синглетный. Вероятность переходов между уровнями различной мультиплетностью (последний случай) очень мала. На возбужденном триплетном уровне электрон может находиться длительное время. Такой уровень называется метастабильным. И поэтому длительность фосфоресценции велика (более 10-3 с), по сравнению с длительностью флуоресценции (@10-8 с).


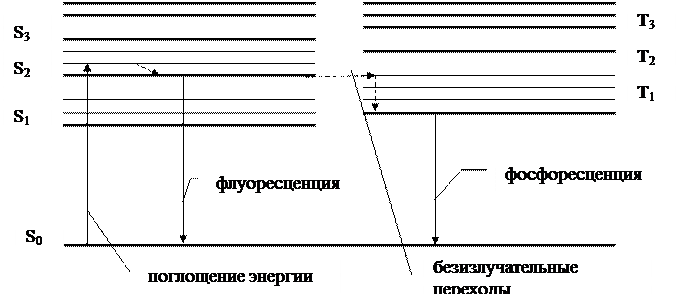
Рис. 6. Системы синглетных и триплетных энергетических уровней молекулы.
Вопрос 5. 5 минут
 2015-05-10
2015-05-10 1956
1956








