Абсолютные давления газов в баллонах до открытия задвижки согласно (1.1):
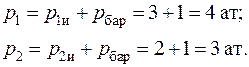
Массы газов в баллонах находятся из уравнения состояния идеального газа (1.4):
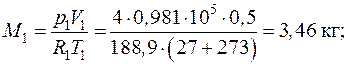
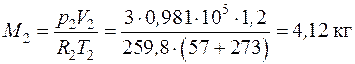 .
.
Здесь газовые постоянные компонентов рассчитываются как:
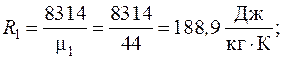
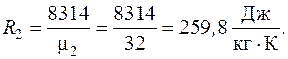
Масса смеси, согласно закону сохранения масс, находится как
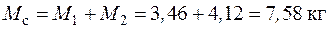 .
.
Тогда массовый состав смеси можно найти по определению массовой доли (2.2):
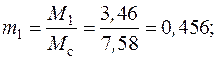
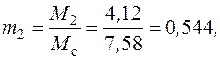
а объемный состав смеси – по формуле (2.4):
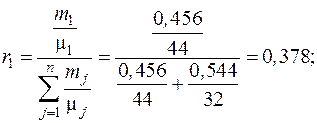
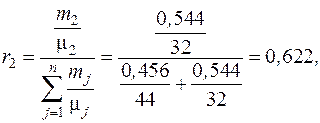
причем выполняются равенства:
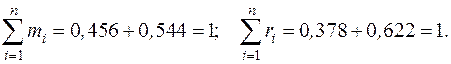
Молекулярная масса смеси согласно (2.5):
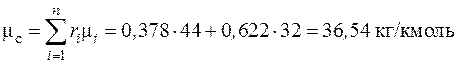 .
.
Газовая постоянная смеси по (2.6):
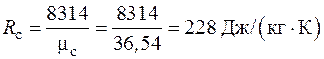 .
.
Давление смеси найдем из уравнения состояния идеального газа (1.4), записанного для смеси
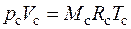 ,
,
где объем смеси найдется как сумма объемов первого и второго баллонов (объемом трубы пренебрегаем):
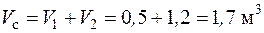 .
.
Тогда
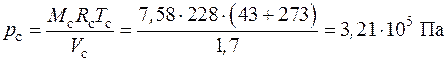 .
.
Парциальные давления компонентов согласно (2.8) будут равны:
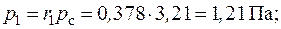
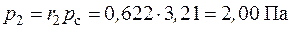 ,
,
причем 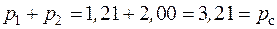 , т. е. закон Дальтона (2.1) выполняется.
, т. е. закон Дальтона (2.1) выполняется.
2.2. Атмосферный воздух имеет следующий массовый состав: кислород О2 – 23,2 %, азот N2 – 76,8 %. Определить объемный состав воздуха, его газовую постоянную, молекулярную массу и парциальные давления кислорода и азота, если барометрическое давление воздуха 760 мм рт. ст.
Ответ: 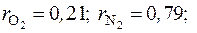
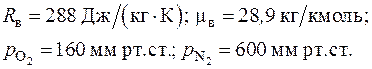
2.3. Определить газовую постоянную смеси газов, образованной при смешении 1 м3 генераторного газа и 1,5 м3 воздуха, взятых при нормальных физических условиях, и парциальные давления компонентов смеси. Плотность генераторного газа принять равной 1,2 кг/м3.
Ответ: 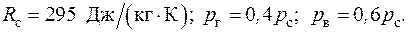
2.4. Смесь 10 кг кислорода и 15 кг азота имеет давление 3 бар и температуру 27 оС. Определить объемный состав смеси, молекулярную массу, газовую постоянную и объем смеси, парциальные давления и приведённые объемы компонентов смеси.
Ответ: 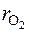 = 0,368;
= 0,368; 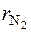 = 0,632; μс = 29,47 кг/кмоль;
= 0,632; μс = 29,47 кг/кмоль;
Rс = 282,1 Дж/(кмоль×К); V с= 7,053 м3.
2.5. 0,3 м3 воздуха смешиваются с 0,5 м3 углекислого газа. Оба газа до смешения имели давление 6 бар и одинаковую температуру. Определить парциальное давление углекислого газа после смешения.
Ответ: 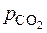 = 3,75 бар.
= 3,75 бар.
2.6. Известно, что перегретый водяной пар, содержащийся в атмосферном воздухе, с достаточной степенью точности может считаться идеальным газом. Вычислить массу водяных паров, содержащихся во влажном воздухе помещения размерами 6×5×3 м3 при давлении p = 745 мм рт. ст. и при температуре t = 20 оС, если парциальное давление водяных паров 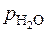 = 14 мм рт. ст.
= 14 мм рт. ст.
Ответ: 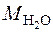 = 1,24 кг.
= 1,24 кг.
2.7. Влажный воздух представляет собой смесь сухого воздуха и водяного пара. Известно, что на каждый килограмм сухого воздуха во влажном воздухе приходится d г/кгс.в. водяного пара. Определить массовые и объемные доли сухого воздуха и водяного пара, плотность при нормальных условиях, газовую постоянную и молекулярную массу влажного воздуха, если d = 10 г/кгс.в..
Ответ: 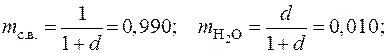
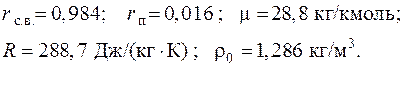
2.8. Горючая смесь состоит из водорода H2 и этана C2H6 и задана объемными долями: 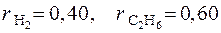 . Подсчитать объем сухого воздуха, теоретически необходимый для сжигания 1 м3 смеси при нормальных физических условиях.
. Подсчитать объем сухого воздуха, теоретически необходимый для сжигания 1 м3 смеси при нормальных физических условиях.
 2015-05-13
2015-05-13 6512
6512
