Выражение 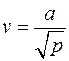 легко приводится к стандартному соотношению для политропного процесса в переменных p–v
легко приводится к стандартному соотношению для политропного процесса в переменных p–v 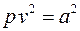 , откуда следует значение показателя политропы процесса n = 2. Далее, используя уравнение состояния идеального газа pv=RT, находим зависимость температуры в процессе от текущего значения объема
, откуда следует значение показателя политропы процесса n = 2. Далее, используя уравнение состояния идеального газа pv=RT, находим зависимость температуры в процессе от текущего значения объема
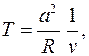
откуда получаем
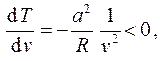
т. е. температура газа в процессе расширения по указанному закону уменьшается.
Изобразим процессы в p–v и T–s координатах (рис. 6.14)
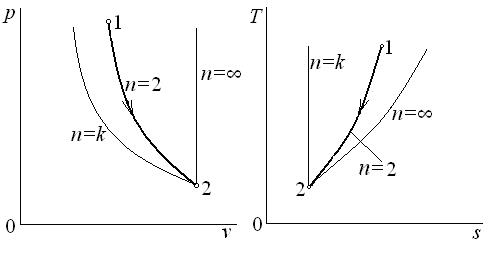
Рис. 6.14. К задаче 6.15
6.16. Перестроить группу процессов идеального газа из одной термодинамической диаграммы в другую. Указать знаки теплоты q, работы изменения объема l и изменения внутренней энергии Δ u для каждого из процессов.
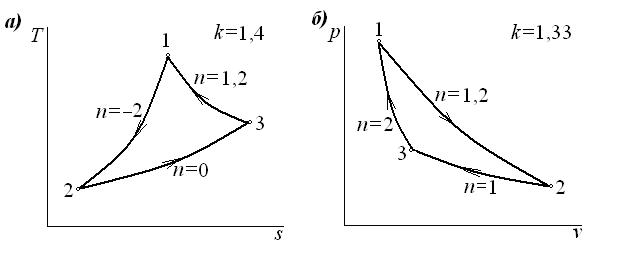
a) из p–v в T–s б) из T–s в p–v
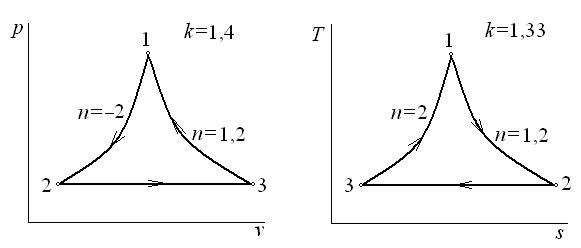
Ответ:
| Процесс | l | q | Δ u | Процесс | l | q | Δ u | |
| 1–2 | <0 | <0 | <0 | 1–2 | >0 | >0 | <0 | |
| 2–3 | >0 | >0 | >0 | 2–3 | <0 | <0 | =0 | |
| 3–1 | <0 | <0 | >0 | 3–1 | <0 | >0 | >0 |
 2015-05-13
2015-05-13 1215
1215
