Ведущими клиническими проявлениями холестаза (как острого, так и хронического) являются кожный зуд и нарушение всасывания. При хроническом холестазе наблюдаются поражение костей (печёночная остеодистрофия), отложения холестерина (ксантомы, ксантелазмы) и пигментация кожи вследствие накопления меланина. В отличие от больных с гепатоцеллюлярным заболеванием слабость и утомляемость нехарактерны. При объективном исследовании печень, как правило, увеличена, с гладким краем, уплотнена, безболезненна. Спленомегалия нехарактерна, если нет билиарного цирроза и портальной гипертензии. Кал обесцвечен.
Кожный зуд рассматривают как следствие задержки жёлчных кислот. Однако даже с помощью точных биохимических методов не удаётся выявить корреляцию между выраженностью зуда и концентрацией эндогенных жёлчных кислот в сыворотке и коже |32|. Более того, в терминальной стадии печёночной недостаточности кожный зуд может исчезать, в то время как концентрация жёлчных кислот в сыворотке остаётся повышенной.
Предполагается, что кожный зуд при холестазе вызывают соединения, в норме экскретирующиеся в жёлчь и, возможно, синтезирующиеся в печени (в пользу этого свидетельствует исчезновение зуда в терминальной стадии печёночной недостаточности). Приём холестирамина эффективен, однако препарат обладает способностью связывать многие соединения, что не позволяет выделить конкретный агент, ответственный за развитие зуда.
Повышенное внимание привлекают соединения, которые могут вызывать кожный зуд путём воздействия на центральные нейротрансмиттерные механизмы [47]. Данные экспериментальных исследований на животных и результаты испытаний лекарственных препаратов позволяют предполагать роль эндогенных опиоидных пептидов в развитии зуда [8]. У животных с холестазом развивается состояние анальгезии вследствие накопления эндогенных опиатов, которое может быть устранено налоксоном. Выраженность зуда у больных с холестазом уменьшается при лечении налоксоном [7]. Антагонист 5-НТ3-серотониновых рецепторов ондансетрон также уменьшает зуд у больных с холестазом [75]. Необходимы дальнейшее исследование патогенеза кожного зуда и поиск эффективных и безопасных методов борьбы с этим мучительным, иногда изнуряющим симптомом холестаза.
Стеаторея обусловлена недостаточным содержанием солей жёлчных кислот в просвете кишечника, необходимых для всасывания жиров и жирорастворимых витаминов А, Д, К, Е (рис. 13-11 и 13-12), и соответствует выраженности желтухи. Отсутствует адекватное мицеллярное растворение липидов. Стул становится жидким, слабоокрашенным, объёмным, зловонным. По цвету кала можно судить о динамике обструкции жёлчных путей (полной, интермиттирующей, разрешающейся).
Жирорастворимые витамины. При непродолжительном холестазе, когда планируется исследование или лечение инвазивными методами, может потребоваться коррекция увеличенного протромбинового времени введением витамина К.
При длительном холестазе снижается уровень витамина А в сыворотке вследствие нарушения всасывания; процесс накопления витамина в печени не нарушен [62]. При истощении печёночных запасов витамина А наступает нарушение адаптации глаза к темноте («куриная слепота») [86]. Может наблюдаться также дефицит витамина Д, приводящий к остеомаляции.
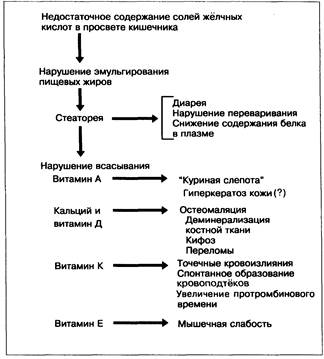
Рис. 13-11. Последствия дефицита жёлчи в просвете кишечника при хронической холестатической желтухе.
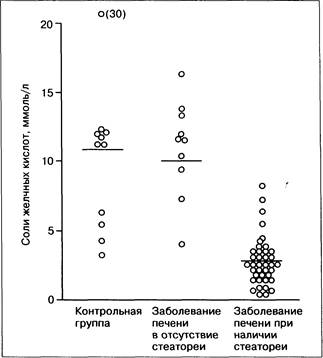
Рис. 13-12. Концентрация солей жёлчных кислот в аспирате кишечного содержимого у больных с неалкогольным поражением печени при наличии и отсутствии стеатореи [6].
Имеются сообщения о дефиците витамина Е при холестазе у детей [24, 82]. Клинические проявления включают мозжечковую атаксию, дисфункцию задних столбов спинного мозга, периферическую полиневропатию и дегенерацию сетчатки. У взрослых больных при повышении уровня билирубина в сыворотке более 100 мкмоль/л (6 мг%) уровень витамина Е снижен всегда |46|, однако специфический неврологический синдром не развивается.
Ксантомы. Развитие ксантом наблюдается при хроническом холестазе. В наши дни ксантомы встречаются реже, так как лечение холестаза (в том числе трансплантация печени) проводится на достаточно ранних этапах. Разновидность ксантом — ксантелазмы — представляют собой плоские или слегка возвышающиеся мягкие образования жёлтого цвета, обычно вокруг глаз. Ксантомы могут также наблюдаться в ладонных складках, под молочными железами, на шее (рис. 13-13 и 13-14), груди или спине. Туберозные ксантомы появляются позднее и обнаруживаются на разгибательных поверхностях, особенно в области лучезапястных, локтевых, коленных суставов, лодыжек, ягодиц (рис. 13-15), в местах, подвергающихся давлению, в рубцах. Сухожильные влагалища поражаются редко. Могут поражаться кости, иногда периферические нервы [84]. Локальные скопления ксантомных клеток обнаруживаются в печени.
Ксантомы кожи развиваются пропорционально уровню сывороточных липидов. Появлению ксантом предшествует длительное (более 3 мес) повышение уровня холестерина в сыворотке более 11,7 мкмоль/л (450 мг%). Ксантомы исчезают при разрешении холестаза и нормализации уровня холестерина или в терминальной стадии печеночной недостаточности.
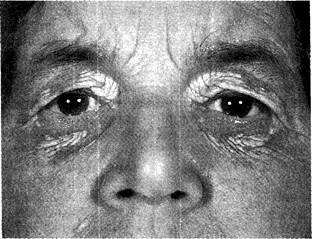
Рис. 13-13. ПБЦ. Ксантелазмы и гиперпигментация кожи. См. также цветную иллюстрацию на с. 772.
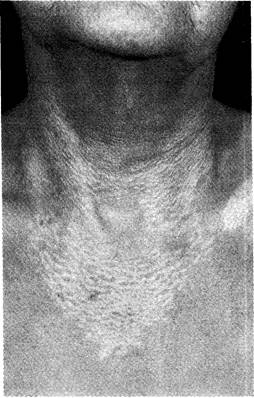
Рис. 13-14. ПБЦ. Ксантоматозное поражение кожи в области воротниковой зоны. См. также цветную иллюстрацию на с.773.
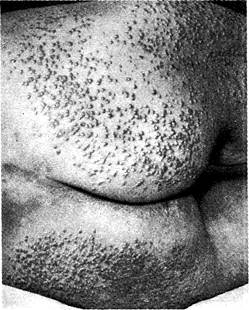
Рис. 13-15. ПБЦ. Хроническая обструктивная желтуха. Туберозные ксантомы на ягодицах.
ПЕЧЁНОЧНАЯ ОСТЕОДИСТРОФИЯ [39]
Поражение костей является осложнением хронических заболеваний печени, особенно холестатических, при которых оно наиболее детально изучено. Наблюдаются боли в костях и переломы. Вероятными причинами этого являются остеомаляция и остеопороз. Исследования при ПБЦ и ПСХ показали, что в большинстве случаев поражение костей обусловлено остеопорозом, хотя определённое значение имеет и остеомаляция.
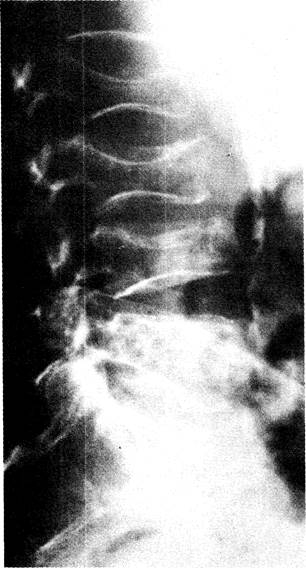
Рис. 13-16. ПБЦ с желтухой, длящейся 3 года. Выраженная двояковогнутая деформация и компрессия тел поясничных позвонков.
Поражение костей проявляется болями в спине (обычно в грудном или поясничном отделе позвоночника), уменьшением роста, компрессией тел позвонков, переломами при минимальных травмах, особенно рёбер. Рентгенография позвоночника позволяет выявить снижение плотности и компрессионные переломы тел позвонков (рис. 13-16).
Минеральная плотность костной ткани может быть определена методом двойной абсорбционной фотометрии. У 31% из 123 женщин, больных ПБЦ, при использовании данного метода было выявлено тяжёлое поражение костей. В дальнейшем у 7% наблюдались переломы [14]. Снижение минеральной плотности костной ткани также выявлено у больных с далеко зашедшим ПСХ с повышенным уровнем билирубина (рис. 13-17).
Патогенез поражения костей окончательно не уточнён. Предполагается участие нескольких факторов. Нормальная структура костной ткани поддерживается равновесием двух разнонаправленных процессов: резорбции кости с помощью остеокластов и формирования остеобластами новой кости. Перестройка костной ткани начинается с уменьшения числа клеток бездействующих зон кости. Остеокласты, резорбируя кость, формируют лакуны. В дальнейшем эти клетки замешаются остеобластами, которые наполняют лакуны новой костью (остеоидом), коллагеном и другими белками матрикса. Затем происходит кальцийзависимый, а следовательно, и витамин Д-зависимый процесс минерализации остеоида. Метаболические костные нарушения включают две основные формы: остеомаляцию и остеопороз. При остеопорозе наблюдается потеря костной ткани (матрикса и минеральных элементов). При остеомаляции страдает минерализация остеоида. Верификация костных нарушений при хроническом холестазе проводилась с помощью биопсии и изучения костной ткани с использованием специальных методик.
Исследования показали, что в большей части случаев печёночная остеодистрофия представлена остеопорозом. При хронических холестатических заболеваниях выявлено как снижение образования новой кости, так и повышение резорбции костной ткани. Высказано предположение, что в ранней, доцирротической стадии поражения происходит нарушение процесса образования кости, в то время как при циррозе — повышение резорбции [39]. У женщин, не имеющих заболевания печени, в менопаузе усилены процессы образования новой кости и резорбции костной ткани с преобладанием последней [57]. Это может играть роль в поражении костей при ПБЦ у женщин в менопаузе.
Причина остеопороза при хронических холестатических заболеваниях печени окончательно не установлена. Патогенетическое значение могут иметь многие факторы, участвующие в метаболизме костной ткани: витамин Д, кальцитонин, паратгормон, гормон роста, половые гормоны. На состояние костей у больных с хроническим холестазом оказывают влияние такие внешние факторы, как ограниченная подвижность, неполноценное питание, уменьшение мышечной массы. Уровень витамина Д снижается вследствие нарушения всасывания, неадекватного поступления с пищей, недостаточного пребывания на солнце. Однако лечение витамином Д не влияет на состояние костной ткани. Процессы активации витамина Д в печени (25-гидроксилирование) и в почках (1-гидроксилирование) не нарушены.
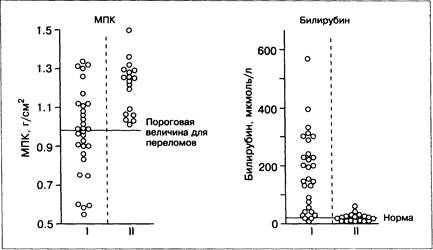
Рис. 13-17. Минеральная плотность кости (МПК) и концентрация билирубина в сыворотке у больных с далеко зашедшим ПСХ (I) и недавно диагностированным ПСХ (II) [41|.
В недавних исследованиях было показано уменьшение пролиферации остеобластов под действием плазмы, полученной от больных с желтухой; при этом ингибирующее действие оказывал неконъюгированный билирубин, но не жёлчные кислоты |451. Эти данные позволяют объяснить нарушения формирования костной ткани при хроническом холестазе, однако требуют дальнейшего подтверждения.
Лечение урсодезоксихолевой кислотой не останавливает потерю костной массы у больных с ПБЦ |53|. После трансплантации печени плотность кости повышается лишь через 1— 5 лет [5,40|. В течение первого года часто у 35% больных с ПСХ наблюдаются спонтанные переломы. Возможно, одна из причин высокой частоты переломов — применение кортикостероидов с целью иммуносупрессии. Уровень витамина Д не возвращается к нормальному на протяжении нескольких месяцев после трансплантации. В связи с этим рекомендуется заместительная терапия |5|.
Определение уровня витамина Д у больных с хроническим холестазом имеет большое значение, так как остеомаляция, несмотря на редкость, легко поддаётся лечению. При исследовании изоферментов ЩФ сыворотки, помимо печёночной, может быть повышена костная фракция фермента. По уровню кальция и фосфора в сыворотке невозможно предсказать развитие костных изменений. При рентгенографии обнаруживаются изменения, характерные для остеомаляции: псевдопереломы, зоны Лоозера. Рентгенография кистей выявляет разрежение костной ткани. При биопсии костей выявляются широкие некальцифицированные остеоидные массы, окружающие трабекулы. Причины снижения уровня витамина Д многочисленны. Больные с хроническим холестазом недостаточно времени проводят на воздухе под солнечными лучами, соблюдают неадекватную диету. Стеаторея, нарушение всасывания могут усугубляться длительным приёмом холестирамина.
Другим проявлением костной патологии является болезненная остеоартропатия лодыжек и запястий (рис. 13-18) [27] — неспецифическое осложнение хронических заболеваний печени.
 2015-06-10
2015-06-10 597
597








