По данным мировой статистики, распространённость носительства HBV коррелирует с заболеваемостью ГЦК [9,10,142]. Наибольшая частота развития ГЦК отмечается в странах с наибольшим количеством носителей HBV [40]. Показано, что риск возникновения ГЦК у носителей HBV выше, чем в популяции [10]. В развитии ГЦК доказана этиологическая роль и других представителей семейства гепаднавирусов, например вируса гепатита сурков [130]. В ткани ГЦК обнаруживается HBV-ДНК.
Канцерогенез — многостадийный процесс, в котором играет роль как вирус, так и организм хозяина [46,141]. Конечный результат этого процесса — дезорганизация и перестройка ДНК гепатоцитов (рис. 28-2). При гепатите В вирус интегрируется в хромосомную ДНК хозяина, однако молекулярный механизм канцерогенного эффекта HBV остаётся неясным. Интеграция сопровождается
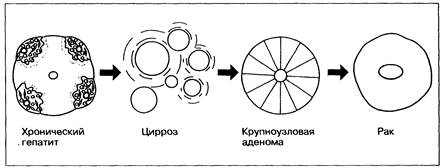
Рис. 28-1. Стадии развития ГЦК при хроническом гепатите через трансформацию в цирроз и образование крупных узлов-регенератов. См. также цветную иллюстрацию на с. 790.
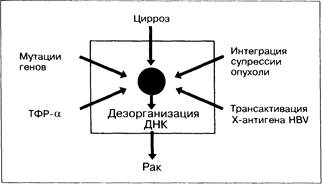
Рис. 28-2. Факторы, способствующие развитию ГЦК [141].
хромосомными делециями и транслокациями, которые влияют на рост и дифференцировку клеток (инсерционный мутагенез). Однако делеции не соответствуют участкам встраивания вирусной ДНК, а в 15% случаев рака последовательности вирусного генома в опухолевой ткани не обнаруживаются [46]. Показано, что встраивание HBV-ДНК в геном хозяина не сопровождается ни повышенной экспрессией какого-либо определённого протоонкогена, ни делециями специфического участка генома, несущего потенциальный антионкоген [46]. Характер интеграции в геном клеток хозяина непостоянен, и вирусный геном у разных больных может интегрироваться в различные участки ДНК опухолевых клеток.
Х-антиген HBV считается трансактиватором, повышающим скорость транскрипции онкогенов [36].
Пре-S-белок оболочки HBV может накапливаться в достаточных для развития опухоли токсических количествах. Повышенное образование пре-S-белка HBV у трансгенных мышей приводит к тяжёлому воспалению печени и регенерации с последующим развитием опухолей [25]. Нарушенная регуляция экспрессии белков оболочки HBV может быть следствием интеграции в ДНК клеток хозяина.
Интеграция HBV-ДНК приводит к транслокации генов-супрессоров опухоли на хромосоме 17. Таким образом, гены супрессии опухоли, например онкоген р53 на хромосоме 17, могут играть важную роль в HBV-зависимом гепатоканцерогенезе [65,101]. Трансформирующий фактор роста а (ТФР-а) усиленно экспрессируется у 80% больных с ГЦК. Возможно, он играет роль кофактора [64]. Гистохимические исследования показывают, что ТФР-а локализуется в тех же гепатоцитах, что и HBsAg, но отсутствует в опухолевых клетках.
Наибольшее значение в качестве предракового состояния имеет хронический гепатит В с исходом в цирроз. HBV приводит к развитию рака посредством интеграции, трансактивации, мутаций генов супрессии опухолей и повышения уровня ТФР-а.
У носителей HBsAg, инфицированных HDV, ГЦК встречается реже, возможно, вследствие подавляющего действия на HDV.
 2015-06-10
2015-06-10 361
361








