Для характеристики эффективности действия ПАВ используется понятие поверхностная активность (способность вещества снижать поверхностное натяжение на границе раздела фаз) - это производная поверхностного натяжения по концентрации ПАВ при стремлении С к нулю.
Поверхностную активность ПАВ при некоторой концентрации С1 определяют графически, проводя касательную к изотерме поверхностного натяжения в точке С = С1; при этом поверхностная активность численно равна тангенсу угла наклона касательной к оси концентраций:
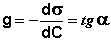
g = называют поверхностной активностью растворенного вещества.
Зависимость поверхностного натяжения от концентрации называется изотермой поверхностного натяжения.

Нетрудно заметить, что с ростом концентрации поверхностная активность ПАВ уменьшается. Поэтому поверхностную активность вещества обычно определяют при бесконечно малой концентрации раствора; в этом случае её величина, обозначаемая gо, зависит только от природы ПАВ и растворителя. Исследуя поверхностное натяжение водных растворов органических веществ, Траубе и Дюкло установили следующее эмпирическое правило:
В любом гомологическом ряду при малых концентрациях удлинение углеродной цепи на одну группу СН2 увеличивает поверхностную активность в 3 – 3.5 раза.
Часто в нормативных документах указывают не поверхностную активность, а значение поверхностного натяжения при заданной концентрации ПАВ.
Изменение поверхностного натяжения раствора при введении поверхностно – активных веществ (для малых и средних концентраций поверхностно-активных веществ) при описании зависимости σ = f(c) используется уравнение Шишковского:
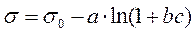
где σ0 – поверхностное натяжение растворителя (Н/м);
c – концентрация поверхностно-активного вещества (ПАВ);
a, b – константы, причем величина a мало меняется от вещества к веществу, а b зависит от поверхностной активности вещества
Следует отметить, что отнесение веществ к той или иной группе зависит от природы растворителя. Одно и тоже вещество для разных растворителей может быть и поверхностно-активным веществом (ПАВ), и не влиять на поверхностное натяжение.
2) Критическая концентрация мицеллообразования (ККМ)~ концентрация ПАВ в растворе, при которой в системе образуются в заметных количествах устойчивые мицеллы. При достижении ККМ мицеллы находятся в термодинамическом равновесии с неассоциированными молекулами ПАВ; при разбавлении раствора мицеллы распадаются, а при увеличении концентрации вновь возникают.
Мицеллообразование в растворах коллоидных ПАВ является наиболее термодинамически выгодным процессом по сравнению с процессами образования истинного раствора или разделения фаз. Это обусловлено переходом углеводородной или полярной части дифильных молекул ПАВ в подобную им по полярности фазу. Hапример, полярные группы молекул ПАВ обращаются к воде, поскольку они гидратированы, а углеводородные радикалы выталкиваются из водной фазы. Оба этих процесса сопровождаются выделением теплоты, что способствует уменьшению энергии Гиббса системы.
Выше ККМ весь избыток ПАВ находится в виде мицелл. При концентрациях, незначительно превышающих ККМ, мицеллы имеют сферическую форму. С ростом концентрации мицеллы начинают взаимодействовать, образуя более крупные мицеллы цилиндрической, дискообразной, палочкообразной, пластинчатой формы.
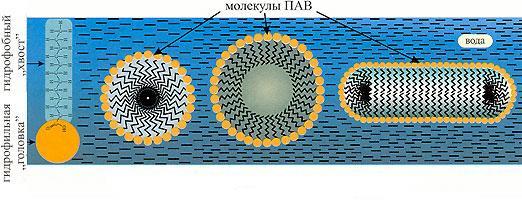
При очень большом содержании ПАВ в системе образуются жидкие кристаллы или гели.
В области ККМ изменяются поверхностное натяжение, показатель преломления, вязкость, электропроводимость раствора, светорассеяние.
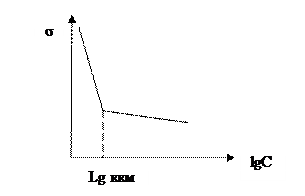 | Если излома нет, то ПАВ немицеллообразующее |
| Рисунок 2- Изотерма коллоидных ПАВ | |
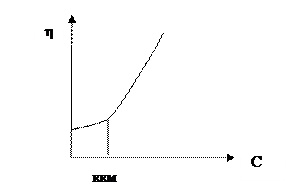 | При мицеллообразовании резко повышается вязкость. |
| Рисунок 3- Зависимость вязкости от концентрации раствора ПАВ |
В области концентраций до ККМ зависимости удельной и эквивалентной электропроводности от концентрации ПАВ соответствуют аналогичным зависимостям для растворов средних по силе электролитов. При концентрации, соответствующей ККМ, на графиках зависимости наблюдается излом, обусловленный образованием сферических ионных мицелл. Подвижности ионных мицелл меньше подвижности ионов и, кроме того, значительная часть противоионов находится в плотном слое Гельмгольца, что существенно уменьшает электропроводность раствора ПАВ. Поэтому при увеличении концентрации ПАВ больше ККМ, эквивалентная электропроводность более резко уменьшается, а возрастание удельной электропроводности значительно ослабляется. По изменению удельной электропроводности можно также определить ККМ.
Отличительным признаком мицеллообразования служит помутнение раствора ПАВ. Водные растворы ПАВ, при мицеллообразовании приобретают голубоватый оттенок (студенистый оттенок) за счёт преломления света мицеллами.
ККМ связана с поверхностной активностью зависимостью:
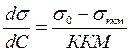
σ0 – поверхностное натяжение для растворителя.
Методы определения ККМ:
1. Метод поверхностного натяжения
2. Метод измерения контактного угла с тв. или жидкой поверхностью (Contact angle)
3. Метод вращающейся капли (Spindrop/Spinning drop)
Ккм необходимо для выбора условий применения ПАВ, если рабочая концентрация меньше ККМ, то ПАВ диспергаторы, если больше, то стабилизаторы.
 2015-06-14
2015-06-14 2135
2135








