Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Внутренняя энергия системы может изменяться в результате различных процессов, например, совершения над системой работы и сообщения ей теплоты. Так, вдвигая поршень в цилиндр, в котором находится газ, мы сжимаем этот газ, в результате чего его температура повышается, т.е. тем самым изменяется (увеличивается) внутренняя энергия газа. С другой стороны, температуру газа и его внутреннюю энергию можно повысить за счет сообщения ему некоторого количества теплоты - энергии, переданной: системе внешними телами путем теплообмена.
Таким образом, можно говорить о двух формах передачи энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии; применительно к термодинамическим процессам этим законом и является первое начало термодинамики, установленное в результате обобщения многовековых опытных данных.
Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U1, получила некоторое количество теплоты Q и, перейдя в новое состояние, характеризующееся внутренней энергией U2, совершила работу А над внешней средой, т.е. против внешних сил. Количество теплоты считается положительным, когда оно подводится к системе, а работа - положительной, когда система совершает ее против внешних сил. Опыт показывает, что в соответствии с законом сохранения энергии при любом способе перехода системы из первого состояния во второе изменение внутренней энергии DU=U2 –U1 будет одинаковым и равным разности между количеством теплоты Q, полученным системой, и работой А, совершенной системой против внешних сил:
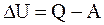
или
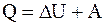 . (2.2.1)
. (2.2.1)
Уравнение (2.2.1) выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил.
Выражение (2.2.1) в дифференциальной форме будет иметь вид
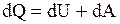
или в более корректной форме
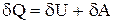 , (2.2.2)
, (2.2.2)
где dQ - бесконечно малое количество теплоты; dU - бесконечно малое изменение внутренней энергии системы; dА -элементарная работа. В выражении dU является полным дифференциалом, а dА и dQ таковыми не являются. В дальнейшем будем использовать запись первого начала термодинамики в форме (2.2.2).
Из формулы (2.2.2) следует, что в системе СИ количество теплоты выражается в тех же единицах, что работа и энергия, т.е. в джоулях (Дж).
Если система периодически возвращается в первоначальное состояние, то изменение ее внутренней энергии DU=0. Тогда, согласно первому началу термодинамики, А=Q, т.е. вечный двигатель первого рода - периодически действующий двигатель, который совершал бы большую работу, чем сообщенная ему извне энергия, - невозможен (одна из формулировок первого начала термодинамики).
 2015-06-04
2015-06-04 389
389







