1. Понятие об адиабатическом процессе. Первый закон термодинамики. Расчёт работы газа с помощью РV - диаграмм.
Адиабатический процесс
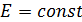
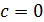
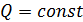
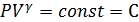
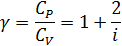
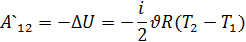

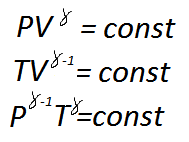
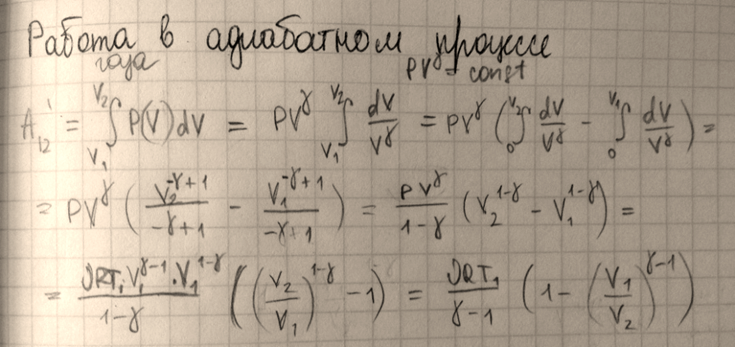
Для идеальных газов, чью теплоёмкость можно считать постоянной, в случае квазистатического процесса адиабата имеет простейший вид и определяется уравнением.
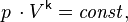
где 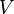 — его объём,
— его объём, 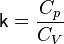 — показатель адиабаты,
— показатель адиабаты, 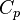 и
и 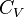 теплоёмкости газа соответственно при постоянном давлении и постоянном объёме.
теплоёмкости газа соответственно при постоянном давлении и постоянном объёме.
Один из методов для экспериментального определения показателя был предложен в 1819 г. Клеманом и Дезормом. Стеклянный баллон вместимостью несколько литров наполняется исследуемым газом при давлении 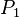 . Затем открывается кран, газ адиабатически расширяется, и давление падает до атмосферного —
. Затем открывается кран, газ адиабатически расширяется, и давление падает до атмосферного — 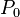 . Затем происходит его изохорное нагревание до температуры окружающей среды. Давление повышается до
. Затем происходит его изохорное нагревание до температуры окружающей среды. Давление повышается до 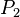 . В результате такого эксперимента k можно вычислить как.
. В результате такого эксперимента k можно вычислить как.
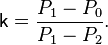
Первый закон термодинамики:
 2015-06-05
2015-06-05 460
460








