Основой масс-спектрометрии является разделение ионов по величинам m/z (отношение массы к заряду) и измерение количества (интенсивностей) ионов каждого типа. Метод позволяет определять молекулярную массу и молекулярную формулу вещества, расходуя очень маленькое (микро- или нанограммы) количество образца (метод разрушающего контроля). Кроме того, осколочные ионы несут полезную информацию о структуре изучаемого вещества.
При ионизации молекулы образуется молекулярный ион М+·, внутренняя энергия которого может быть достаточной для распада с выбросом нейтральной частицы m0 и образованием осколочного иона (фрагмента) А+:
М ® М+· ® А+ + m0.
Если осколочный ион А+ обладает достаточной внутренней энергией, то может происходить его дальнейший распад с образованием новых фрагментов.
Масс-спектр обычно представляют либо в нормализованной форме (в процентах от максимального, основного пика), либо в процентах от общего ионного тока в виде таблиц и графически (рис. 8.1).
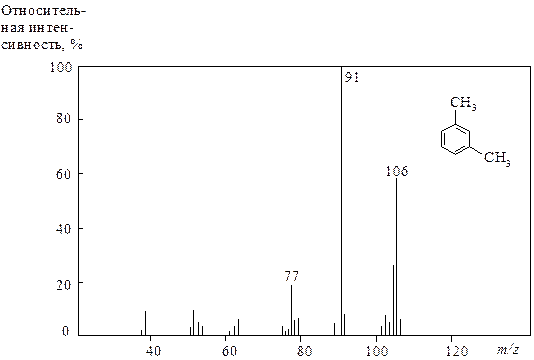 |
| Рис. 8.1. Масс-спектр м- ксилола в нормализованной форме (относительная интенсивность пика с т/z = 91 составляет 100%) |
Для получения спектра в процентах от общего ионного тока сумма интенсивностей пиков всех ионов принимается за меру общего ионного тока, относительный вклад каждого иона рассчитывается в процентах.
Обычно в масс-спектрометрии наблюдаются однозарядные положительные ионы, но иногда образуются ионы с двумя, тремя зарядами. Чаще всего такие ионы встречаются в масс-спектрах ароматических соединений:
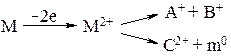
Масса двухзарядного иона в спектре равна m/2.
Кроме обычных узких пиков ионов, в масс-спектре часто наблюдаются уширенные пики низкой интенсивности, соответствующие метастабильным ионам. Их максимумам в спектре соответствуют, как правило, нецелочисленные значения m/z. Такие ионы широко используются для установления путей фрагментации. Если ион с массой m1 распадается с образованием иона с массой m2, то в спектре будет наблюдаться метастабильный ион m*= m22/ m1.
В атомной шкале масса 12С принята равной 12,0000, но другие элементы имеют нецелочисленные массы, например, масса 1Н равна 1,0078.
Разрешающая сила масс-спектрометра есть мера его способности разделять два иона с какой-либо определенной разницей масс. При низком разрешении масс-спектр состоит из ряда пиков с целочисленными значениями m/z. При сравнительно высоком разрешении пики могут быть расщеплены благодаря наличию ионов различного элементного состава.
Многие элементы имеют некоторое естественное содержание нескольких изотопов, и поскольку на масс-спектрометре измеряют отношение массы к заряду, эти изотопы проявляются в масс-спектре.
Для некоторых элементов, обычно встречающихся в масс-спектрометрии органических веществ, в табл. 8.1 дано приблизительное естественное содержание наиболее распространенных изотопов.
Следует отметить, что сера, хлор и бром имеют наиболее распространенные изотопы, отличающиеся на две массовые единицы. По этой причине хлор- и бромсодержащие соединения особенно легко распознать по масс-спектру. При этом из анализа изотопных пиков в области молекулярного иона можно определить число атомов хлора и брома в молекуле.
Таблица 8.1
Естественное содержание наиболее распространенных изотопов
элементов, обычно встречающихся в органической масс-спектрометрии
| Элемент | Изотоп (% естественного содержания) |
| Водород | 1Н (99,99) |
| Углерод | 12С (98,9) 13C (1,1) |
| Азот | 14N (99,6) 15N (0,4) |
| Кислород | 16O (99,8) 18O (0,2) |
| Фтор | 19F (100,0) |
| Кремний | 28Si (92,2) 29Si (4,7) 30Si (3,1) |
| Фосфор | 31P (100,0) |
| Сера | 32S (95,0) 33S (0,7) 34S (4,2) |
| Хлор | 35Cl (75,5) 37Cl (24,5) |
| Бром | 79Br (50,5) 81Br (49,5) |
| Иод | 127I (100,0) |
На рис. 8.2 показана область молекулярного иона в масс-спектре дихлорбензола. Главные пики, отстоящие друг от друга на две массовые единицы, соответствуют изотопам 35Cl и 37Cl, а меньшие пики обусловлены вкладом изотопа 13С. Обычно за молекулярный ион принимают пик с наименьшей изотопной массой. Здесь молекулярному иону соответствуют все шесть пиков.
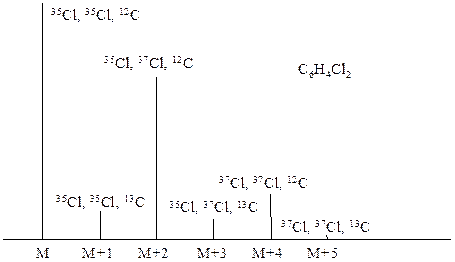 |
| Рис. 8.2. Изотопные вклады углерода и хлора в области молекулярного иона в масс-спектре дихлорбензола |
При интерпретации (расшифровки) масс-спектра если пик молекулярного иона имеет низкую интенсивность или его отнесение (распознание) вызывает затруднение, то подтвердить правильность отнесения можно с помощью методов мягкой ионизации (химической ионизации и т.д.), позволяющих обнаружить более интенсивные квазимолекулярные ионы.
С помощью масс-спектрометрии высокого разрешения можно определить молекулярную формулу исследуемого вещества путем точного определения массы молекулярного иона, изучения относительных интенсивностей в кластере пиков молекулярного иона и сравнения их со справочными данными, использования результатов других методов анализа. Молекулярный ион с четным значением m/z не содержит атомов азота или содержит их четное число. Молекула с четным числом атомов азота или фосфора или галогена содержит четное число атомов водорода. При нечетном числе атомов указанных элементов число атомов водорода также будет нечетным.
Интенсивность пика молекулярного иона и общая картина осколочных ионов в масс-спектре позволяют отнести исследуемое соединение к определенному классу. Спектр, содержащий много пиков осколочных ионов, интенсивность которых увеличивается в направлении уменьшения значений m/z, как правило, указывает на алифатический характер соединения, тогда как спектр с небольшим числом пиков, содержащий интенсивный пик молекулярного иона и пики двухзарядных ионов, обычно соответствует ароматической структуре.
На следующей стадии расшифровки масс-спектра следует выделить главные осколочные ионы и попытаться установить основные направления распада ионов. Нужно всегда иметь в виду возможность присутствия примесей. Наиболее распространенными загрязнениями являются фталатные пластификаторы (m/z 149, 167, 279) и силиконовая смазка (m/z 133, 207, 281, 355, 429).
Принципиальная блок-схема прибора представлена на рис. 8.3. В системе прибора от ввода пробы до регистрации ионов включительно поддерживается вакуум.
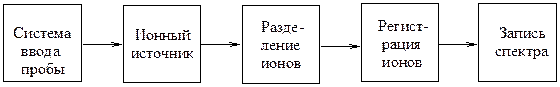 |
| Рис. 8.2. Принципиальная схема масс-спектрометра |
Ввод пробы возможен путем непосредственного ввода в ионный источник на конце металлического стержня (зонда), а также из колонки газового или жидкостного хроматографа. В случае сочетания масс-спектрометра с хроматографом требуется при помощи вакуумного насоса удалять из камеры ионизации газ-носитель (если ввод производится из колонки газового хроматографа) или элюент, который предварительно распыляют при нагревании, для испарения растворителя (если ввод производится из колонки жидкостного хроматографа).
Наиболее распространенный метод ионизации – это ионизация электронным ударом, заключающаяся в воздействии на изучаемое вещество (обычно при давлении около 10-6 мм рт. ст.) пучка электронов. Источником электронов служит нагретая катодная нить (чаще всего вольфрамовая). Электроны ускоряются в электрическом поле, создающемся в ионном источнике между катодом и анодом, разность потенциалов между которыми обычно составляет около 70 эВ. При такой энергии обычно образуются многочисленные осколочные ионы, полезные с точки зрения выяснения строения изучаемого соединения. При электронном ударе в вакууме образуются как положительно, так и отрицательно заряженные ионы. В большинстве случаев масс-спектры с ионизацией электронным ударом регистрируют в режиме положительных ионов, которые образуются в большем количестве.
Существует также режим химической ионизации, при которой масс-спектры содержат меньше осколочных ионов, чем при ионизации электронным ударом. Химическая ионизация позволяет обнаружить молекулярные ионы, иногда отсутствующие в масс-спектрах с ионизацией электронным ударом. При химической ионизации исследуемое вещество (парциальное давление которого в ионном источнике составляет около 10-4 мм рт. ст.) смешивают в ионном источнике с газом-реагентом, находящимся в большом избытке (парциальное давление около 1 мм рт. ст.). Чаще всего в качестве газов-реагентов применяют метан, изобутан или аммиак. Смесь исследуемого вещества и газа-реагента подвергают электронному удару. При этом сначала ионизируются находящиеся в избытке молекулы газа-реагента, например, из метана образуются ионы СН4+· и СН3+. Поскольку давление газа-реагента довольно велико, то обычно в ионном источнике осуществляются ион-молекулярные реакции, приводящие к образованию вторичных ионов с небольшим избытком внутренней энергии:
СН4+· + СН4 ® СН5+ + СН3·
СН3+ + СН4 ® С2Н5+ + Н2 .
Образовавшиеся в большом количестве вторичные ионы сталкиваются с молекулами изучаемого вещества и ионизируют их. Ионизация обычно осуществляется путем протонирования:
М + СН5+ ® [М + Н]+ + СН4.
Образующиеся так называемые квазимолекулярные ионы [М + Н]+ имеют четное число электронов и, следовательно, должны быть более устойчивыми, чем возникающие при электронном ударе молекулярные ион-радикалы. Сочетание большей устойчивости с низкой избыточной внутренней энергией приводит к тому, что в масс-спектрах с химической ионизацией квазимолекулярные ионы имеют весьма высокую интенсивность.
Ионы разделяют в соответствии с их отношением массы к заряду (m/z) в магнитном и (или) электрическом полях. Сочетание электрического и магнитного анализаторов дает масс-спектрометр с двойной фокусировкой, так как пучок ионов из ионной камеры сначала разделяется по кинетической энергии с помощью электрического поля, а затем ионы попадают в магнитное поле, напряженность которого изменяется таким образом, чтобы каждый ион с определенным значением m/z фокусировался на коллекторе ионов по очереди.
В масс-спектрометрах с квадрупольным анализатором разделение ионов осуществляется с помощью электронного фильтра, который представляет собой четыре стержнеобразных электрода. При подходящем радиочастотном поле между электродами пропускается только ион с определенной массой и предотвращается прохождение всех остальных ионов. Благодаря такому фильтрующему действию квадруполь часто называют фильтром масс.
Регистрация масс-спектра может проводиться при помощи диодной матрицы, электрический сигнал с которой направляется на компьютер, производящий запись спектра.
Масс-спектроскопия используется в основном в химии нефти. По массе молекулярного иона можно с большой точностью определить молекулярную массу углеводорода или гетероатомного соединения, выделенного из нефти, элементный состав вещества и качественный состав углеводородных смесей.
Количественный анализ сложных смесей проводится в основном методом хромато-масс-спектрометрии. В этом случае используется блок из масс-спектрометра с газовым или жидкостным хроматографом, производящим разделение индивидуальных веществ. Далее вещества по очереди поступают в масс-спектрометр, который в данном случае можно рассматривать в качестве хроматографического детектора. Полученный масс-спектр можно обработать на ЭВМ, идентифицируя вещество и определяя его количественные характеристики.
 2015-06-28
2015-06-28 1710
1710






