Круговым процессом (или циклом) называется процесс, при котором система, пройдя через ряд состояний, возвращается в исходное. Если за цикл совершается положительная работа  (цикл протекает по часовой стрелке), то он называется прямым; если за цикл совершается отрицательная работа
(цикл протекает по часовой стрелке), то он называется прямым; если за цикл совершается отрицательная работа 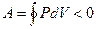 (цикл протекает против часовой стрелки), то он называется обратным.
(цикл протекает против часовой стрелки), то он называется обратным.
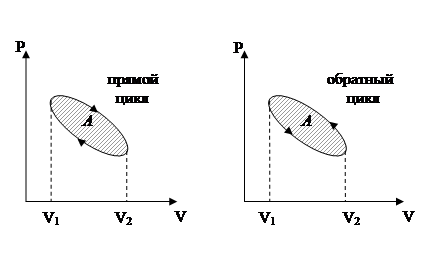
Прямой цикл используется в тепловых двигателях, обратный – в холодильных установках.
Термодинамический процесс называется обратимым, если его одинаково легко можно провести как в прямом, так и в обратном направлении; в каждом из этих случаев
система проходит через одни и те же промежуточные состояния; после проведения прямого и обратного процесса система и окружающие её тела возвращаются в исходное состояние.
Второе начало термодинамики из анализа работы тепловых и холодильных установок:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Приведенное количество теплоты – это отношение теплоты dQ, сообщаемое телу на бесконечно малом участке процесса, к температуре T теплоотдающего тела.
Энтропия S – это функция состояния, приращение которой определяется суммой приведенных количеств теплот.
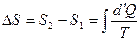
Второе начало термодинамики: энтропия изолированной системы не может убывать, она остается постоянной, если процессы, протекающие в системе обратимые, и возрастает, если процессы необратимые:
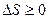
Энтропия связана с термодинамической вероятностью состояния систем. Термодинамическая вероятность W состояния системы – это число способов, которыми может быть реализовано данное состояние системы, или число микросостояний, осуществляющих данное макросостояние (по определению 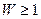 ).
).
Согласно Больцману, энтропия и термодинамическая вероятность связаны между собой следующим образом:
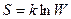 ,
,
где k – постоянная Больцмана. Эта формула позволяет дать энтропии следующее статистическое толкование: энтропия является мерой неупорядоченности системы.
Второе начало термодинамики, отражая его статистический смысл, может быть сформулировано: наиболее вероятными являются процессы, протекающие с возрастанием энтропии.
Третье начало термодинамики (теорема Нернста): при стремлении абсолютной температуры к нулю энтропия любой системы стремится к нулю.
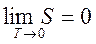
 2015-07-21
2015-07-21 540
540








