Для построения градуировочного графика в 5 мерных колб вместимостью 100 см3 вводят 2,0 см3 раствора хлорида бария и хлороводородной кислоты, разбавляют небольшим объёмом дистиллированной воды, прибавляют по 3,30 см3 раствора желатины. В колбы последовательно добавляют 3, 5, 10, 15 и 20 см3 стандартного раствора серной кислоты, дистиллированною воду до метки и перемешивают. Получают серию мутных растворов, содержащих в 100 см3 соответственно 0,15; 0,25; 0,50; 0,75 и 1,00 мг ионов SO42-. Через 10 мин растворы поочерёдно помещают в кювету и снимают показания прибора; контроль – анализируемая питьевая вода без добавления реактивов.
По полученным данным строят градуировочный график в координатах: содержание SO42-, мг/100 см3 – показания прибора.
В мерную колбу вместимостью 100 см3 помещают по 2,0 см3 раствора хлорида бария и хлороводородной кислоты, разбавляют небольшим объёмом дистиллированной воды, добавляют 3,0 см3 раствора желатины, 25,0 см3 анализируемой питьевой воды, доводят до метки дистиллированной водой, перемешивают. Через 10 мин помещают раствор в кювету и снимают показания шкалы прибора. По градуировочному графику находят содержание SO42- в пробе.
Содержание SO42- в 1000 см3 анализируемой питьевой воды (Q мг/1000 см3) рассчитывают по формуле
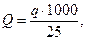 (15)
(15)
где q – найденное по градуировочному графику количество SO42-, мг; 28 – объём анализируемой питьевой воды, см3.
Контрольные вопросы и задания
1. Составить уравнение реакции получения сульфатов.
2. С какой целью применяются защитные коллоиды при определении сульфатов?
3. Как выбирают длину волны при измерении оптической плотности суспензии сульфата бария?
4. С какой целью в анализируемую воду добавляют хлороводородную кислоту?
5. Какие правила необходимо соблюдать при фототурбидиметрическом измерении оптической плотности?
 2015-07-14
2015-07-14 569
569








