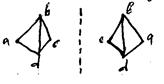
 Оптическая: Вещество имеющие предельные углеродные атом, существуют в двух структурно одинаковых стериоизомерных формах. Они одинаковы по физ. и хим. св-вам и отличаются лишь в двух свойствах: 1)кристаллизуются в формах, не имеющих плоскости симметрии и относящихся друг к другу, как предмет к своему зеркальному отражению. 2) оба стереоизомера по разному относятся к поляризованному свету. При прохождении луча поляризованного света ч/з «оптически активную» среду плоскость поляризации света поворачивается (вокруг оси луча) на угол, пропорциональный длине слоя оптически активного вещества.
Оптическая: Вещество имеющие предельные углеродные атом, существуют в двух структурно одинаковых стериоизомерных формах. Они одинаковы по физ. и хим. св-вам и отличаются лишь в двух свойствах: 1)кристаллизуются в формах, не имеющих плоскости симметрии и относящихся друг к другу, как предмет к своему зеркальному отражению. 2) оба стереоизомера по разному относятся к поляризованному свету. При прохождении луча поляризованного света ч/з «оптически активную» среду плоскость поляризации света поворачивается (вокруг оси луча) на угол, пропорциональный длине слоя оптически активного вещества.
Проекция Фишера:
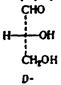
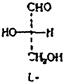
D,L– номенклатура:D–правовращ.,L–левовращ. мол-ла.
Если путём хим превращений, не затрагивая ассиметрический центр, получили глиц. альдегид. И если он вращается по часовой стрелке плоскополяр-й свет, то его называют D-изомером, если против часовой –L.
Абсолютная номенклатура: пусть глаз человека смотрит вдоль связи С-младший заместитель. Если старшинство заместителей убывает по часовой стрелке, то R–изомер, против S-изомер. Использую проекцию Фишера, путём чётного числа перестановок младший заместитель поместить вниз.
|
|
|
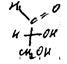
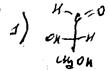
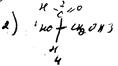
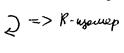
Мезоформа–обозначает охиральный диастереоизоме, не имеющий энантиомер:
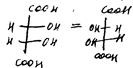
Диастереомер– пространственные изомеры, отличающиеся м/у собой конфигурацией одного и того же хирального центра, но сходные по конфигурации других хиральных центров: Диастериомеры– стереоизомеры, не являются энантиомерами. Энантиомеры– любая пара оптических изомеров, относящихся друг к другу как предмет и его зеркальное изображение.
Рацимат –смесь равных количеств энантиомеров.
Хиральность– св-во объекта бать несовместимым со своим зеркальным отображением. Является необходимым условием оптической активности молекул. Хиральные молекулы хар-ся отсутствием плоскости симметрии.
1) при наличии заместителей в положении 2, 2’ и 6, 6’ –из-за стерических препятствий происходит поворот по связи 1-1’ и циклы ориентируются почти ┴ друг к другу.
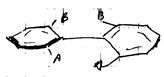
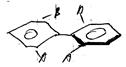
2) азотсодержащие соединения 

62.Класификация и номенклатура органических соединений. Номенклатура ИЮПАК. Классификация органических реакций и реагентов.
I)По расположению углеродных атомов в молекуле:
1)соединения с открытой(ацеклической) цепью атомов углерода: СН3-СН3, СН3СН2СН3, СН2=СН2 и т.д.
2) карбоциклические соединения с циклами из С
2.1)алициклческие

2.2)ароматические: бензол
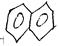
3)гетероциклические, содержащие гетероатом (O, N, S..)
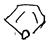
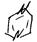
II) по хар-ским струк. Элементам
а) галогенпроизводные
б) спирты и фенолы
в) альдегиды (R-C(=O)-H)
г) кетоны (R1-C(=O)-R2)
д) карбоновые кислоты (R-COOH)
|
|
|
Классификация хим. реакций:
1) изменение структуры элементов:
1.1)замещение (S)
2.2)присоединение(В)
2.3)элиминирование(Е)
2.4)перегруппировка(R)
2.5)внедрение
2) природа реог-х в-в:
2.1) электрофильные
2.2) нуклеофильные
2.3) свободнорадикальные
2.4) перициклические
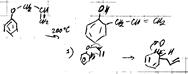
2) по изменению скелета
3.1)конденсация
3.2)перегруппировка
4)окисл-востан р-ции
Примеры:
Электрофильное замещение (п-комплекс)
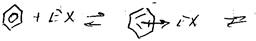

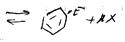
Нуклеофильное замещение
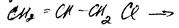
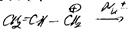
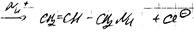 SN(1)
SN(1)
Свободнорадикальные:
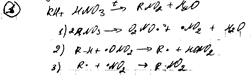
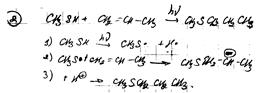
Перегруппировка Бекхмана:

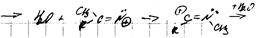
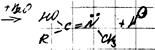 по проавилу Эйлера
по проавилу Эйлера 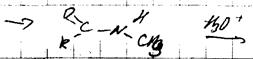
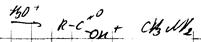
Альдольнокротоновая конденсация
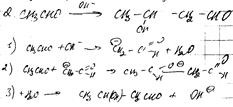
Номенклатура.
Тривиальная– не имеет научной основы. Названия случайны, обусловлены методом синтеза, происхождением, от автора. Не дают представление о структуре.
Рациональная– основа теория типов, за основу берут название первого члена гомологического ряда. Остальные соединения рассматриваются как производные этого гомолога.
Женевская– (1889г.) логично и тесно связана с научной систематикой хим соединений. Основа названия – нормальный углеводород, содержащий то же число атомов, что и наиболее длинная углеродная цепь. Приставки и окончания показывают наличие заместителей, кратных связей.
ИЮПАК– смесь старых и новых названий.
1) заместительная система– основана на выражении характеристических групп (F, Cl, I, NO, NO2, -OR, -SR) с помощью приставок (с умножающим приставками и цифровыми указателями). Другие группы м/б обозначены как суффиксами, так и приставками. Если в соединении неск-ко хар-х групп (не указанных выше), то обозначают старшую.
2) радикально-заместительная – в основе названия лежит наименование функц. группы (функции), к к–рому присоединяют наименование орг. радикала, напр, СН2СНС1 — винилхлорид, PhCOOH — фенилкарбоновая к-та;
3)заменительная– для соединений с гетероатомами. Они рр-ся как производные их углеводородных аналогов, образованные заменой ат. углерода гетероатомом. Для последних применяют корни их латинских наименований с окончанием «а», напр. Н3С—О—СН2—СН2—NH—CH2—СН3 — 2-окса-5-азагептап.
 2015-08-12
2015-08-12 1582
1582








