1. Молярная масса вещества в системе СИ имеет размерность:
1) кг∙моль; 2) кг∙моль-1; 3) кг∙м-3; 4) кг∙м∙моль-1; 5) кг∙м-3∙моль.
2. По какой из приведенных ниже формул можно правильно рассчитать давление газа через его температуру Т и концентрацию молекул 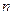 ? (
? (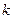 - постоянная Больцмана).
- постоянная Больцмана).
1) 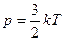 ; 2)
; 2) 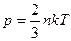 ; 3)
; 3) 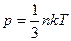 ; 4)
; 4) 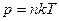 ; 5)
; 5) 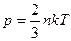 .
.
3. Металлический стержень внесли с мороза в комнату. При этом его температура повысилась на
300 С. По абсолютной шкале температуры стержень нагрелся на:
1) 303 К; 2) 243 К; 3) 30 К; 4) 15 К; 5) 60 К.
4. Если 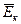 - средняя кинетическая энергия поступательного движения одной молекулы газа, а
- средняя кинетическая энергия поступательного движения одной молекулы газа, а 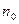 - концентрация молекул, то основное уравнение молекулярно – кинетической теории идеальных газов может быть записано в виде:
- концентрация молекул, то основное уравнение молекулярно – кинетической теории идеальных газов может быть записано в виде:
1) 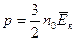 ; 2)
; 2) 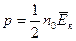 ; 3)
; 3) 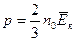 ; 4)
; 4) 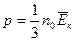 ; 5)
; 5) 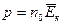 .
.
5. В сосуде закрытом подвижным поршнем находится газ. Какой из графиков правильно отражает зависимость концентрации молекул газа от объема?
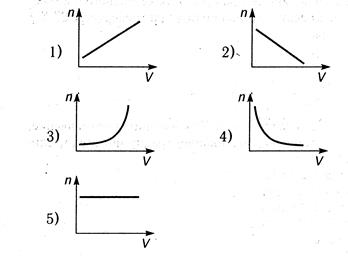
6. Какой из графиков правильно отражает зависимость плотности газа от концентрации его молекул?
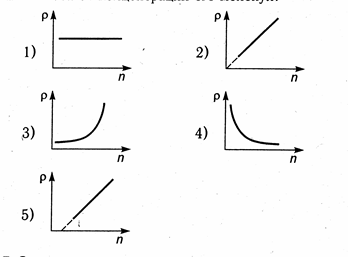
7. Средняя кинетическая энергия поступательного движения молекулы идеального газа равна
6∙10-21 Дж. Определите концентрацию молекул газа, если он находится в сосуде под давлением
2∙105 Па.
1) 1∙1025 м-3; 2) 2∙1025 м-3; 3) 3∙1025 м-3; 4) 4∙1025 м-3; 5) 5∙1025 м-3.
8. Чему равна средняя кинетическая энергия хаотичного поступательного движения молекул идеального газа при температуре 270 С?
1) 6,2∙10-21 Дж; 2) 4,1∙10-21 Дж; 3) 2,8∙10-21 Дж; 4) 0,6∙10-21 Дж; 5) 0,4∙10-21 Дж.
9. В сосуде находится идеальный газ. Как изменится его давление, если и абсолютная температура, и концентрация молекул увеличатся на 20 %?
1) возрастет в 1,2 раза; 2) понизится в 1,2 раза; 3) возрастет в 1,44 раза;
4) понизится в 1,44 раза; 5) не изменится.
10. Если М – молярная масса, 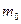 - масса молекулы, а
- масса молекулы, а 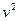 - средний квадрат скорости молекул идеального газа, имеющего температуру
- средний квадрат скорости молекул идеального газа, имеющего температуру 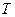 и давление
и давление 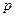 , то концентрация молекул этого газа может быть вычислена по формуле:
, то концентрация молекул этого газа может быть вычислена по формуле:
1) 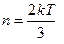 ; 2)
; 2) 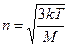 ; 3)
; 3) 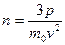 ; 4)
; 4) 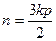 ; 5)
; 5) 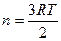 .
.
11. Число молекул в 1 м3 кислорода при нормальных условиях равно (молярная масса кислорода М, число Авогадро NА, плотность кислорода при нормальных условиях 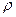 ):
):
1) 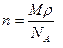 ; 2)
; 2) 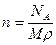 ; 3)
; 3) 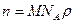 ; 4)
; 4) 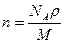 ; 5)
; 5) 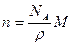 .
.
12. Найдите массу молекулы азота (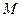 =0,028 кг/моль):
=0,028 кг/моль):
1) 2,8∙10-26 кг; 2) 4,7∙10-26 кг; 3) 5,6∙10-26 кг; 4) 9,4∙10-26 кг; 5) 1,4∙10-26 кг.
13. Какое количество вещества содержится в алюминиевой ложке массы 27 г? Относительная атомная масса алюминия равна 27.
1) 1 моль; 2) 2,5 моль; 3) 5 моль; 4) 10 моль; 5) 25 моль.
14. Определите число молекул, содержащихся в 64 г кислорода, молярная масса которого равна 0,032 кг/моль.
1) 3∙1023; 2) 6∙1023; 3) 12∙1023; 4) 16∙1023; 5) 24∙1023.
15. За 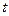 =10 суток полностью испарилось из стакана
=10 суток полностью испарилось из стакана 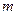 =100 г воды. Сколько в среднем вылетало молекул с поверхности воды за
=100 г воды. Сколько в среднем вылетало молекул с поверхности воды за 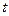 =1 с?
=1 с?
1) 3,9∙1018; 2) 7,8∙1018; 3) 3,9∙1016; 4) 5,4∙1017; 5) 7,8∙1017.
16. Сколько молекул содержится в стакане воды? (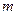 =200 г,
=200 г, 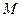 =0,018 кг/моль)
=0,018 кг/моль)
1) 0,67∙1025; 2) 0,67∙1022; 3) 1,5∙1025; 4) 1,5∙1022; 5) 6∙1025.
17. Количество вещества, находящееся в железной отливке объемом 28∙10-3 м3, равно (относительная атомная масса железа 56, плотность железа 7,8∙103 кг/м3):
1) 218,4 кг; 2) 1800 моль; 3) 436,8 кг; 4) 3900 моль; 5) 23,5∙1026 молекул.
18. Если концентрация молекул кислорода (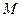 =32∙10-3 кг/моль) в сосуде вместимостью 5 л равна 9,41∙1023 м3, то масса газа в сосуде равна:
=32∙10-3 кг/моль) в сосуде вместимостью 5 л равна 9,41∙1023 м3, то масса газа в сосуде равна:
1) 0,25 г; 2) 0,36 г; 3) 0,82 г; 4) 1,25 г; 5) 2,16 г.
19. Определите концентрацию молекул водорода, находящегося под давлением 2,67∙104 Па, если средний квадрат скорости поступательного движения молекул при этих условиях равен
4∙106 м2/с2. (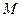 =0,002 кг/моль):
=0,002 кг/моль):
1) 3,0∙1024 м-3; 2) 6,0∙1024 м-3; 3) 12,0∙1024 м-3; 4) 24,0∙1024 м-3; 5) 36,0∙1024 м-3.
20. Если в сосуде вместимостью 1 м3 находится 1,2 кг идеального газа при давлении 105 Па, то средняя квадратичная скорость молекул газа равна:
1) 200 м/с; 2) 300 м/с; 3) 400 м/с 4) 500 м/с; 5) 600 м/с.
21. При увеличении средней квадратичной скорости молекул идеального газа в два раза и уменьшении концентрации молекул в два раза давление газа:
1) увеличится в 4 раза; 2) увеличится в 2 раза; 3) уменьшится в 2 раза;
4) увеличится в 8 раз; 5) не изменится.
22. Если в сосуде при давлении 105 Па плотность идеального газа составляет 1,2 кг/м3, то средняя квадратичная скорость молекул этого газа равна:
1) 160 м/с; 2) 250 м/с; 3) 300 м/с 4) 450 м/с; 5) 500 м/с.
23. Плотность идеального газа в сосуде равна 1,2 кг/м3. Если средняя квадратичная скорость молекул газа равна 500 м/с, то газ находится под давлением:
1) 104 Па; 2) 2∙104 Па; 3) 105 Па; 4) 5∙105 Па; 5) 106 Па.
24. Средняя квадратичная скорость молекул кислорода при 9270 С равна 960 м/с. Какова средняя квадратичная скорость этих молекул при температуре газа 270 С?
1) 200 м/с; 2) 824 м/с; 3) 320 м/с 4) 480 м/с; 5) 560 м/с.
25. Молекулы водорода (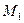 =2 г/моль) при температуре 150 С имеют такую же среднеквадратичную скорость, как и молекулы гелия (
=2 г/моль) при температуре 150 С имеют такую же среднеквадратичную скорость, как и молекулы гелия (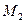 =4 г/моль) при температуре, равной:
=4 г/моль) при температуре, равной:
1) 281 К; 2) 303 К; 3) 436 К; 4) 481 К; 5) 576 К.
26. Ядра атомов гелия состоят из двух протонов и двух нейтронов. Если гелий находится при нормальных условиях, то средняя квадратичная скорость его атомов равна:
1) 0,8∙103 м/с; 2) 1,3∙103 м/с; 3) 1,5∙103 м/с; 4) 1,8∙103 м/с; 5) 2,0∙103 м/с.
27. Если при увеличении абсолютной температуры идеального газа в 2 раза его давление увеличилось на 25 %, то объем этого газа заданной массы:
1) уменьшился в 1,6 раза; 2) увеличится в 1,6 раза; 3) уменьшился в 2 раза;
4) увеличился в 2 раза; 5) не изменился.
28. Как изменится температура идеального газа, если уменьшить его объем в два раза при осуществлении процесса, в котором давление и объем газа связаны соотношением 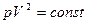 ?
?
1) увеличился в 2 раза; 2) увеличится в 4 раза; 3) не изменился;
4) уменьшился в 2 раза; 5) уменьшится в 4 раза.
29. Если баллон, содержащий 12 л кислорода при давлении 1 МПа, соединить с пустым баллоном вместимости 3 л, то в процессе изотермического расширения газа в сосудах установится давление, равное:
1) 4,0 МПа; 2) 0,8 МПа; 3) 0,6 МПа; 4) 0,4 МПа; 5) 0,2 МПа.
30. Баллон с воздухом соединяют с тремя одинаковыми сосудами, из которых воздух выкачан. Как изменится давление в баллоне, если процесс проходил при постоянной температуре, а объем каждого сосуда равен объему баллона?
1) уменьшился в 1 раз; 2) уменьшится в 2 раза; 3) уменьшится в 3 раза;
4) уменьшится в 4 раза; 5) уменьшится в 5 раз.
31. Некоторую массу идеального газа сжимают изотермически от объема 3 л до объема 1 л. Давление при этом возрастает на 2∙105 Па. Первоначальное давление газа было равно:
1) 5∙105 Па; 2) 4∙105 Па; 3) 3∙105 Па; 4) 2∙105 Па; 5) 1∙105 Па.
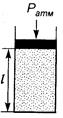 32. Идеальный газ находится в цилиндре и заперт тяжелым поршнем, который может перемещаться без трения. При температуре 270 С поршень находится на расстоянии
32. Идеальный газ находится в цилиндре и заперт тяжелым поршнем, который может перемещаться без трения. При температуре 270 С поршень находится на расстоянии 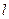 =30 см от дна цилиндра. На каком расстоянии от дна сосуда будет находится поршень, если газ нагреть до температуры 1270 С?
=30 см от дна цилиндра. На каком расстоянии от дна сосуда будет находится поршень, если газ нагреть до температуры 1270 С?
1) 70 см; 2) 60 см; 3) 50 см; 4) 40 см; 5) 30 см.
33. При изотермическом сжатии газа его объем уменьшился на 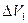 =1 л, а давление возросло на 20 %. Если при той же температуре первоначальный объем газа изотермически уменьшить на
=1 л, а давление возросло на 20 %. Если при той же температуре первоначальный объем газа изотермически уменьшить на 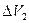 =2 л, то давление увеличится на:
=2 л, то давление увеличится на:
1) 100 %; 2) 75 %; 3) 60 %; 4) 50 %; 5) 40 %.
34. На какой глубине пузырьки воздуха имеют радиус, вдвое меньший, чем у поверхности воды? Атмосферное давление 105 Па, плотность воды 103 кг/м3. Температура воздуха постоянна.
1) 30 м; 2) 40 м; 3) 55 м; 4) 70 м; 5) 80 м.
35. Открытая с обоих концов трубка наполовину погружена в ртуть. Верхнее отверстие трубки плотно закрывают и вынимают трубку из ртути. В трубке остается столбик ртути, который занимает четверть ее длины. Если плотность ртути 13,6 г/см3, а длина трубки 1 м, то атмосферное давление равно… кПа.
36.Трубку длиной 57 см, закрытую с одного конца, погружают открытым концом в ртуть. Если атмосферное давление равно 760 мм. рт. ст., то длина столбика воздуха в трубке в тот момент, когда ее верхний конец сравняется с уровнем ртути, будет равна:
1) 9,5 см; 2) 19,0 см; 3) 28,5 см; 4) 38,0 см; 5) 47,5 см.
37. Запаянная с одного конца трубка длиной 25 см погружена открытым концом в ртуть на 1/3 ее длины так, что уровень ртути в трубке совпадает с уровнем ртути в сосуде. До какой температуры надо нагреть воздух в трубке, чтобы из нее вышла вся ртуть? Атмосферное давление равно 760 мм. рт. ст., начальная температура воздуха 270 С. Изменением уровня ртути в сосуде пренебречь.
1) 1270 С; 2) 1770 С; 3) 2270 С; 4) 2770 С; 5) 3270 С.
38. Чтобы при изобарном нагревании воздуха его объем увеличился вдвое по сравнению с объемом при 00 С, температуру газа нужно:
1) уменьшить на 2000С; 2) увеличить на 2000С; 3) увеличить на 2730С;
4) увеличить на 3720С; 5) увеличить на 5460С.
39. Некоторая масса идеального газа нагревается при постоянном давлении от температуры 270 С до температуры 1270 С. Объем газа при этом увеличился на 1 л. В первоначальном состоянии газ занимал объем, равный:
1) 1 л; 2) 2 л; 3) 3 л; 4) 4 л; 5) 5 л.
40. В изохорном процессе давление идеального газа увеличивается на 5∙104 Па. На сколько увеличится при этом температура газа, если первоначальное давление было 2∙105 Па, а первоначальная температура газа равна 300 К? Масса газа остается неизменной.
1) 150 К; 2) 125 К; 3) 100 К; 4) 75 К; 5) 50 К.
41. Некоторая масса идеального газа нагревается изохорно от температуры 270 С до температуры 1270 С. Давление газа при этом возросло на 4∙104 Па. Первоначальное давление газа равно:
1) 4∙104 Па; 2) 8∙104 Па; 3) 12∙104 Па; 4) 16∙104 Па; 5) 2∙105 Па.
42. Идеальный газ с абсолютной температурой 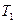 , занимавший при давлении р1 =4∙105 Па объем
, занимавший при давлении р1 =4∙105 Па объем 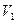 =3 л, изотермически расширяется до объема
=3 л, изотермически расширяется до объема 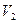 =12 л. Затем при изохорическом нагревании его давление и абсолютная температура становятся равными р2 =2∙105 Па и Т2 соответственно. Отношение Т2/Т1 равно:
=12 л. Затем при изохорическом нагревании его давление и абсолютная температура становятся равными р2 =2∙105 Па и Т2 соответственно. Отношение Т2/Т1 равно:
1) 1; 2) 2; 3) 3; 4) 4; 5) 6.
43. Горизонтально расположенный закрытый цилиндрический сосуд с гладкими стенками разделен тонким подвижным теплопроводящим поршнем на две части, в которых находятся равные массы различных идеальных газов: в одной части газ с молярной массой М1 в другой – с молярной массой М2. Какую часть объема сосуда занимает газ с молярной массой 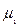 при равновесном положении поршня?
при равновесном положении поршня?
1) 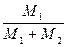 ; 2)
; 2) 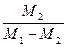 ; 3)
; 3) 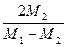 ; 4)
; 4)  ; 5)
; 5) 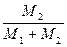 .
.
44. Закрытый горизонтальный цилиндр с гладкими стенками разделен на две части подвижным тонким поршнем. Слева от поршня в цилиндре имеется некоторое количество газа при температуре 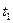 =-73 0С, а справа от поршня – такое же количество этого газа при температуре
=-73 0С, а справа от поршня – такое же количество этого газа при температуре
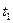 =-27 0С. Поршень находится в равновесии. Если общий объем цилиндра 500 см3, то объем, занимаемый газом в левой части цилиндра, равен:
=-27 0С. Поршень находится в равновесии. Если общий объем цилиндра 500 см3, то объем, занимаемый газом в левой части цилиндра, равен:
1) 0,5∙10-4 м3; 2) 2∙10-4 м3; 3) 1∙10-3 м3; 4) 2,5∙10-3 м3; 5) 5∙10-3 м3.
45. Горизонтально расположенный закрытый цилиндрический сосуд длины 0,6 м с гладкими стенками, разделенный на две части легким теплонепроницаемым поршнем, заполнен идеальным газом. В начальный момент объем левой части сосуда вдвое больше объема правой, а температура газа в обеих частях одинакова. Если температуру газа в правой части увеличить вдвое, а в левой поддерживать постоянной, то поршень переместится на:
1) 0,05 м; 2) 0,10 м; 3) 0,15 м; 4) 0,20 м; 5) 0,25 м.
46. Теплоизолированный сосуд разделен теплопроводной неподвижной перегородкой на две части: объем первой части сосуда в 3 раза меньше объема второй части сосуда. В первой части сосуда находится 14 г азота (молярная масса азота 28∙10-3 кг/моль), а во второй – 4 г гелия (молярная масса гелия 4∙10-3 кг/моль). Отношение давления азота к давлению гелия после установления теплового равновесия равно:
1) 0,17; 2) 0,67; 3) 1,5; 4) 4,5; 5) 6,0.
47. Давление газа р, абсолютная температура Т, молярная масса М. При этом плотность данного газа, выраженная через заданные величины, равна (R – газовая постоянная):
1) 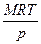 ; 2)
; 2) 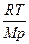 ; 3)
; 3) 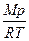 ; 4)
; 4) 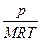 ; 5)
; 5) 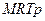 .
.
48. Плотность газа 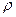 , абсолютная температура Т, молярная масса М. Давление данного газа, выраженное через данные величины, равно (R – газовая постоянная):
, абсолютная температура Т, молярная масса М. Давление данного газа, выраженное через данные величины, равно (R – газовая постоянная):
1) 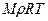 ; 2)
; 2) 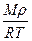 ; 3)
; 3) 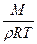 ; 4)
; 4) 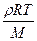 ; 5)
; 5) 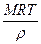 .
.
49. Какое количество молей 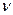 идеального газа может находиться в сосуде объемом
идеального газа может находиться в сосуде объемом 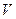 при давлении р и температуре Т? (R – газовая постоянная, k – постоянная Больцмана):
при давлении р и температуре Т? (R – газовая постоянная, k – постоянная Больцмана):
1) 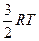 ; 2)
; 2) 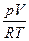 ; 3)
; 3) 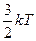 ; 4)
; 4) 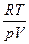 ; 5)
; 5)  .
.
50. Каково давление воздуха (М =29∙10-3 кг/моль) в камере сгорания дизельного двигателя при температуре 503 0С, если плотность воздуха равна 1,8 кг/м3?
1) 400 кПа; 2) 4∙106 Па; 3) 40 кПа; 4) 4000 Па; 5) 40 Па.
51. Для того, чтобы плотность идеального газа при неизменном давлении увеличилась в два раза, абсолютную температуру газа следует:
1) увеличить в 2 раза; 2) увеличить в 4 раза; 3) увеличить в  раз;
раз;
4) уменьшить в 2 раза; 5) уменьшить в 4 раза.
52. Чему равна плотность азота (М =28∙10-3 кг/моль) при температуре 47 0С и давлении 1 МПа?
1) 5,2 кг/м3; 2) 7,3 кг/м3; 3) 10,5 кг/м3; 4) 14,0 кг/м3; 5) 28,0 кг/м3.
53. Молярная масса водорода М =2∙10-3 кг/моль. При нормальных условиях (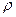 =105 Па, t0 =0 0С) плотность водорода равна:
=105 Па, t0 =0 0С) плотность водорода равна:
1) 0,02 кг/м3; 2) 0,04 кг/м3; 3) 0,09 кг/м3; 4) 0,86 кг/м3; 5) 1,26 кг/м3.
54. Баллон содержит идеальный газ при температуре 27 0С и давлении 200 кПа. Из баллона выпустили 80 % газа и охладили его до температуры 12 0С. В баллоне установилось давление:
1) 38 кПа; 2) 152 кПа; 3) 94 кПа; 4) 72 кПа; 5) 76 кПа.
55. Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40 %, а абсолютная температура – на 20 %. Какая часть газа осталась в сосуде?
1) 0,85; 2) 0,75; 3) 0,65; 4) 0,50; 5) 0,25.
 56. В баллоне, закрытом вентилем, находился некоторый газ. После того, как вентиль открыли, а затем снова закрыли, температура уменьшилась в 4 раза, а давление – в 5 раз. Какая часть газа (в процентах) была выпущена из баллона?
56. В баллоне, закрытом вентилем, находился некоторый газ. После того, как вентиль открыли, а затем снова закрыли, температура уменьшилась в 4 раза, а давление – в 5 раз. Какая часть газа (в процентах) была выпущена из баллона?
1) 20; 2) 40; 3) 60; 4) 64; 5) 80.
57. На диаграмме 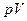 изображены процессы перевода некоторой неизменной массы идеального газа из состояния 1 в состояние 3. Начальная (Т1) и конечная (Т3) температуры газа связаны между собой соотношением:
изображены процессы перевода некоторой неизменной массы идеального газа из состояния 1 в состояние 3. Начальная (Т1) и конечная (Т3) температуры газа связаны между собой соотношением:
1) 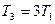 ; 2)
; 2) 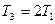 ; 3)
; 3) 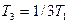 ; 4)
; 4) 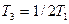 ; 5)
; 5)  .
.
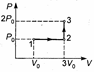 58. Постоянную массу идеального газа переводят из состояния 1 в состояние 3., как показано на рисунке. Если в состоянии 1 температура газа была равна 100 К, то в состоянии 3 она станет равной:
58. Постоянную массу идеального газа переводят из состояния 1 в состояние 3., как показано на рисунке. Если в состоянии 1 температура газа была равна 100 К, то в состоянии 3 она станет равной:
1) 600 К; 2) 300 К; 3) 150 К; 4) 100 К; 5) 50 К.
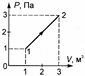 59. Если в состоянии 1 температура идеального газа была Т1, топосле осуществления процесса 1-2, изображенного на диаграмме (масса газа в ходе процесса не изменялась) его температура оказалась равной:
59. Если в состоянии 1 температура идеального газа была Т1, топосле осуществления процесса 1-2, изображенного на диаграмме (масса газа в ходе процесса не изменялась) его температура оказалась равной:
1) 3 Т1; 2) 2 Т1; 3) 4 Т1; 4) 9 Т1; 5) 8 Т1.
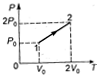 60. Если температура идеального газа в состоянии была 300 К, то после осуществления процесса 1-2, изображенного на диаграмме
60. Если температура идеального газа в состоянии была 300 К, то после осуществления процесса 1-2, изображенного на диаграмме 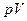 , температура газа в состоянии 2 оказалась равной:
, температура газа в состоянии 2 оказалась равной:
1) 150 К; 2) 300 К; 3) 600 К; 4) 900 К; 5) 1200 К.
61. В сосуде, закрытом подвижным поршнем, находится некоторое количество идеального газа. Газ нагревают так, что его давление изменяется прямо пропорционально объему. Если объем газа увеличился в 1,1 раза, то температура газа возросла на:
1) 30 0С; 2) 63 0С; 3) 163 0С; 4) 330 0С; 5) 363 0С.
62. Идеальный газ находится в сосуде, закрытом подвижным поршнем. Газ сжимают так, что зависимость давления от объема имеет вид, изображенный на рисунке. Если температура газа в 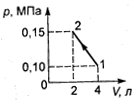 начальном состоянии равна 300 К, то в конечном состоянии она составляет:
начальном состоянии равна 300 К, то в конечном состоянии она составляет:
1) 100 К;
2) 225 К;
3) 300 К;
4) 400 К;
5) среди ответов нет правильного.
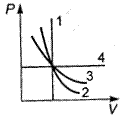 63. На рисунке представлены изотерма, адиабата, изохора и изобара идеального газа. При этом изотерма изображена линией:
63. На рисунке представлены изотерма, адиабата, изохора и изобара идеального газа. При этом изотерма изображена линией:
1) 1;
2) 2;
3) 3;
4) 4;
5) на рисунке не представлена.
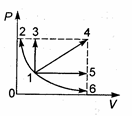 64. В каком из изображенных на рисунке процессов, проведенных с постоянной массой идеального газа, температура газа достигает наибольшей величины? Кривая 2-1-6 описывается уравнением
64. В каком из изображенных на рисунке процессов, проведенных с постоянной массой идеального газа, температура газа достигает наибольшей величины? Кривая 2-1-6 описывается уравнением 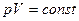 :
:
1) 1-2;
2) 1-3;
3) 1-4;
4) 1-5;
5) 1-6.
65. В каких изображенных на 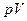 -диаграмме процессах температура идеального газа увеличивается?
-диаграмме процессах температура идеального газа увеличивается?
 1) А1 и А2;
1) А1 и А2;
2) А2 и А3;
3) А1 и А4;
4) А3 и А4;
5) А1 и А3.
66. Из приведенных ниже графиков изобарический процесс происходит с изменением параметров газа в соответствии с графиком:
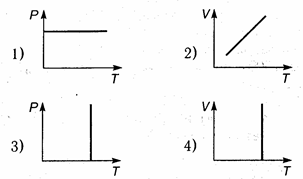
1) только 1; 2) только 3; 3) 1 и 2; 4) 1 и 3; 5) 3 и 4.
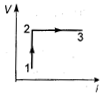 67. На рисунке приведен график зависимости изменения состояния идеального газа в координатах
67. На рисунке приведен график зависимости изменения состояния идеального газа в координатах 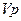 . Какой из графиков в координатах
. Какой из графиков в координатах 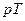 соответствует данному процессу?
соответствует данному процессу?
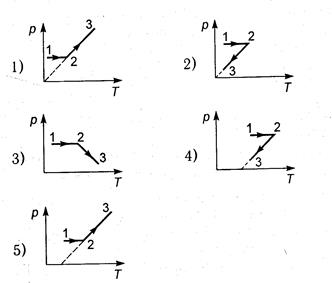
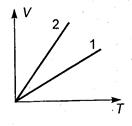 68. На диаграмме
68. На диаграмме 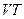 представлены два процесса изобарического нагревания при одном и том же давлении двух различных масс одного и того же идеального газа. Для масс справедливо соотношение:
представлены два процесса изобарического нагревания при одном и том же давлении двух различных масс одного и того же идеального газа. Для масс справедливо соотношение:
1) 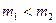 ;
;
2) 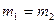 ;
;
3) 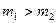 ;
;
4) 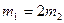 ;
;
5) соотношение может быть любым.
 69. На диаграмме
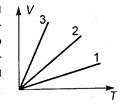
69. На диаграмме 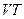 изображены зависимости объема от температуры при изобарном нагревании трех газов – кислорода, гелия и углекислого газа. Массы газов одинаковы, все три газа находятся под одним и тем же давлением. Какой график соответствует какому газу?
изображены зависимости объема от температуры при изобарном нагревании трех газов – кислорода, гелия и углекислого газа. Массы газов одинаковы, все три газа находятся под одним и тем же давлением. Какой график соответствует какому газу?
1) 1-Не, 2-О2, 3-СО2;
2) 1- СО2, 2-О, 3- Не;
3) 1-Не, 2- СО2, 3- О2;
4) 1- О2, 2- Не, 3- СО2;
5) 1- СО2, 2- Не, 3- О2.
 70. На диаграмме
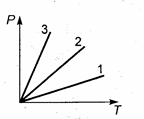
70. На диаграмме 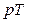 представлена зависимость давления от температуры при изохорном нагревании различных масс одного и того же газа в одинаковых по объему сосудах. Что можно сказать о массах этого газа?
представлена зависимость давления от температуры при изохорном нагревании различных масс одного и того же газа в одинаковых по объему сосудах. Что можно сказать о массах этого газа?
1) 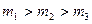 ;
;
2) 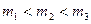 ;
;
3) 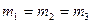 ;
;
4) при разных значениях объема зависимость может быть разная;
5) для разных газов может быть разная зависимость.
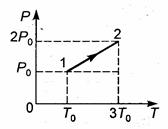 71. На диаграмме
71. На диаграмме 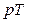 изображен процесс перехода некоторой неизменной массы идеального газа из состояния 1 в состояние 2. Соотношение между объемами газа в состоянии 1 (
изображен процесс перехода некоторой неизменной массы идеального газа из состояния 1 в состояние 2. Соотношение между объемами газа в состоянии 1 (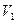 ) и состоянии 2 (
) и состоянии 2 (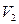 ) имеет вид:
) имеет вид:
1) 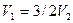 ;
;
2) 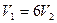 ;
;
3) 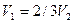 ;
;
4) 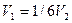 ;
;
5) 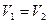 .
.
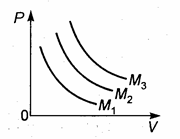 72. На рисунке изображены гиперболы для трех идеальных газов с одинаковыми массами и различными молярными массами (М1, М2, М3), находящихся при одинаковой температуре. Каково соотношение между молярными массами этих газов?
72. На рисунке изображены гиперболы для трех идеальных газов с одинаковыми массами и различными молярными массами (М1, М2, М3), находящихся при одинаковой температуре. Каково соотношение между молярными массами этих газов?
1) 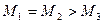 ;
;
2) 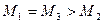 ;
;
3) 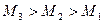 ;
;
4) 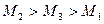 ;
;
5) 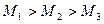 .
.
73. В цилиндре под поршнем массой 30 кг и сечением 15 см2 находится идеальный газ. Поршень располагается на высоте 3 м от дна цилиндра. Атмосферное давление 105 Па. Цилиндр помещают в лифт, движущийся с ускорением 3,75 м/с2. Если поршень может перемещаться без трения о стенки цилиндра, то он:
1) опустится на 1 м;
2) опустится на 2 м;
3) останется на месте;
4) поднимется на 1 м;
5) поднимется на 2 м.
 2015-09-07
2015-09-07 7260
7260






