Сахароза і продукти її гідролізу оптично активні, тобто здатні обертати площину поляризації поляризованого світла: сахароза має праве обертання 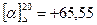 , глюкоза також праве
, глюкоза також праве 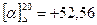 , фруктоза має ліве обертання
, фруктоза має ліве обертання 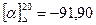 . Кут обертання еквімолекулярної суміші дорівнює алгебраїчній сумі кутів обертання глюкози і фруктози
. Кут обертання еквімолекулярної суміші дорівнює алгебраїчній сумі кутів обертання глюкози і фруктози 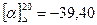 . Тому в ході реакції відбувається зменшення кута обертання площини поляризації світла реакційною сумішшю. Реакція проходить в присутності каталізатора – розчину соляної кислоти. Концентрацію розчину можна розрахувати за рівнянням:
. Тому в ході реакції відбувається зменшення кута обертання площини поляризації світла реакційною сумішшю. Реакція проходить в присутності каталізатора – розчину соляної кислоти. Концентрацію розчину можна розрахувати за рівнянням:
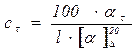 ( 6.16)
( 6.16)
Дане рівняння пов’язує концентрацію 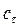 (г/100 мл) оптично активної речовини в розчині, обертання площини поляризації поляризованого світла (питоме обертання
(г/100 мл) оптично активної речовини в розчині, обертання площини поляризації поляризованого світла (питоме обертання 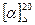 ) і довжину l (дм) поляриметричної трубки (товщина шару розчину).
) і довжину l (дм) поляриметричної трубки (товщина шару розчину).
Оскільки концентрація сахарози прямо пропорційна куту обертання площини поляризації світла, тоді вираз для константи швидкості реакції матиме вигляд:
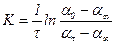 ( 6.17)
( 6.17)
де 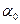 – кут обертання на момент початку реакції; ατ – кут обертання на момент часу
– кут обертання на момент початку реакції; ατ – кут обертання на момент часу 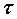 ;
; 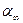 – кут обертання, що відповідає закінченню реакції.
– кут обертання, що відповідає закінченню реакції.
Таблиця 6.1
| Час від початку досліду, хв. | ατ | 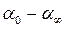
| 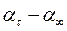
| 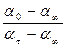
| 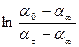
| 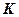
|
Знайдене значення константи швидкості реакції К порівнюють з середнім значенням константи швидкості гідролізу сахарози, одержаним аналітично.
Загальна похибка експерименту складає:
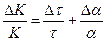 ,
,
де 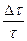 – похибка вимірювання часу;
– похибка вимірювання часу; 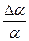 – похибка вимірювання кута обертання.
– похибка вимірювання кута обертання.
Виміри кутів обертання фіксуються за допомогою секундоміру з точністю до 1 с, що дає похибку:
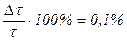 .
.
Похибка вимірювання кута обертання за допомогою поляриметра складає 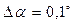 . Отже, загальна похибка буде дорівнювати:
. Отже, загальна похибка буде дорівнювати:
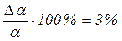 .
.
Виходячи з вище сказаного студент робить висновок, що відносна похибка визначення константи швидкості реакції дорівнює 3,1 %.
 2015-09-06
2015-09-06 415
415








