Лабораторная работа № 4
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ИЗОБАРНОЙ И ИЗОХОРНОЙ ТЕПЛОЁМКОСТЕЙ ГАЗА
Цель работы: измерение отношения изобарной и изохорной теплоемкостей воздуха.
Оборудование: экспериментальная установка ФПТ1-6н.
Краткая теория и методика выполнения работы
Удельной теплоемкостью вещества называется величина, равная количеству теплоты, которую необходимо сообщить единице массы вещества для увеличения ее температуры на один градус Кельвина:
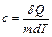 . (4.1)
. (4.1)
Теплоемкость одного моля вещества называется молярной теплоемкостью:
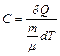 , (4.2)
, (4.2)
где m – масса, µ – молярная масса вещества, 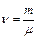 – число молей газа.
– число молей газа.
Значение теплоемкости газов зависит от условий их нагревания. В соответствии с первым законом термодинамики количество теплоты 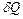 , сообщенное системе, расходуется на увеличение ее внутренней энергии
, сообщенное системе, расходуется на увеличение ее внутренней энергии 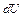 и на совершение системой работы
и на совершение системой работы 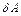 против внешних сил:
против внешних сил:
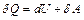 . (4.3)
. (4.3)
Изменение внутренней энергии идеального газа в случае изменения его температуры 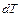 равно:
равно:
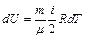 , (4.4)
, (4.4)
здесь 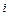 – число степеней свободы молекулы газа, под которым подразумевается число независимых координат, полностью определяющих положение молекулы в пространстве;
– число степеней свободы молекулы газа, под которым подразумевается число независимых координат, полностью определяющих положение молекулы в пространстве; 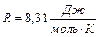 – универсальная газовая постоянная.
– универсальная газовая постоянная.
При расширении газа система совершает работу:
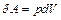 . (4.5)
. (4.5)
Если газ нагревать при постоянном объеме (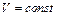 ), то
), то 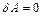 и, согласно (4.3), все полученное газом количество теплоты расходуется только на увеличение его внутренней энергии
и, согласно (4.3), все полученное газом количество теплоты расходуется только на увеличение его внутренней энергии 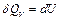 . Следовательно, учитывая (4.4), молярная теплоемкость идеального газа при постоянном объеме будет равна:
. Следовательно, учитывая (4.4), молярная теплоемкость идеального газа при постоянном объеме будет равна:
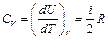 . (4.6)
. (4.6)
Если газ нагревать при постоянном давление (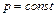 ), то полученное газом количество теплоты расходуется на увеличение его внутренней энергии
), то полученное газом количество теплоты расходуется на увеличение его внутренней энергии 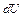 и совершение газом работы
и совершение газом работы 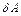 :
:
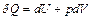 .
.
Тогда молярная теплоемкость идеального газа при постоянном давлении определяется следующим образом:
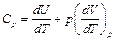 . (4.7)
. (4.7)
Используя уравнение состояния идеального газа (уравнение Клапейрона–Менделеева) 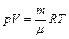 , можно показать, что для одного моля газа справедливо соотношение:
, можно показать, что для одного моля газа справедливо соотношение:
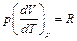 ,
,
поэтому:
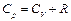 .
.
Последнее выражение называют уравнением Майера. Из него, учитывая (4.6), получаем:
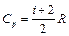 . (4.8)
. (4.8)
Отношение теплоемкостей 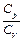 обозначают
обозначают 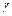 и называют показателем адиабаты или коэффициентом Пуассона:
и называют показателем адиабаты или коэффициентом Пуассона:
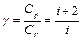 . (4.9)
. (4.9)
Адиабатным называется процесс, протекающий в термоизолированной системе, т.е. без теплообмена с окружающей средой, 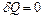 .
.
На практике он может быть осуществлен в системе, окруженной теплоизоляционной оболочкой, но поскольку для теплообмена необходимо некоторое время, то адиабатным можно считать также процесс, который протекает так быстро, что система не успевает вступить в теплообмен с окружающей средой.
Первый закон термодинамики для адиабатного процесса имеет вид 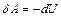 . Знак минус говорит о том, что при адиабатном процессе система может совершать работу только за счет внутренней энергии. С учетом (4.4)–(4.6) имеем:
. Знак минус говорит о том, что при адиабатном процессе система может совершать работу только за счет внутренней энергии. С учетом (4.4)–(4.6) имеем:
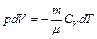 . (4.10)
. (4.10)
Продифференцировав уравнение Клапейрона–Менделеева, получим:
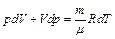 .
.
Выразим из него 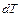 и подставим в формулу (4.10):
и подставим в формулу (4.10):
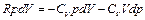 .
.
Выразив 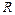 из уравнения Майера и учитывая соотношение (4.8), получим:
из уравнения Майера и учитывая соотношение (4.8), получим:
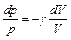 .
.
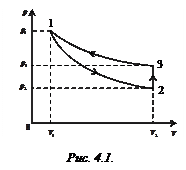 Интегрируя данное дифференциальное уравнение при условии
Интегрируя данное дифференциальное уравнение при условии 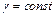 получим выражение:
получим выражение:
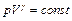 . (4.11)
. (4.11)
Уравнение (4.11) называется уравнением адиабаты или уравнением Пуассона.
Метод определения показателя адиабаты, предложенный Клеманом и Дезормом (1819 г.), основывается на изучении параметров некоторой массы газа, переходящей из одного состояния в другое двумя последовательными процессами – адиабатным и изохорным. Эти процессы на диаграмме 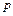 –
– 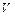 (рис. 4.1) изображены кривыми соответственно 1–2 и 2–3.
(рис. 4.1) изображены кривыми соответственно 1–2 и 2–3.
Если в сосуд, соединенный с дифференциальным датчиком давления, накачать воздух и подождать до установления теплового равновесия с окружающей средой, то в этом начальном состоянии 1 газ имеет параметры 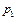 ,
, 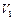 ,
, 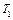 , причем температура газа в сосуде равна температуре окружающей среды
, причем температура газа в сосуде равна температуре окружающей среды 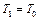 , а давление
, а давление 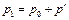 немного больше атмосферного.
немного больше атмосферного.
Если теперь на короткое время соединить сосуд с атмосферой, то произойдет адиабатное расширение воздуха. При этом воздух в сосуде перейдет в состояние 2, его давление понизится до атмосферного 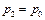 . Масса воздуха, оставшегося в сосуде, которая в состоянии 1 занимала часть объема сосуда, расширяясь, займет весь объем
. Масса воздуха, оставшегося в сосуде, которая в состоянии 1 занимала часть объема сосуда, расширяясь, займет весь объем 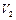 . При этом температура воздуха, оставшегося в сосуде, понизится до
. При этом температура воздуха, оставшегося в сосуде, понизится до 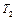 . Поскольку процесс 1–2 – адиабатный, к нему можно применить уравнение Пуассона (4.11):
. Поскольку процесс 1–2 – адиабатный, к нему можно применить уравнение Пуассона (4.11):
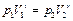 или
или 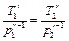 .
.
Отсюда:
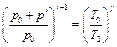 . (4.12)
. (4.12)
После кратковременного соединения сосуда с атмосферой охлажденный из-за адиабатного расширения воздух в сосуде будет нагреваться (процесс 2–3) до температуры окружающей среды 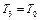 при постоянном объеме
при постоянном объеме 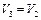 . При этом давление в сосуде поднимется до
. При этом давление в сосуде поднимется до 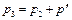 .
.
Поскольку процесс 2–3 – изохорный, к нему можно применить закон Шарля:
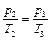 или
или 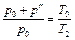 . (4.13)
. (4.13)
Из уравнений (4.12) и (4.13) получим:
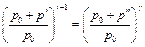 .
.
Прологарифмируем это выражение:
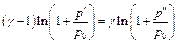 .
.
Поскольку избыточные давления 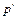 и
и 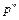 очень малы по сравнению с атмосферным давлением
очень малы по сравнению с атмосферным давлением 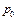 , а также учитывая, что при
, а также учитывая, что при 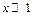
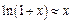 , будем иметь:
, будем иметь:
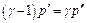 .
.
Откуда:
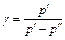 . (4.14)
. (4.14)
Избыточные давления 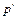 и
и 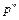 измеряют с помощью дифференциального датчика давления.
измеряют с помощью дифференциального датчика давления.
 2. Описание экспериментальной установки
2. Описание экспериментальной установки
Для определения отношения теплоемкостей воздуха 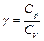 используется экспериментальная установка ФПТ1-6н, общий вид которой показан на рис. 4.2.
используется экспериментальная установка ФПТ1-6н, общий вид которой показан на рис. 4.2.
Установка состоит из металлического сосуда емкостью 3,5 литра, соединенного с компрессором, размещенным в блоке приборов 2. Компрессор включается переключателем «Компрессор», установленным на передней панели установки 5. Клапан соединения с атмосферой «Атмосфера» 6, расположенный в зоне управления 1, позволяет при повороте его по часовой стрелке до щелчка кратковременно соединить колбу с атмосферой. В информационной зоне 3 изображена принципиальная схема установки.
Давление в колбе измеряется дифференциальным датчиком давления 8. В установке также предусмотрен контроль температуры (измеритель температуры 7) как внутри колбы, так и снаружи. Подключение установки осуществляется выключателем 4.
3. Выполнение упражнений и обработка результатов измерений
1. Нарисовать таблицу 4.1.
Таблица 4.1
| № | 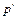 , кПа , кПа | 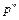 , кПа , кПа | 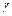 |
| … | |||
2. Включить установку тумблером «Сеть».
3. Открыть кран К1. Для подачи воздуха в сосуд включить переключатель «Компрессор».
4. С помощью измерительного прибора «Давление» контролировать давление в сосуде. Когда давление в сосуде достигнет 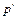 , закрыть кран К1 и отключить подачу воздуха. Значение
, закрыть кран К1 и отключить подачу воздуха. Значение 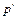 выбирается произвольно.
выбирается произвольно.
5. Подождать 2–3 мин., пока температура воздуха в сосуде сравняется с температурой окружающего воздуха 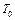 , в сосуде при этом установится постоянное давление
, в сосуде при этом установится постоянное давление 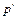 . С помощью измерителя давления снять показания давления
. С помощью измерителя давления снять показания давления 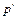 , установившегося в сосуде. Полученное значение занести в таблицу 4.1.
, установившегося в сосуде. Полученное значение занести в таблицу 4.1.
6. На короткое время соединить сосуд с атмосферой, повернув пневмотумблер «Атмосфера» по часовой стрелке до щелчка.
7. Через 2–3 мин., когда в сосуде установится постоянное давление 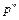 снять показания измерителя давления
снять показания измерителя давления 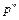 . Полученное значение занести в таблицу.
. Полученное значение занести в таблицу.
8. Повторить измерения по п.п. 2–6 не менее 10 раз при различных значениях величины 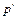 .
.
9. После окончания работы выключить установку тумблером «Сеть».
10. Для каждого измерения по формуле (4.16) определить значение показателя адиабаты 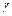 . Найти среднее значение
. Найти среднее значение 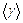 .
.
11. Оценить погрешность результатов измерения 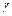 .
.
12. Рассчитать число степеней свободы молекулы воздуха, используя формулу (4.9).
13. Сравнить полученные значения 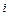 и
и 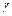 с теоретическими значениями.
с теоретическими значениями.
Контрольные вопросы
1. Какие процессы в термодинамических системах называют изопроцессами? Каким законам они подчиняются?
2. Представьте эти процессы графически в координатах 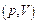 ,
, 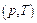 ,
, 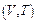 .
.
3. Сформулируйте I закон термодинамики. Запишите этот закон для изобарного, изохорного, изотермического и адиабатного процессов.
4. Дайте определение удельной и молярной теплоемкости. В каких единицах в системе СИ они измеряются.
5. Выведите формулы для расчета молярных теплоемкостей 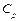 и
и 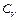 для идеального газа. Получите уравнение Майера.
для идеального газа. Получите уравнение Майера.
6. Дайте определение числа степеней свободы молекулы 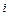 . Чему равна величина
. Чему равна величина 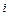 для одно-, двух-, трех- и многоатомного идеальных газов?
для одно-, двух-, трех- и многоатомного идеальных газов?
7. Какой процесс называется адиабатным? Выведите уравнение Пуассона, связывающее величины 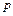 и
и 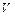 .
.
8. Рассчитайте значения показателя адиабаты для одно-, двух- и трехатомного идеальных газов.
9. В чем заключается метод Клемана и Дезорма для определения отношения 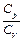 ?
?
10. Опишите рабочий цикл экспериментальной установки с помощью 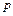 –
– 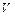 диаграммы.
диаграммы.
11. Выведите расчетную формулу (4.16) для определения 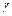 .
.
12. Как и почему изменяется температура газа в сосуде при проведении опыта?
Лабораторная работа № 5
ОПРЕДЕЛЕНИЕ КОЭФФИЦИЕНТА ДИФФУЗИИ
ПАРОВ ВОДЫ В ВОЗДУХЕ
Цель работы: определение коэффициента диффузии паров воды в воздухе.
Приборы и материалы: экспериментальная установка ФПТ1-4, термометр, секундомер, микроскоп МПБ-3, исследуемая жидкость (вода).
 2015-09-06
2015-09-06 1465
1465