В электрофлотационных установках для проведения процесса флотации используют газообразные продукты – водород и кислород, выделяющиеся на электродах при электролизе обрабатываемой воды. На катоде происходит разряд молекул воды с образованием водорода:
2Н2О + 2e- → Н2 + 2ОН-. (5.11)
На аноде процесс окисления сопровождается выделением кислорода:
2Н2О → О2 + 4Н+ + 2e-. (5.12)
Электроды выполняют в виде пластин, однако чаще их изготавливают в виде проволочной сетки из меди или нержавеющей стали. Оптимального распределения по размерам газовых пузырьков, а также газонаполнения достигают варьированием плотности тока на электродах.
В многокамерных электрофлотаторах, в одной из камер катодное пространство отделено от анодного ионообменной мембраной, водный поток направляется раздельно в анодную и катодную части камер (рис. 5.4).
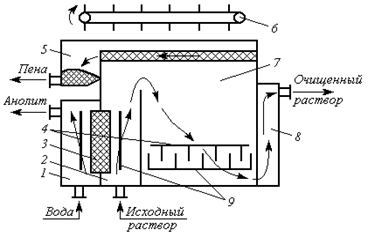
Рис. 5.4. Электрофлотатор с электрокорректором рН: 1 – анодная камера электрокорректора рН; 2 – катодная камера электрокорректора рН; 3 – анионообменная мембрана; 4 – анод; 5 – приемник пены; 6 –пеносборник; 7 – камера электрофлотационной доочистки; 8 – гидрозатвор; 9 – катод.
Исходный раствор направляется в катодное пространство первой камеры, после чего поступает во вторую – основную флотационную камеру. В катодном пространстве вследствие протекания реакции (5.11) происходит смещение равновесия в реакции диссоциации воды и изменение рН воды вплоть до значений, соответствующих образованию нерастворимых гидроксидов тяжелых металлов, присутствующих в качестве загрязняющих компонентов. Таким образом, обеспечивается электрохимическая коррекция рН вместо реагентной обработки, поэтому первую камеру называют электрокорректором рН. Для полного осаждения металлов из растворов в виде гидроксидов металлов необходимо в катодной камере поддерживать значения рН на некотором определенном уровне.
Однако катодная камера выполняет помимо указанной и другие функции:
- газонасыщение раствора, необходимое для осуществления флотационного процесса;
- обессоливание раствора вследствие миграции анионов в анодную камеру;
- образования гидроксидов катионов металлов.
Наиболее важной функцией является все же изменение кислотности обрабатываемого раствора в катодном пространстве, поэтому необходимая токовая нагрузка в корректоре рН должна определяться исходя из функции:
Q = F(C Me + K), (5.13)
где Q – удельный расход электричества, А·ч/л; C Me – концентрация ионов металлов (г-экв/л); K – константа, зависящая от содержания других примесей в растворе; F – число Фарадея (26,8 А·ч).
Эффект обессоливания за счет удаления анионов в анодную камеру может быть определен из выражения:
С ан = t ан(С Me + K), (5.14)
где С ан – изменение концентрации анионов в растворе при переносе их через анионообменную мембрану; t ан – селективность анионообменной мембраны, доли единицы (t ан = 0,8÷0,9); С Me и K – то же, что и в выражении (5.13).
Изменение кислотности анионита может быть определено из выражения:
[H+] = (Q 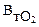 )/F, (5.15)
)/F, (5.15)
где Q – удельный расход электричества, А·ч/л; 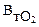 – выход по току реакции образования кислорода на аноде; F – число Фарадея (26,8 А·ч).
– выход по току реакции образования кислорода на аноде; F – число Фарадея (26,8 А·ч).
 2015-10-13
2015-10-13 1643
1643