Лабораторная работа
Перманганатный метод определения окисляемости
(применим для текущего ориентировочного определения
содержания органических примесей)
4.1. Сущность метода заключается в измерении избытка окислителя (перманганата калия) после окисления им веществ, присутствующих в пробе исследуемой воды в серно - кислой или щелочной среде при кипячении.
Метод можно использовать только для проб, окисляемость которых ниже 100мг О /дм3.
4.2. Приготовление рабочих растворов
4.2.1. Калий марганцовокислый, раствор концентрации с (1/5КМnО4) = 0,1моль/дм3 готовят из фиксанала, а в случае его отсутствия из марганцовокислого калия. В плоскодонную колбу вместимостью 4-5дм3 вливают 3дм3 дистиллированной воды, всыпают 1г марганцовокислого калия и, нагрев до кипения, кипятят 2-3ч. Прекратив кипячение, закрывают колбу пробкой с отверстием, в которое вставлена хлор - кальциевая трубка, заполненная ватным тампоном для задержания пыли из проникающего в колбу при охлаждении воздуха. Через 2-3 суток осторожно сливают отстоявшийся от мелких частиц оксидов марганца раствор в чистую склянку с хорошо пришлифованной пробкой.
Для установления титра приготовленного раствора в несколько чистых конических колб отмеривают из бюретки вместимостью 50см3 со стеклянным краном различные объемы этого раствора (например, по 5 и 7см3). Затем в каждую колбу вливают дистиллированную воду примерно до 50см3, по 10см3 раствора серной кислоты и по 10см3 титрованного раствора щавелевой кислоты концентрации с (1/2 Н2С2О4∙2Н2О)=0,1моль/дм3 или щавелевокислого натрия. После полного обесцвечивания жидкостей в колбах избыток оксалат-ионов от титровывают раствором перманганата калия из упомянутой бюретки до появления весьма слабого, но не исчезающего, розового окрашивания.
Поправочный коэффициент К раствора калия марганцовокислого концентрации точно с (1/5 КМnО4)=0,1моль/дм3 вычисляют по формуле:
К= 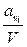 , (4)
, (4)
где ащ – количество раствора щавелевой кислоты или щавелевокислого натрия, введение в колбу, см3;
V – общий объем раствора перманганата, израсходованный на титрование, см3.
Раствор устойчив длительное время, его хранят в защищенном от света месте в хорошо закупоренной склянке.
Этим раствором пользуются для приготовления рабочего раствора концентрации с (1/5 КМnО4)=0,01моль/дм3. Для этого отбирают пипеткой объем Х (см3) этого раствора в мерную колбу вместимостью 1дм3, доливают до метки дистиллированной водой и перемешивают. Рабочий раствор пригоден в течение недели. Объем Х (см3) определяют по формуле
Х= 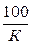 , (5)
, (5)
Его отмеривают из бюретки вместимостью 100см3.
4.2.2. Раствор щавелевой кислоты концентрации с (1/2 Н2С2О2·Н2О)=0,1 моль/дм3 или щавелевокислого натрия. Раствор щавелевой кислоты готовят из фиксанала, а в случае его отсутствия из щавелевокислого натрия. Для этого отвешивают точно 6,701г щавелевокислого натрия, выдержанного в течение 1ч в сушильном шкафу при 1100С, и растворяют это количество в мерной колбе вместимостью 1дм3 в дистиллированной воде. После полного растворения доливают жидкость в колбе до метки дистиллированной водой и хорошо перемешивают.
Растворы щавелевой кислоты и щавелевокислого натрия устойчивы, их хранят в хорошо закупоренной склянке в защищенном от света месте. Этими растворами пользуются для проверки титра калия марганцовокислого концентрации с (1/5 КМnО4)=0,1моль/дм3.
Рабочий концентрации с (1/5 КМnО4)=0,01моль/дм3 готовят разбавлением точно в десять раз. Рабочие растворы не устойчивы, их следует готовить на срок не более 10 суток.
4.2.3. Раствор серной кислоты концентрации с (1/2 Н2 SО4)=10моль/дм3. К 1дм3 дистиллированной воды малыми порциями осторожно приливают 400см3 концентрированной химически чистой серной кислоты. После полного остывания жидкости ее переливают в склянку с хорошо пригнанной пришлифованной пробкой. Реактив устойчив.
4.3. Проведение анализа
В коническую колбу вместимостью 250, 300см3 отбирают измеренный объем анализируемой воды, отфильтрованной от взвешенных веществ. Если предполагают, что вода сильно загрязнена органическими примесями, то отбирают не более 5см3, если воды менее загрязнены – до 20см3, а малозагрязненные воды – 100см3. Объем жидкости в колбе доливают дистиллированной водой до 100см3, приливают 10см3 серной кислоты (по п.4.2.3), нагревают до начинающегося кипения и приливают точно 10см3 раствора перманганата калия (по п.4.2.1). Кипятят точно 10мин, после чего вводят точно 10см3 раствора щавелевой кислоты или щавелево-кислого натрия (по п.4.2.2). Для равномерного и спокойного кипения в колбу помещают тонкие запаянные с одного конца капилляры или мелкие стеклянные шарики. Обесцветившуюся жидкость титруют из бюретки раствором на калия марганцовокислого концентрации с (1/5 КМnО4)=0,01моль/дм3 (по п.4.2.1) до слабой, но не исчезающей, розовой окраски. Если при кипячении жидкость приобрела бурую окраску или в ней образовался коричневый осадок, то определение повторяют, отобрав меньший объем анализируемой воды. Одновременно проводят определение со 100см3 дистиллированной воды таким же порядком. Определение окисляемости проводят в 2-3 параллельных пробах, расхождения между которыми не должны превышать 0,25мг кислорода.
4.4 Обработка результатов анализа
Перманганатная окисляемость (Оn) определяется в миллиграммах окислителя (кислорода), расходуемых на кубический дециметр воды по формуле:
(Оn)= 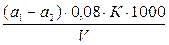 , (6)
, (6)
где а1 – расход раствора перманганата калия на титрование пробы анализируемой воды, см3;
а2 – расход раствора перманганата калия на титрование пробы дистиллированной воды, см3;
V – объем анализируемой воды, отобранный для определения, см3;
К – поправочный коэффициент раствора калия марганцово-кислого концентрации точно с (1/5 КМnО4)=0,01моль/дм3;
0,08 – количество кислорода, отвечающее 1см3 этого раствора, мг;
1000 – пересчет расхода окислителя (кислорода) к 1дм3.
Среднеарифметические расхождения между параллельными определениями а1 не должны превышать 0,25см3, что соответствует 0,02мг кислорода.
Форма журнала записи результатов анализа приведена в приложении Б ОСТ 34-70-953.3-88;
 2015-10-13
2015-10-13 797
797







